微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
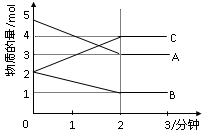
1、填空题 (12分)某可逆反应从0―2分钟进行过程中, 在不同反应时?间各物质的量的变化情况如下图所示。则该反应的的反应物是??????,生成物是???????,化学方程式为?????????????????????????????;反应开始至2分钟时,能否用C表示反应速率?若能,其反应速率为??? _____?????,若不能,则其原因为?????????? _???????????? ________________???????????????;2分钟后A、B、C各物质的量不再随时间的变化而变化,说明在这个条件下,反应已达到了 ____??????状态。
参考答案:A和B;C;2A+B 本题解析:
本题解析:
试题分析:根据图示可知:在反应中A、B减少,C增加。所以A、B是反应物,C是生成物。它们反应时的物质的量的比为2:1:2,最终达到平衡。所以化学反应方程式是2A+B 2C;反应开始至2分钟时,由于只知道物质的量的变化,而不知道容器的容积,所以不能否用C表示反应速率。2分钟后A、B、C各物质的量不再随时间的
2C;反应开始至2分钟时,由于只知道物质的量的变化,而不知道容器的容积,所以不能否用C表示反应速率。2分钟后A、B、C各物质的量不再随时间的
本题难度:一般
2、填空题 氢能以其洁净、高效、高热值、环境友好等特点成为最有前途的新能源,制氢和储氢方法很多。
(1)直接热分解法制氢
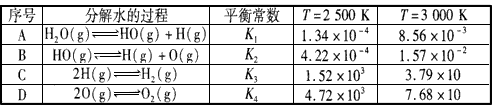
①属于吸热反应的是___(选填:A、B、C、D)。
②某温度下,H2O(g)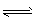 H2(g)+1/2O2(g),平衡常数K=___(用含K1、K2、K3、K4的式子表示)。
H2(g)+1/2O2(g),平衡常数K=___(用含K1、K2、K3、K4的式子表示)。
(2)热化学循环制氢
已知:
Br2(g)+CaO(s)=CaBr2(s) +1/2O2(g) △H= -73 kJ/mol
3FeBr2(s)+4H2O(g)=Fe3O4(s)+6HBr(g)+H2(g) △H=+384 kJ/mol
CaBr2(s)+H2O(g)=CaO(s)+2HBr(g) △H=+212 kJ/mol
Fe3O4(s) +8HBr(g)=Br2(g)+3FeBr2(s)+4H2O(g) △H= -274 kJ/mol
则:H2O(g)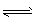 H2 (g) +1/2O2 ( g) △H=-___kJ/mol。
H2 (g) +1/2O2 ( g) △H=-___kJ/mol。
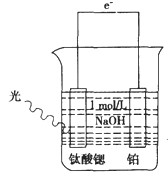
(3)光电化学分解制氢 光电化学分解制氢原理如图所示。钛酸锶光电极的电极反应为
4OH-+ 4hv-4e-→O2↑+2H2O,则铂电极的电极反应为___。
(4)生物质制氢
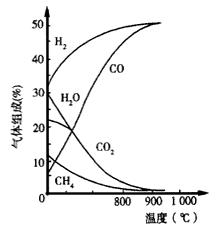
若将生物质气化炉中出来的气体[主要有CH4、CO2、H2O(g)、CO及 H2]在1. 01×105 Pa下,通入转换炉,改变温度条件,各成分的体积组成关系如图所示。下列有关图象的解读正确的是__。
A.利用CH4与H2O(g)及CO2转化为合成气CO和H2,理论上是可行的
B.CH4(g)+CO2(g)→2CO(g)+2H2(g)和CH4(g) +H2O(g)→ CO(g)+3H2(g),都是放热反应
C.CH4与CO2及H2O(g)转化为合成气CO和H2的适宜温度约为 900℃
D.图象中曲线的交点处表示反应达到平衡
(5) LiBH4由于具有非常高的储氢能力,分解时生成氢化锂和两种单质,试写出反应的化学方程式______。
参考答案:(1)①AB
②K1・K2・ K3・K41/2
本题解析:
本题难度:一般
3、选择题 为了说明影响化学反应快慢的因素,甲、乙、丙、丁四位学生分别设计了如下A~D四个实验,你认为结论不正确的是
A.将铜片放入稀硫酸中,无现象。若再向所得的溶液中加入硝酸银溶液,一段时间后,由于形成原电池,可看到有氢气产生
B.在相同条件下,等质量的大理石块和大理石粉与相同的盐酸反应,大理石粉反应快
C.将浓硝酸分别放在冷暗处和强光照射下,会发现光照可以加快浓硝酸的分解
D.两支试管中分别加入相同质量的氯酸钾,其中一支试管中再加入少量二氧化锰,同时加热,产生氧气的快慢不同
参考答案:A
本题解析:
试题分析:A.将铜片放入稀硫酸中,无现象。若再向所得的溶液中加入硝酸银溶液,Cu与AgNO3溶液会发生置换反应,产生Ag和Cu(NO3)2,而不是过程原电池,反应原理有误,错误。B.在相同条件下,等质量的大理石块和大理石粉与相同的盐酸反应,大理石粉由于与盐酸的接触面积增大,所以反应速率比块状的快,反应原理无误,正确;C.浓硝酸光照容易分解,所以将浓硝酸分别放在冷暗处和强光照射下,会发现光照可以加快浓硝酸的分解,反应原理无误,正确;D.两支试管中分别加入相同质量的氯酸钾,其中一支试管中再加入少量二氧化锰,同时加热,由于二氧化锰是氯酸钾分解的催化剂,因此产生氧气的速率加入少量二氧化锰的比没有加入的快,反应原理无误,正确。
考点:考查反应原理的正误判断的知识。
本题难度:一般
4、选择题 氙气和氟气按一定比例混合,在一定条件下可直接反应达到如下平衡


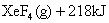
下列变化既能加快反应速率又能使平衡向正反应方向移动的是(???)
A.升高温度
B.加压
C.减压
D.适当降温
参考答案:B
本题解析:加压可以加快反应速率,同时由于反应是一个体积减小的反应,因此加压能够使反应向正方向移动。
本题难度:简单
5、选择题 下列各组实验中最先出现浑浊的是( )
| 实验 | 反应温度/℃ | Na2S2O3溶液 | 稀H2SO4 | H2O
V/mL
c/(mol?L-1)
V/mL
c/(mol?L-1)
V/mL
A
25
5
0.1
10
0.1
5
B
25
5
0.2
5
0.2
10
C
35
5
0.1
10
0.1
5
D
35
5
0.2
5
0.2
10
A.A
B.B
C.C
D.D
参考答案:对于该反应来说浓度越大,温度越高,反应速率越大,表中C、D温
本题解析:
本题难度:一般
|