微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、实验题 我国规定饮用水的硬度不能超过25度。硬度的表示方法是:将水中的Ca2+和Mg2+都看作Ca2+,并将其折算成CaO的质量。通常把1升水中含有10 mg CaO 称为1度。某化学实验小组对本地区地下水的硬度进行检测
实验中涉及的部分反应:
M2+(金属离子)+Y4-(EDTA)=MY2-
MEBT+Y4-(EDTA)=MY2++EBT(铬黑T)
实验过程如下:
(1)取地下水样品25.0mL进行预处理。已知水中由Ca2+、Mg2+和HCO3-所引起的硬度称为暂时硬度,可通过加热减小硬度,写出加热时所发生的化学反应(任写一个)____________________。预处理的方法是向水样中加入浓盐酸,煮沸几分钟,煮沸的目的是______________。
(2)将处理后的水样转移到250 mL的锥形瓶中,加入氨水一氯化铵缓冲溶液调节pH为10,滴加几滴铬黑T溶液,用0.010 0 mol/L的Y4-(EDTA)标准溶液进行滴定,滴定时眼睛应_______________,滴定终点时的实验现象是_______________
(3)滴定终点时共消耗Y4-(EDTA)溶液15.0mL,则该地下水的硬度是____。
(4)若实验时装有Y4-(EDTA)标准液的滴定管只用蒸馏水洗涤而未用标准液润洗。则测定结果将____(填“偏大”“偏小”或“无影响”)。
2、实验题 石灰石的主要成份是碳酸钙,此外还有?SiO2?、?Fe2O3、?Al2O3等杂质。测定石灰石中钙元素的质量百分含量的流程图如下:
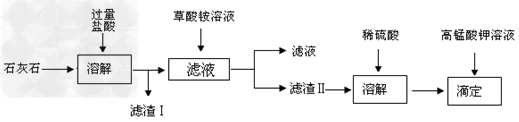
已知:草酸(H2C2O4)是一种二元弱酸。
(1)滤渣Ⅰ的成分是_________,该物质溶于氢氧化钠溶液的化学方程式为__________________________。
(2)请写出生成滤渣Ⅱ(CaC2O4・H2O)的离子方程式____________________。
(3)加入的(NH4)2C2O4?溶液要求是饱和的,其原因是____________。不仅如此,在加入饱和(NH4)2C2O4?溶液后,还需要向溶液中滴加氨水,其原因是_______________?。
(4)将草酸钙沉淀?(CaC2O4・H2O),用硫酸溶解,用a?mol/L的标准高锰酸钾溶液滴定生成的草酸,发生化学反应:H2C2O4?+?MnO4-?+?H+?→??Mn2+?+?CO2??↑+?H2O(未配平),其中还原剂是___________。若开始取用样品的质量为m?g,硫酸溶解后所得草酸溶液的体积为100mL,每次取25.00mL进行滴定,达到滴定终点时所耗KMnO4溶液体积为?b?ml(三次平均值),所得草酸溶液的物质的量的浓度是____________?;石灰石中钙元素的质量百分含量为_________。(相对原子质量:Ca-40)
3、选择题 下列实验目的能实现的是 [???? ]
A.用托盘天平称取3.23固体
B.用50的量筒量取30.12的水
C.向小试管中加入100mL稀盐酸
D.用滴管取约1mL溶液
4、选择题 医生建议因缺少某种元素而患甲状腺肿大的病人多食海带,这是由于海带中含有较丰富的( )
A.碘元素
B.钙元素
C.钾元素
D.锌元素
5、简答题 某白色固体可能是Na2SO3、Na2SO4、Na2CO3中的两种或三种,化学兴趣小组在实验室对该固体进行探究:取少量固体滴加稀硫酸并将产生的气体通入澄清的石灰水后出现浑浊.一位同学由此得出该固体一定含有Na2CO3的结论.
(1)请指出该结论是否合理并说明理由______.
(2)请完成对该固体的探究:
①提出合理假设
假设1:______;假设2:______;假设3:______.
假设4:含有Na2SO3、Na2SO4和Na2CO3
②基于假设,设计出实验方案,在答题卷中画出装置图并描述实验操作、预期的实验现象和结论.