微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
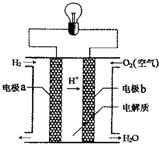
1、选择题 氢氧燃料电池可以使用在航天飞机上,其反应原理示意图如右图.下列有关氢氧燃料电池的说法正确的是( )
A.该电池工作时电能转化为化学能
B.该电池中电极a是正极
C.外电路中电子由电极b通过导线流向电极a
D.该电池的总反应:2H2+O2=2H2O
2、选择题 目前已研制成功多种锂电池。某种锂电池的总反应式为Li+MnO2=LiMnO2,下列说法正确的是(? )。
A.Li是正极,电极反应为Li-e-=Li+
B.Li是负极,电极反应为Li-e-=Li+
C.Li是负极,电极反应为MnO2+e-=Mn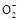
D.Li是负极,电极反应为Li-2e-=Li2+
3、选择题 在盛有饱和Na2CO3溶液的烧杯中,插入惰性电极,保持温度不变,通电一定的时间后,下列判断正确的是
A.溶液的pH将增大
B.Na+数和CO32-数的比值将变小
C.溶液浓度不变,有晶体析出
D.溶液浓度逐渐增大并有晶体析出
4、选择题 将纯锌片和纯铜片按下图示方式插入同浓度同体积的稀硫酸中一段时间,以下叙述正确的是
 [???? ]
[???? ]
A.两烧杯中铜片表面均无气泡产生
B.甲中铜片是正极,乙中铜片是负极
C.两烧杯中溶液的pH均增大
D.产生气泡的速度甲比乙慢
5、填空题 硫-碘循环分解水制氢主要涉及下列反应:
Ⅰ.SO2+2H2O+I2=H2SO4+2HI???? Ⅱ. 2HI H2+I2(g)?
H2+I2(g)?
Ⅲ. 2H2SO4=2SO2+O2+2H2O
(1)分析上述反应,下列判断正确的是??????。
a.反应Ⅲ易在常温下进行??????
b.反应Ⅰ中SO2氧化性比HI强
c.循环过程中需补充H2O????
d.循环过程中产生1 mol O2的同时产生1 mol H2
(2)一定温度下,向1 L密闭容器中加入1 mol HI(g),发生反应Ⅱ,H2物质的量随时间的变化如右图所示。那么,0~2 min内的平均反应速率:υ(HI)=???????????????????。
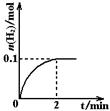
相同温度下,若开始加入HI(g)的物质的量是原来的2倍,则???是原来的2倍。
a.压强???????????????b.HI的平衡浓度???
c.达到平衡的时间?????d.平衡时H2的体积分数
(3)用足量Zn和一定量的硫酸制取H2,反应时溶液中水的电离
(H2O H++OH-)平衡?????移动(填“向左”“向右”或者“不”);若要减小产生H2的速率而又不影响产生H2的总量,应向硫酸中加入下列试剂中的??????。
H++OH-)平衡?????移动(填“向左”“向右”或者“不”);若要减小产生H2的速率而又不影响产生H2的总量,应向硫酸中加入下列试剂中的??????。
a.Na2CO3溶液??b.K2SO4溶液? c.NaNO3溶液?d.水??e.CuSO4溶液
(4)以H2为燃料制成燃料电池,若:2H2(g)+O2(g)=2H2O(l) ΔH=-572 kJ/mol,
当电池释放228.8 kJ电能时,生成1 mol液态水,该电池的能量转化率为????。