B����˵�����������������������ǿ
C������Ӳ������ӣ�ԭ�Ӱ뾶��������ԭ����ǿ
D����Li��Na��K��Rb��Cs�������۷е����ߣ��ܶ�����
�ο��𰸣�B
�����������
�����Ѷȣ���
2��ѡ���� ����˵����ȷ����
A����������NaӦ������ˮ��
B������ȡ�ķ����ɳ�ȥˮ�е�Cl������
C��Na2SiO3��ҺӦ�����ڴ����������Լ�ƿ��
D�������ˮ�еμ�FeCl3������Һ�ķ�������Fe(OH)3����
�ο��𰸣�D
���������A����������NaӦ������ú���У�����ˮ��Ӧ�ʲ��ܱ�����ˮ�У�A����
B���ó����ķ����ɳ�ȥˮ�е�Cl�����ӣ�����ȡ�ķ����ɳ�ȥˮ�е��������ӣ�B����
C��Na2SiO3��Һ�Լ��ԣ������ò�������Ӧ��������C����
D��Fe(OH)3������Ʊ���������FeCl3��Һ�����ˮ�С�D��ȷ��
��ѡD
�����Ѷȣ�һ��
3��ѡ���� ����(Na2CO3) �����������о��й㷺����;��������ʵ����ģ���Ƽ�ԭ����ȡNa2CO3������ͼ��
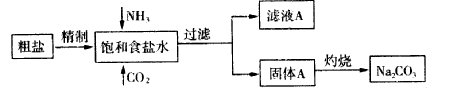
��֪����ʳ��ˮ��ͨ��NH3��CO2�����ķ�ӦΪNaCl+NH3+CO2+H2O��NaHCO3��+NH4Cl����ش��������⣺
��1�������к��е�����������Ca2+��Mg2+��SO42-�ȡ�
���Ƴ��ӵIJ���˳��a��_______��________��________��b(����ĸ��ţ���
a�������ܽ⣬��ȥ������
b�����������pH��
c������Ba(OH) 2��Һ��
d������Na2CO3��Һ��
e������
��ʳ��ˮ����ͨ��NH3����ͨ��CO2��������_____________________��
��2�����չ���A��Na2CO3Ӧ��_____������ĸ��ţ��н��С�
a����������b��������c���ձ�����d����ƿ
֤����ҺA�к���NH4+�ķ���������������������������������ҺA�����ؽᾧ�ܹ����NH4HCO3����pH=13��Na+��K+����Һ�м�������NH4HCO3��ʹpH���ͣ���Ӧ�����ӷ���ʽ______________________��
��3����ͼװ���г�����ʵ�����Ʊ�CO2����_____(����ĸ��ţ�����bʾ���װ���Ʊ�NH3ʱ����Һ©����ʢ�ŵ��Լ�______(���Լ����ƣ�����ƿ�ڿɼ���Ĺ����Լ����������������Լ����ƣ���
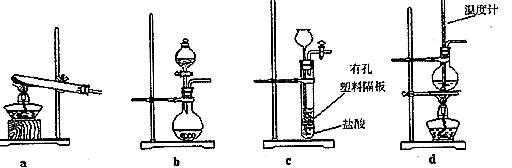
��4��һ����Ȼ���ɷ���aNa2CO3��bNa2SO4��cH2O��ijͬѧ���������ṩ���Լ�����������¼����ⶨNa2CO3������������ʵ�鷽�������ʵ�鷽������������������ѡ����
��ѡ����Լ���1��0 mol��L-1H2SO4��Һ��1��0 mol��L-1BaCl2��Һ��ϡ��ˮ����ʯ�ҡ�Ca(OH) 2��Һ������ˮ
�ٳ�ȡm1 gһ������Ȼ�����Ʒ��������������ˮ�У�
��_________________________________________________________________��
��_________________________________________________________________��
�ܼ�����Ȼ����к�Na2CO3������������
�ο��𰸣���1��c��d��e��2�֣���NH3������ˮ�������������ܽ�Ȳ�
���������
�����������1�����⿼�����ʵķ����ᴿ��Ϊ��֤�������ӳ����������Լ�Ҫ�����������������ں��������б����ȥ�����������Ϣ֪���������Ba(OH) 2��Һ�ɳ�ȥSO42-��Mg2+���������Na2CO3��Һ�ɳ�ȥCa2+������Ba2+�����˺������ܳ�ȥ������CO32����OH����Һ������Ӧ�ȼ�Ba��OH��2��Һ�ټ�Na2CO3��Һ�����ˣ����������ᣬ���Ƴ��ӵIJ���˳��c��d��e��NH3��������ˮ�������������ܽ�Ȳ����CO2��������ʳ��ˮ����ͨ��NH3����ͨ��CO2����2�����չ���Ӧ������
�����Ѷȣ�һ��
4������� �п��Ľ���Na��¶�ڿ����У���仯�������£�

��1����Ӧ��ķ�Ӧ�����������仯�Ĺ�ϵ���£�
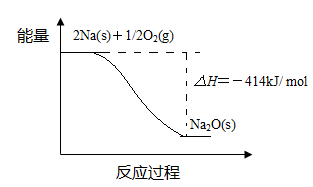
�� ��Ӧ�� ���� ����Ӧ������ȡ������ȡ������ж���������������
�� 1 mol Na(s)ȫ��������Na2O(s)���Ȼ�ѧ����ʽ����������
��2����Ӧ����Na2O��ˮ�ķ�Ӧ�������ĵ���ʽ��?????��
��3����ɫ��ĩΪNa2CO3����������ˮ����Ϊ0.1 mol/L Na2CO3��Һ������˵����ȷ����?????������ĸ����
A�������¶ȣ���Һ��pH����
B��c(OH��)��c (H��)��c (HCO3��)��2 c (H2CO3)
C����������NaOH���壬c (CO32�D)��c (Na��)������
D��c (Na��) > c (CO32�D) > c (HCO3�D) > c(OH�D) > c (H��)
��4�� �Ƶ�ص��о�������һ���̶��Ͽɻ��������Դ��ȱ�����ĵ�ط�չ�������⡣
�� �Ʊ�﮻��ã���ԭ�ӽṹ����ԭ��_______��
��ZEBRA �����һ���Ƶ�أ��ܷ�ӦΪNiCl2 + 2Na  ?Ni + 2NaCl����������Ӧʽ��_____�� ?Ni + 2NaCl����������Ӧʽ��_____��
�ο��𰸣���1���ٷ���????��Ӧ������������������������
��
���������
�����������1�������ڷ�Ӧ�������������������������ߣ����Է����ķ�Ӧ���Ƿ��ȷ�Ӧ���� ����Ŀ�ṩ��������ϵ�ɵø÷�Ӧ���Ȼ�ѧ����ʽΪ��Na(s)��1/4O2(g)��1/2Na2O(s) ��H����207 kJ/ mol����2����Ӧ����Na2O��ˮ�ķ�Ӧ��Na2O��ˮ��Ӧ����NaOH����Ӧ�ķ���ʽΪNa2O��H2O =2NaOH��NaOH�ĵ���ʽΪ��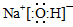 �����Ѷȣ�һ�� �����Ѷȣ�һ��
5��ѡ���� �±��У��Գ��������ȷ�Լ������Ƿ���������ϵ���ж϶���ȷ���ǣ�������
ѡ��
| ������
| ������
| �ж�
| A
| ̼���ơ�̼���������ó���ʯ��ˮ����
| Na2CO2�������ʯ��ˮ��Ӧ���ɰ�ɫ��������NaHCO3����
| ��ԣ�
��ԣ���
| B
| ��Na2O2��ˮ��Һ�е����̪���ɫ
| Na2O2��ˮ��Ӧ������������
| ��ԣ�
�������
| C
| �����ƾ���ǿ��ԭ��
| ��ѹ�ƵƷ�������ǿ�Ļƹ�
| ��ԣ�
��ԣ���
| D
| ��̪��Һ��̼������Һ�е���ɫ����̼��������Һ����
| CO32��ˮ��̶ȴ���HCO3��
| ��ԣ�
��ԣ���
�ο��𰸣�D
���������
���������A�������������������ó���ʯ��ˮ����NaHCO3Ҳ��Ca(OH)2��Ӧ������ɫ������B�������ȫ�棬Ӧ�ȱ�����ɫ��C�����֮��û�������ϵ��D�������˵��Na2CO3��Һ����ǿ��NaHCO3��Һ����������������ϵ����D��ȷ��
�����������Ѷ����У�����ȫ�棬�Ƚ�ѵ��ѧ������˼ά������
�����Ѷȣ�һ��
|
|