微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 已知温度越高,AgI在水中的溶解度越大,现向有AgI固体的AgI饱和溶液中分别进行如下操作,有关离子浓度的变化情况是:
(1)若加入少量水,则c(I-)______(填“增大”、“减小”或“不变”)
(2)若加入AgNO3固体,则AgI在水中的溶解度______(填“增大”、“减小”或“不变”)
(3)若加入NaCl固体,则AgI的溶度积Ksp______(填“增大”、“减小”或“不变”)
(4)若某温度下,AgI的溶度积Ksp=9.0×10-20,则AgI在该温度下的溶解度是______g(AgI饱和溶液的密度可近似为1g?mL-1).
参考答案:在一定温度下,向AgI的饱和溶液中存在沉淀溶解平衡,AgI(
本题解析:
本题难度:简单
2、选择题 已知25℃,Fe(OH)3(s) Fe3+(aq)+3OH-(aq),Ksp;Fe3+(aq)+3H2O(l)
Fe3+(aq)+3OH-(aq),Ksp;Fe3+(aq)+3H2O(l) Fe(OH)3(s)+3H+(aq),Kh;水的离子积常数为Kw。下列Ksp、Kh、Kw的关系是( )
Fe(OH)3(s)+3H+(aq),Kh;水的离子积常数为Kw。下列Ksp、Kh、Kw的关系是( )
A.Kh/Kw=Ksp
B.Ksp・Kw=Kh
C.Ksp・Kh=(Kw)3
D.Kw/Kh=(Ksp)3
参考答案:C
本题解析:
试题分析:根据Ksp=c(Fe3+)c(OH-)3, Kh= c(H+)3/ c(Fe3+),Kw= c(H+) c(OH-),所以三者的关系是Ksp・Kh=(Kw)3,答案选C。
考点:考查常数表达式之间的换算关系
本题难度:一般
3、选择题 下列叙述错误的是
A.在加热搅拌条件下加入MgO,可除去MgCl2溶液中的Fe3+
B.pH=4.5的番茄汁中c(H+)是pH=6.5的牛奶中c(H+)的100倍
C.常温下,CH3COONa和CH3COOH的混合溶液中(pH=7):c(Na+)=c(CH3COO-)>c(CH3COOH)>c(H+)=c(OH-)
D.常温下,Cd(OH)2和Co(OH)2的混合悬浊液中,c(Cd2+)是c(Co2+)的3.5倍。已知:KSP(Cd(OH)2)=7.2×10-15, KSP(Co(OH)2)=1.8×10-15
参考答案:D
本题解析:
试题分析:A.在加热搅拌条件下加入MgO,调节溶液的pH同时不会引入杂质,因此可除去MgCl2溶液中的Fe3+,A正确;B.pH=4.5的番茄汁中c(H+)是pH=6.5的牛奶中c(H+)的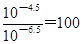 倍,B正确;C.常温下,CH3COONa和CH3COOH的混合溶液中(pH=7),根据得失守恒可知溶液中c(Na+)=c(CH3COO-)>c(CH3COOH)>c(H+)=c(OH-),C正确;D.常温下,Cd(OH)2和Co(OH)2的混合悬浊液中,
倍,B正确;C.常温下,CH3COONa和CH3COOH的混合溶液中(pH=7),根据得失守恒可知溶液中c(Na+)=c(CH3COO-)>c(CH3COOH)>c(H+)=c(OH-),C正确;D.常温下,Cd(OH)2和Co(OH)2的混合悬浊液中, ,即c(Cd2+)是c(Co2+)的4倍,D错误,答案选D。
,即c(Cd2+)是c(Co2+)的4倍,D错误,答案选D。
考点:考查pH计算、离子浓度比较以及溶解平衡等
本题难度:困难
4、选择题 已知H2CrO4是弱酸,在一饱和Ag2CrO4水溶液(含有Ag2CrO4固体)中,添加下列试剂能使c(CrO42-)减少的是 [???? ]
A. NH3
B. 硝酸
C. 水
D. AgNO3
参考答案:BD
本题解析:
本题难度:一般
5、选择题 已知锌及其化合物的性质与铝及其化合物相似。如图,横坐标为溶液的pH,纵坐标为Zn2+离子或[Zn(OH)4]2-离子的物质的量浓度(假设Zn2+离子浓度为10-5mol・L-1时,Zn2+离子已沉淀完全)。下列说法不正确的是????
 [???? ]
[???? ]
A.往ZnCl2溶液中加入足量的氢氧化钠溶液,反应的离子方程式可表示为: Zn2++4OH-=[Zn(OH)4]2-
B.从图中数据计算可得Zn(OH)2的溶度积Ksp=10-17 mol3・L-3
C.某废液中含Zn2+离子,沉淀Zn2+离子可以控制溶液pH的范围是8~12
D.向1L1?mol・L-1 ZnCl2溶液中加入NaOH固体至pH=7,需NaOH?2mol
参考答案:D
本题解析:
本题难度:一般