微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 现有等浓度的下列溶液:①CH3COOH?②HCl??③Na2CO3?④NaHCO3?⑤FeCl3??按溶液pH由小到大排列正确的是
A.①②⑤④③
B.②①⑤④③
C.⑤②①④③
D.①④③②⑤
参考答案:B
本题解析:略
本题难度:一般
2、选择题 能说明0.1 mol・L-1的NaHA溶液一定呈酸性的是
①稀释时,溶液中c(OH-)增大 ②溶液的pH<7 ③溶液中c(Na+)=c(A2-) ④溶液可与等体积等物质的量浓度的NaOH溶液恰好反应
A.①②③④
B.①③④
C.①③
D.②④
参考答案:C
本题解析:①分析知NaHA溶液不可能 呈中性,溶液呈碱性(或酸性),稀释时溶液的碱性(或酸性)都应该减弱,现溶液中c(OH-)增大,则溶液中c(H+)减小,酸性减弱,故溶液呈酸性;②因温度不确定,故pH<7的溶液不一定呈酸性;③溶液中存在电荷守恒:c(Na+)+c(H+)=c(OH-)+c(HA-)+2c(A2-),现c(Na+)=c(A2-),故c(H+)=c
本题难度:一般
3、选择题 常温下,用 0.1000 mol・L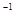 NaOH溶液滴定 20.00mL0.1000 mol・L
NaOH溶液滴定 20.00mL0.1000 mol・L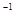 CH3COOH溶液所得滴定曲线如右图。下列说法正确的是
CH3COOH溶液所得滴定曲线如右图。下列说法正确的是
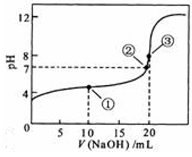
A.点①所示溶液中: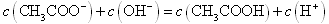
B.点②所示溶液中: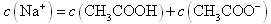
C.点③所示溶液中:
D.滴定过程中可能出现:
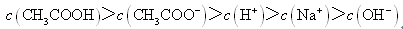
参考答案:D
本题解析:点①所示溶液中的溶质为0.001mol的CH3COOH和0.001mol的CH3COONa;根据电荷守恒得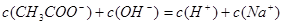 ,而溶液中
,而溶液中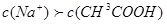
本题难度:简单
4、选择题 把0.2 mol・L-1NH4Cl溶液与0.1 mol・L-1NaOH溶液等体积混合后溶液中下列微粒的物质的量浓度的关系正确的是(???)
A.c( )=c(Na+)=c(OH-)>c(NH3・H2O)
)=c(Na+)=c(OH-)>c(NH3・H2O)
B.c( )=c(Na+)>c(NH3・H2O)>c(OH-)
)=c(Na+)>c(NH3・H2O)>c(OH-)
C.c( )>c(Na+)>c(OH-)>c(NH3・H2O)
)>c(Na+)>c(OH-)>c(NH3・H2O)
D.c( )>c(Na+)>c(NH3・H2O)>c(OH-)
)>c(Na+)>c(NH3・H2O)>c(OH-)
参考答案:D
本题解析:此类型题目,若发生化学反应,优先考虑化学反应,通过化学反应各种离子浓度能比较出来,则不必考虑水解和电离,因为弱电解质电离或盐的水解程度都很小,对离子浓度影响不大,若通过化学反应各种离子浓度大小比较不出来则再考虑水解和弱电解质电离。此题中NH4Cl和NaOH发生反应:NH4Cl+NaOH=NaCl+NH3・H2O生成NH3・H2O,同时 本题难度:简单
本题难度:简单
5、选择题 下列推断合理的是
A.在常温下,Na2SiO3+H2O+CO2 = Na2CO3+H2SiO3↓,说明H2CO3酸性强于H2SiO3;
在高温下,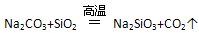 ,说明H2SiO3酸性强于H2CO3
,说明H2SiO3酸性强于H2CO3
B.c(NH4+)相等的(NH4)2SO4、(NH4)2CO3、(NH4)2Fe(SO4)2溶液,则
c[(NH4)2SO4]>c[(NH4)2CO3] >c[(NH4)2Fe(SO4)2]
C.向1L0.3mol/L的NaOH溶液中缓慢通入CO2气体至溶液增重8.8g时,则溶液中
2c(Na+)=3[c(HCO3-)+c(CO32-)+c(H2CO3)]
D.在海带中提取碘的实验中既可以用四氯化碳作萃取剂也可以用酒精作萃取剂
参考答案:C
本题解析:
正确答案:C
A、不正确,强酸制弱酸,是在水溶液中的结论;B、溶液浓度c[(NH4)2CO3] >c[(NH4)2SO4]>c[(NH4)2Fe(SO4)2],(NH4)2CO3中NH4+水解得最多,(NH4)2Fe(SO4)2,Fe2+?水解后呈酸性,抑制NH4+的水解;D、不能用酒精作萃取剂,酒精与水互溶,不分层。
本题难度:简单