微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 将a?g?Na,Na2O,Na2O2的混合物,与足量水完全反应,得到常温常压下的气体bmL;该气体用电火花引燃恰好反应完全,原混合物中Na,Na2O,Na2O2的物质的量比可能是
A.2:1:1
B.0.5a:b:1
C.4:3:2
D.数据不足无法计算
参考答案:AC
本题解析:分析:Na、Na2O、Na2O2?的混合物与足量的水反应得到的气体是氢气和氧气的混合物,将该混合气体通过放电,恰好完全反应,说明氢气和氧气反应的物质的量之比恰好等于它们反应的计量数之比,氢气来源于钠和水的反应,氧气来源于过氧化钠与水的反应,通过钠与水、过氧化钠与水、氢气和氧气反应的方程式,找出钠与过氧化钠的物质的量之比,据此判断,
解答:钠与水、过氧化钠与水、氢气与氧气的反应方程式如下:
2Na+2H2O=2NaOH+H2↑???? 钠与氢气的关系式为2Na~H2
2Na2O2+2H2O=4NaOH+O2↑? 过氧化钠与氧气的关系式为?2Na2O2~O2???
2H2+O2 2H2O????????氢气和氧气的关系式为2H2~O2
2H2O????????氢气和氧气的关系式为2H2~O2
将该混合气体通过放电,恰好完全反应,说明氢气和氧气反应的物质的量之比恰好等于它们反应的计量数之比,即氢气和氧气的物质的量之比为2:1,
通过钠与氢气、过氧化钠与氧气、氢气与氧气的关系式可得钠与过氧化钠的关系式为:4Na~2H2~O2~2Na2O2
所以钠与过氧化钠的物质的量之比为4:2=2:1,而氧化钠的物质的量不确定,
显然A、C中符合钠与过氧化钠的物质的量之比为2:1,
故选AC.
点评:本题考查无数据计算,如果采用常规做法,计算量较大,应用公式次数较多,较容易出错,采用关系式进行分析化繁为简,效果较好,难度中等,关键在于氢气与氧气恰好完全反应.
本题难度:简单
2、选择题 向某NaOH溶液中通人CO2气体后得溶液M,因CO2通入量的不同,溶液M的组成也不同.若向M中逐滴加人盐酸,产生的气体体积V(CO2)与加入盐酸的体积V(HCl)的关系有下列图示四种情况,且(2)中有OA<AB,(3)中有OA=AB,(4)中有OA>AB,则下列分析与判断不正确的是(不计CO2的溶解)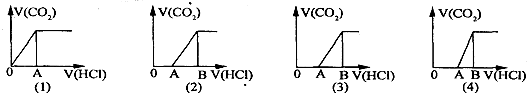
A.图(1)显示M中一定有:c(Na+)>c(HCO3-)>c(OH-)>c(H2CO3)>c(CO32-)
B.图(2)显示M中一定有:c(NaHCO3)>c(Na2CO3)
C.图(3)显示M中一定有:c(Na+)=c(HCO3-)+2c(CO32-)+c(OH-)-c(H+)
D.图(4)显示M中的溶质是:NaOH和Na2CO3
参考答案:B
本题解析:分析:CO2与NaOH反应为①CO2+NaOH=NaHCO3,②CO2+2NaOH=Na2CO3+H20,
当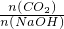 ≥1,反应按①进行,等于1时,CO2、NaOH恰好反应生成NaHCO3;大于1时,生成生成NaHCO3,CO2有剩余;
≥1,反应按①进行,等于1时,CO2、NaOH恰好反应生成NaHCO3;大于1时,生成生成NaHCO3,CO2有剩余;
当 <
<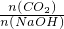 <1,反应按①②进行,CO2、NaOH反应,无剩余,生成物为NaHCO3、Na2CO3;
<1,反应按①②进行,CO2、NaOH反应,无剩余,生成物为NaHCO3、Na2CO3;
当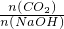 ≤
≤ ,反应按②进行,等于
,反应按②进行,等于 时,CO2、NaOH恰好反应生成Na2CO3;小于
时,CO2、NaOH恰好反应生成Na2CO3;小于 时,生成Na2CO3,NaOH有剩余;
时,生成Na2CO3,NaOH有剩余;
向M中逐滴加入盐酸,根据溶液M中溶质不同,通过反应过程判断;
解答:由分析可知向NaOH溶液中通入CO2气体后得溶液M中溶质情况有:
(1)当含有两种溶质时,
①若溶质为Na2CO3、NaOH时,不能立即产生气体,滴加盐酸先中和氢氧化钠,然后与碳酸钠反应生成碳酸氢钠,碳酸氢钠再与盐酸发生反应生成二氧化碳,且与碳酸钠反应生成碳酸氢钠消耗盐酸体积同碳酸氢钠与盐酸反应生成二氧化碳所消耗的盐酸体积相等,产生的气体体积V(CO2)与加入盐酸的体积V(HCl)的关系为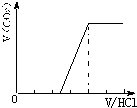 ;
;
②若为NaHCO3、Na2CO3,不能立即产生气体,滴加盐酸先与碳酸钠反应生成碳酸氢钠,碳酸氢钠再与盐酸发生反应生成二氧化碳,且与碳酸钠反应生成碳酸氢钠消耗盐酸体积小于与碳酸氢钠反应生成二氧化碳所消耗的盐酸体积,产生的气体体积V(CO2)与加入盐酸的体积V(HCl)的关系为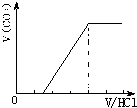 ;
;
(2)若只有一种溶质时,
①当溶质为Na2CO3时,不能立即产生气体,滴加盐酸先与碳酸钠反应生成碳酸氢钠,碳酸氢钠再与盐酸发生反应生成二氧化碳,且与碳酸钠反应生成碳酸氢钠消耗盐酸体积等于与碳酸氢钠反应生成二氧化碳所消耗的盐酸体积,产生的气体体积V(CO2)与加入盐酸的体积V(HCl)的关系为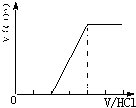 ;
;
②当溶质为NaHCO3时,滴加盐酸与碳酸氢钠反应生成二氧化碳,立即产生气体,产生的气体体积V(CO2)与加入盐酸的体积V(HCl)的关系为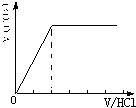 .
.
A、由上述分析可知,图(1)显示M中只有NaHCO3,碳酸氢根离子的水解大于电离,故c(Na+)>c(HCO3-)>c(OH-)>c(H2CO3)>c(CO32-),故A正确;
B、由上述分析可知,图(1)显示M中NaHCO3、Na2CO3,且NaHCO3的物质的量大于Na2CO3,则c(NaHCO3)<c(Na2CO3),故B错误;
C、由上述分析可知,图(1)显示M中只有Na2CO3,根据质子守恒可知:c(Na+)=c(HCO3-)+2c(CO32-)+c(OH-)-c(H+),故C正确;
D、由上述分析可知,图(1)显示M中有Na2CO3、NaOH,故D正确.
故选:B;
点评:本题考查学生金属钠的化合物的性质,可根据碳酸钠、碳酸氢钠、氢氧化钠分别与盐酸反应的化学方程式来计算,注意量的关系.
本题难度:简单
3、选择题 下列化合物不能由两种单质直接化合生成的是
A.CuS
B.Na2O2
C.FeCl2
D.NO
参考答案:AC
本题解析:分析:氯气有强氧化性,和变价金属反应生成最高价态化合物,硫的氧化性较弱,和变价金属反应生成低价态化合物,钠在空气中燃烧生成过氧化钠,据此分析解答.
解答:A.硫的氧化性较弱,和铜反应生成Cu2S,故A选;
B.钠在氧化中燃烧生成过氧化钠,钠和氧气在没有条件的条件下反应生成氧化钠,故B不选;
C.铁在氯气中燃烧生成氯化铁,故C选;
D.氮气和氧气在放电条件下反应生成一氧化氮,故D不选;
故选AC.
点评:本题考查了金属和非金属的性质,注意:无论铁是否过量,铁在氯气中燃烧都生成氯化铁不是氯化亚铁,为易错点.
本题难度:简单
4、选择题 下列物质必须隔绝空气和水蒸气保存的是
①Na? ②NaOH? ③Na2O? ④Na2O2? ⑤Na2CO3? ⑥NaClO
A.①④
B.②③④⑤
C.①②③④
D.①②③④⑥
参考答案:D
本题解析:Na与空气中的H2O和O2反应;
NaOH吸收空气中的CO2而变质;
Na2O与空气中的O2发生反应;
Na2O2与空气中的CO2和H2O反应;
NaClO与空气中的CO2反应.
本题难度:一般
5、选择题 下列几种物质露置于空气中都会变质,其中一种物质不同于另外三种物质的是
A.钠
B.漂白粉
C.氧化钠
D.过氧化钠
参考答案:C
本题解析:钠、漂白粉、过氧化钠露置于空气中分别发生下列反应:4Na+O2====2Na2O,Ca(ClO)2+CO2+H2O====CaCO3↓+2HClO,2HClO====2HCl+O2↑,2Na2O2+2H2O="===4NaOH" +O2↑,2Na2O2+2CO2====2Na2CO3+O2,均为氧化还原反应,而氧化钠露置于空气中,发生的反应为Na2O+CO2====Na2CO3,是非氧化还原反应。
本题难度:一般