��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� �������ʲ����ϼȿ���ͨ�����ʻ����ֿ���ͨ����Һ�临�ֽⷴӦ���ַ����õ�����
A.FeCl2
B.NaCl
C.CuCl2
D.FeCl3
�ο��𰸣�A
�����������������������ǿ�����ԣ�������Ӧʱ������FeCl3������ͨ�����Ϸ�Ӧ��ȡ�����������ڱ�۵Ľ�����������ֱ�ӻ������ɣ�
���A����������ǿ�����ԣ�������Ӧʱ������FeCl3������ͨ�����Ϸ�Ӧ��ȡ����Aѡ��
B��NaCl���ɷ�Ӧ��2Na+Cl2=2NaCl��NaOH+HCl=NaCl+H2O���ɣ���B��ѡ��
C��CuCl2���ɷ�Ӧ��Cu+Cl2=CuCl2��Cu��OH��2+2HCl=CuCl2+2H2O���ɣ���C��ѡ��
D��FeCl3���ɷ�Ӧ��2Fe+3Cl2=FeCl3��Fe��OH��3+3HCl=FeCl3+3H2O���ɣ���D��ѡ��
��ѡA��
���������⿼������������ķ�Ӧ����Ŀ�ѶȲ���ע����������ǿ�����ԣ�����б�۵Ľ�����Ӧʱֻ�������̬�Ļ����
�����Ѷȣ���
2��ѡ���� ���й���Na2CO3��NaHCO3�����ʵıȽ��У�����ȷ����
A.���ȶ��ԣ�Na2CO3��NaHCO3
B.�����µ��ܽ��ԣ�NaHCO3��Na2CO3
C.��ϡ���ᷴӦ�ľ��ҳ̶ȣ�Na2CO3��NaHCO3
D.�������Ĺ��������������ᷴӦCO2�ų���������Na2CO3��NaHCO3
�ο��𰸣�C
���������������A������2NaHCO3 Na2CO3+CO2��+H2O��������
Na2CO3+CO2��+H2O��������
B��Na2CO3��NaHCO3���ܣ�
C����ͬ������NaHCO3��Na2CO3��Ӧ�ų�������ң�
D������n=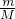 ���ɼ������ʵ�������������������Na2CO3��CO2��NaHCO3��CO2��������
���ɼ������ʵ�������������������Na2CO3��CO2��NaHCO3��CO2��������
���A����2NaHCO3 Na2CO3+CO2��+H2O����̼���Ƽ��Ȳ��ֽ⣬��A��ȷ��
Na2CO3+CO2��+H2O����̼���Ƽ��Ȳ��ֽ⣬��A��ȷ��
B����������ͬ���ܼ�ʱ��Na2CO3��NaHCO3���ܣ���B��ȷ��
C���ֱ�μ�HCl��Һ����Ӧ���ӷ���ʽΪCO32-+2H+�TCO2��+H2O��HCO3-+H+�TH2O+CO2������ͬ������NaHCO3��Na2CO3��Ӧ�ų�������ң���C����
D������������106g����Na2CO3��NaHCO3�����ʵ����ֱ�Ϊ1mol��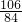 mol������Na2CO3��CO2��NaHCO3��CO2��������CO2�����ʵ����ֱ�Ϊ1mol��
mol������Na2CO3��CO2��NaHCO3��CO2��������CO2�����ʵ����ֱ�Ϊ1mol��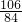 mol����D��ȷ��
mol����D��ȷ��
��ѡ��C��
���������⿼��̼������̼�����Ƶ����ʣ���ȷ�����Ļ�ѧ��Ӧ�ǽ����Ĺؼ�����ע�������ȶ��ԡ�����ķ�Ӧ���ܽ������������
�����Ѷȣ�����
3��ѡ���� ���б仯����Ҫ���뻹ԭ������ʵ�ֵ���
A.S��SO2
B.SO32-��SO2
C.S��H2S
D.S2-��SO42-
�ο��𰸣�C
�����������������Ҫ����ij�ֻ�ԭ������ʵ�֣���ѡ��������Ϊ����������������ijԪ�صĻ��ϼ۽��ͣ��Դ������
���A��S��SO2����Ԫ�ػ��ϼ����ߣ�����Ҫ��������������ʵ�֣��ʴ�A��
B��SO32-��SO2����Ԫ�ء���Ԫ�ػ��ϼ۶����䣬��Ҫ����ǿ�����ʵ�֣���B����
C��S��H2S����Ԫ�صĻ��ϼ۽��ͣ�����Ҫ���뻹ԭ������ʵ�֣���C��ȷ��
D��S2-��SO42-����Ԫ�ػ��ϼ����ߣ�����Ҫ��������������ʵ�֣���D����
��ѡC��
���������⿼��������ԭ��Ӧ����ȷ����������ԭ�������ķ�Ӧ��Ԫ�صĻ��ϼ۱仯�ǽ����Ĺؼ�����Ŀ�ѶȲ���
�����Ѷȣ���
4��ѡ���� Ư���ڿ���������ʧЧ��ԭ����
A.Ca��ClO��2���ȶ����ֽ�
B.CaCl2�׳���
C.Ca��ClO��2��O2��Ӧ
D.Ca��ClO��2�Ϳ����е�CO2��H2O��Ӧ���ɴ����ᣬ������ȶ����ֽ�
�ο��𰸣�D
���������������Ư�۵���Ч�ɷ�ΪCa��ClO��2������HClO�����Ա�̼������Ca��ClO��2��������е�CO2��H2O��Ӧ���ɴ����ᣬ������ȶ����ֽ⣮
���A��Ca��ClO��2�����ȶ������Էֽ⣬��A����
B��Ư���ڿ���������ʧЧ��CaCl2�أ���B����
C��Ca��ClO��2��O2����Ӧ������ʧЧ��ԭ��C����
D��Ư�۵���Ч�ɷ�ΪCa��ClO��2������HClO�����Ա�̼������Ca��ClO��2��������е�CO2��H2O��Ӧ���ɴ����ᣬ������ȶ����ֽ⣬��D��ȷ��
��ѡD��
���������⿼�������Ƶ����ʣ���Ŀ�ѶȲ���ע��HClO�����ԡ����ȶ����Ǿ���Ư��ʧЧ����Ҫԭ��
�����Ѷȣ�����
5��ѡ���� ���з�Ӧ�У�ˮ��Ϊ����������
A.CO+H2O??CO2+H2
B.3NO2+H2O=2HNO3+NO
C.Cl2+H2O=HCl+HClO
D.2F2+2H2O=4HF+O2
�ο��𰸣�A
���������������ˮ��HԪ�ػ��ϼ�Ϊ+1�ۣ�OԪ�ػ��ϼ�Ϊ-2�ۣ���ˮ��Ϊ������ʱ��HԪ�ػ��ϼ۽��ͣ�Ӧ����H2��
���A����Ӧ����H2��HԪ�ػ��ϼ۽��ͣ�ˮΪ����������A��ȷ��
B��H��OԪ�ػ��ϼ�û�з����仯��ˮ�Ȳ���������Ҳ���ǻ�ԭ������B����
C��H��OԪ�ػ��ϼ�û�з����仯��ˮ�Ȳ���������Ҳ���ǻ�ԭ������C����
D��OԪ�ر�������ˮΪ��ԭ������D����
��ѡA��
���������⿼��������ԭ��Ӧ����Ŀ�ѶȲ���ע��Ԫ�ػ��ϼ۵��ж��Լ��ڷ�Ӧ�еı仯����Ԫ�ػ��ϼ۱仯�ĽǶ���ʶ������ԭ��Ӧ��
�����Ѷȣ���