��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� �������ʵ�ˮ��Һ�ܵ��磬�����������ڷǵ���ʵ���
A.HClO
B.Cl2
C.NH3
D.NaHCO3
�ο��𰸣�C
����������������������ָ��ˮ��Һ���ۻ�״̬���ܵ���Ļ�������ǵ������ָ��ˮ��Һ���ۻ�״̬�¶����ܵ���Ļ����
���A��HClO��ˮ���ܵ��룬����ˮ��Һ���磬��HClO���ڵ���ʣ���A����
B����ǵ�����ǻ������Cl2�ǵ��ʣ���Cl2�Ȳ��ǵ����Ҳ���Ƿǵ���ʣ���B����
C��NH3��ˮ��Һ�ܵ��磬����NH3��ˮ��Ӧ����һˮ�ϰ���һˮ�ϰ������������Ӷ����磬���������벻��NH3��������NH3���ڷǵ���ʣ���C��ȷ��
D����NaHCO3��ˮ��Һ���ۻ�״̬�¶��ܵ��磬��NaHCO3���ڵ���ʣ���D����
��ѡC��
���������⿼�����ʺͷǵ���ʣ�ѧ��Ӧ��ȷ����ʺͷǵ���ʶ��ǻ��������ȷ�жϵ����ʱ���������Ϊ�����ﱾ����������ɣ�
�����Ѷȣ�����
2��ѡ���� ij�����ˮ��Һ�����ܺ������������е������֣�K+��NH4+��Cl-��Ca2+��CO32-��SO42-����ÿ��ȡ100mL��Һ�ֱ��������ʵ�飺
A.c��K+����0.2?mol/L
B.һ�������ڵ����ӣ�Ca2+��K+��Cl-
C.c��K+��+c��NH4+��=c��CO32-��+c��SO42-��
D.һ�����ڵ����ӣ�Cl-��NH4+��CO32-��SO42-
�ο��𰸣�A
����������������ټ���AgNO3��Һ���г�������������˵����Һ����Cl-��
�ڼ�������NaOH��Һ��������������ɣ�˵����Һ����NH4+��n��NH4+��=n��NH3��=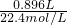 =0.04mol
=0.04mol
�ۼ�������BaCl2 ��Һ���õ�����6.27g����������������ϴ�ӡ������ʣ��2.33g��˵�����ɵij����ܲ����������ᣬ������Һ�к���CO32-��SO42-��������Ca2+��
���AC���ɢڼ�������NaOH��Һ��������������ɣ�˵����Һ����NH4+��n��NH4+��=n��NH3��=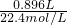 =0.04mol��
=0.04mol��
�ɢۼ���������BaCl2 ��Һ���õ�����6.27g����������������ϴ�ӡ������ʣ��2.33g��˵�����ɵij����ܲ����������ᣬ������Һ�к���CO32-��SO42-�������� Ca2+��ʣ��2.33g��BaSO4��n��SO42- ��=n��BaSO4��=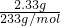 =0.01mol��BaCO3������Ϊm��BaCO3��=6.27g-2.33g=3.94g��n��CO32-��=n��BaCO3��=
=0.01mol��BaCO3������Ϊm��BaCO3��=6.27g-2.33g=3.94g��n��CO32-��=n��BaCO3��=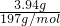 =0.02mol��
=0.02mol��
���ɵ���غ� c��K+��+c��NH4+��=2c��CO32-��+2c��SO42-������֪c��K+��=0.2 mol/L�����Dz���ȷ����û��Cl-������c��K+����0.2 mol/L����A��ȷ��C����
BD���ɢټ���AgNO3��Һ���г�������������˵����Һ����Cl-����ΪCO32-��SO42-��AgNO3��ҺҲ�����ɳ�������B��D����
��ѡA��
���������⿼������Һ�����ӵ��жϣ�����غ�������Ũ������ʱ��Ӧ�ã���д����غ�ʱҪע��������ɵ����ӣ�
�����Ѷȣ�����
3��ѡ���� �������ӷ���ʽ��ȷ����
A.��̼����þ��Һ�м�������Ca��OH��2��Һ��Mg2++2HCO3-+Ca2++2OH-=MgCO3��+CaCO3��+2H2O
B.��0.5molCl2ͨ�뺬2molFeBr2����Һ�У�Cl2+2Fe2+=2Fe3++2Cl-
C.̼�ᱵ����ϡ�����У�BaCO3+2H+=Ba2++CO2��+H2O
D.Fe��OH��3��������Fe��OH��3+3H+=Fe3++3H2O
�ο��𰸣�B
���������������A��̼����þ��Һ�м�������Ca��OH��2��Һ��Ӧ����������þ��������������þ���ܽ�ȸ�С��
B��0.5molCl2��������ʱת��1mol���ӣ���ͨ�뺬2molFeBr2����Һ��ֻ����Fe2+���ӣ�
C��̼�ᱵ����ϡ������Ӧ�������ᱵ������
D��Fe��OH��3�����������Ӧ����������ԭ��Ӧ��
���A��������þ���ܽ�ȸ�С������ȷ�����ӷ�ӦΪMg2++2HCO3-+Ca2++4OH-=Mg��OH��2��+CaCO3��+CO32-+2H2O����A����
B����ԭ��Fe2+��Br-��0.5molCl2��������ʱת��1mol���ӣ���ͨ�뺬2molFeBr2����Һ��ֻ����Fe2+���ӣ����ӷ�ӦΪCl2+2Fe2+=2Fe3++2Cl-����B��ȷ��
C��̼�ᱵ����ϡ������Ӧ�������ᱵ��������ȷ�����ӷ�ӦΪBaCO3+2H++SO42-=BaSO4��+CO2��+H2O����C����
D���������Ӿ��������ԣ��������л�ԭ�ԣ�����ȷ�����ӷ�ӦΪ2Fe��OH��3+6H++2I-=2Fe2++I2+6H2O����D����
��ѡB��
���������⿼�����ӷ�Ӧ����ʽ����д�������жϣ���ȷ�������ӵķ�Ӧ��������ԭ��Ӧ�ǽ����Ĺؼ�����ע�����ʵ��ܽ���������⣮
�����Ѷȣ�һ��
4��ѡ���� �������ӷ���ʽ����д�У���ȷ����
A.Ũ�ռ���Һ�м���������Al+2OH-�TAlO2-+H2��
B.�Ȼ�����Һ�м������ۣ�Fe+Fe3+�T2Fe2+
C.������ͭ�м���������Һ��Cu2++S2-�TCuS��
D.̼����þ��Һ�м��������ռ���Һ��Mg2++2HCO3-+4OH-�TMg��OH��2��+2CO32-+2H2O
�ο��𰸣�D
���������������A��ˮ�μӷ�Ӧ��
B�����ӡ���ɲ��غ㣻
C������������ת����
D����Ӧ����������þ��̼���ơ�ˮ��
���A��Ũ�ռ���Һ�м������������ӷ�ӦΪ2H2O+2Al+2OH-�T2AlO2-+3H2������A����
B���Ȼ�����Һ�м������۵����ӷ�ӦΪFe+2Fe3+�T3Fe2+����B����
C��������ͭ�м���������Һ�����ӷ�ӦΪCu��OH��2+S2-?CuS+2OH-����C����
D��̼����þ��Һ�м��������ռ���Һ�����ӷ�ӦΪMg2++2HCO3-+4OH-�TMg��OH��2��+2CO32-+2H2O����D��ȷ��
��ѡD��
���������⿼�����ӷ�Ӧ����ʽ����д����ȷ���ӷ�Ӧ��ʵ�ʡ����ӷ�Ӧ�б�����ѧʽ�������ǽ����Ĺؼ���ע��������þ�����ܣ���Ŀ�ѶȲ���
�����Ѷȣ���
5��ѡ���� ���г��õĸ�����У����ܸ�����������
A.ŨH2SO4
B.��ʯ��
C.��ʯ��
D.��ˮ�Ȼ���
�ο��𰸣�BC
�������������������ѡ�ø��������ˮ�ұ�������������������Ӧ�����
���A��ŨH2SO4����ˮ������������Ӧ����A��ȷ��
B����ʯ������ˮ�������������������ƺ��������Ʒ�Ӧ����B����
C����ʯ������ˮ�����������ƣ����������������Ʒ�Ӧ����C����
D����ˮ�Ȼ�������ˮ������������Ӧ����D��ȷ��
��ѡBC��
���������⿼���˸������Ҫ����ɴ��⣬�����������������ʽ��У�
�����Ѷȣ���