微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 常温下,取0.1 mol/L HA溶液与0.1 mol/L NaOH溶液等体积混合(混合后溶液体积的变化不计),测得混合溶液的pH=8。试回答以下问题:
(1)混合后溶液的pH=8的原因是________________(用离子方程式表示)。
(2)混合后的溶液中由水电离出的c(OH-)____0.1 mol/L NaOH溶液中由水电离出的c(OH-) (填“>”、“<”或“=”)。
(3)已知NH4A溶液为中性,又知将HA溶液加到NaHCO3溶液中有气体放出,试推断NH4HCO3溶液的pH________7(填“>”、“<”或“=”)。
(4)有相同温度下相同浓度的四种盐溶液:A.NH4HCO3;B.NH4A;C.(NH4)2SO4;D.NH4Cl,按pH由大到小的顺序排列________(填序号)。
参考答案:(1)A-+H2O![]() 本题解析:
本题解析:
本题难度:一般
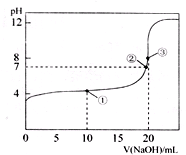
2、选择题 已知某温度时CH3COOH的电离平衡常数为K.该温度下,用0.1000mol?L-1NaOH溶液滴定20.00mL?0.1000mol?L-1CH3COOH溶液所得滴定曲线如图(忽略温度变化).下列说法中不正确的是( )
A.点①所示溶液中:c(CH3COO-)+2c(OH-)=c(CH3COOH)+2c(H+)
B.点②所示溶液中:c(Na+)<c(CH3COO-)+c(CH3COOH)
C.点③所示溶液中:c(Na+)>c(OH-)>c(CH3COO-)>c(H+)
D.①、③点表示的溶液中
c(CH3COO-)?c(H+)
c(CH3COOH)
均等于K
参考答案:A、点①反应后溶液是CH3COONa与CH3COOH物质的量
本题解析:
本题难度:一般
3、选择题 下列物质中属于电解质的是( )
A.CO2
B.BaSO4
C.Zn
D.食盐水
参考答案:A.二氧化碳和水反应生成碳酸,碳酸能电离出自由移动的阴阳离子
本题解析:
本题难度:简单
4、选择题 如表为有关化合物的pKsp,pKsp=-lgKsp。某同学设计实验如下:①向AgNO3溶液中加入适量NaX溶液,得到沉淀AgX;②向①中加NaY,则沉淀转化为AgY;③向②中加入NaZ,沉淀又转化为AgZ。则表中a、b、c的大小关系为
A.a>b>c
B.aC.cD.a+b=c
参考答案:B
本题解析:试题分析:①向AgNO3溶液中加入适量NaX溶液,得到沉淀AgX;②向①中加NaY,则沉淀转化为AgY,这说明AgY的溶度积常数小于AgX的溶度积常数;③向②中加入NaZ,沉淀又转化为AgZ,说明AgZ的溶度积常数小于AgY的溶度积常数。根据pKsp=-lgKsp可知,溶度积常数越小,pKsp越大,所以表中a、b、c的大小关系为a<b<c,答案选B。
考点:考查溶度积常数的计算和溶解平衡的应用
点评:该题设计新颖,针对性强,有利于培养学生的学习兴趣,有助于激发学生的学习积极性。明确沉淀转化的原理和溶度积常数与pKsp的关系是答题的关键,有利于培养学生的逻辑推理能力和知识的迁移能力。
本题难度:一般
5、填空题 (16分)某同学拟用粗氧化铜(含少量FeO及不溶于酸的杂质)制取无水氯化铜,流程如图:
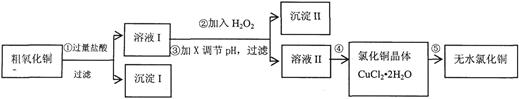
(1)步骤①中氧化铜与盐酸反应的离子万程式:___________________。
(2)步骤②中加入H2O2的目的____________________________________,
沉淀II的化学式为_______________________。
(3)已知:
?
| 氢氧化物开始沉淀时的pH
| 氢氧化物沉淀完全时的pH
| ?Fe3+
| 1.9
| 3.2
| ?Cu2+
| 4.7
| 6.7
| ?Fe2+
| 7
| 9
步骤③中调节pH的最佳范围为____,调节溶液pH的试剂X可以是______________:
a.NaOH???????????? b.CuO?????????? c.Cu(OH)2???????? d.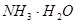
(4)步骤④的操作是___________,过滤、洗涤、干燥。
为得到无水CuCl2,步骤⑤需在干燥的HCl气流中加热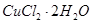 ,原因是__________________________________________________________。 ,原因是__________________________________________________________。
参考答案:(1)CuO+2H+=Cu2++H2O(2分);
(2
本题解析:(1)氧化铜是碱性氧化物,和盐酸反应的离子方程式为CuO+2H+=Cu2++H2O。
(2)由于溶液中含有亚铁离子,而亚铁离子的沉淀pH大于铜离子的,所以应该把亚铁离子转化为铁离子而产生氢氧化铁沉淀,从而除去杂质。
(3)要沉淀铁离子而保留铜离子,则根据pH可知,应该是3.2至4.7之间。由于调节pH是不能引入杂质的,所以答案选bc。
(4)要得到氯化铜晶体,则应该是蒸发浓缩,冷却结晶,然后过滤、洗涤干燥即可。氯化铜是强酸弱碱盐,水解生成氢氧化铜和氯化氢。所以在加热过程中,应该在氯化物的
本题难度:一般
|
|