微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 对于可逆反应:2SO2 + O2 ?2SO3(g)?△H<0,升高温度产生的影响为()
?2SO3(g)?△H<0,升高温度产生的影响为()
A.v正增大, v逆减小
B.v正减小, v逆增大
C.v正和v逆不同程度的增大
D.v正和v逆同等程度的增大
参考答案:C
本题解析:
试题分析:升高温度,同时加快正、逆反应速率,又因升高温度会造成化学平衡的移动,故正、逆反应速率的增大的程度不同。故选C。
点评:温度在加快反应速率中起到很重要的作用,另外化学反应都伴随着能量的变化,故改变温度必然会造成化学平衡的移动。
本题难度:一般
2、选择题 下列反应中生成H2的速率最快的是[???? ]
金属??
酸溶液
温度
A.
Mg
0.5mol/L H2SO4
20℃
B.
Fe
1 mol/L HCl
20℃
C.
Mg?
2 mol/L HCl
20℃
D.
Mg
1 mol/L H2SO4
30℃
参考答案:D
本题解析:
本题难度:一般
3、选择题 为减缓足量的镁和一定量盐酸的反应速率,又不影响氢气的总量,可采用的措施是( )
A.加固体NaOH
B.加固体硝酸钠
C.加固体醋酸钾
D.加硫酸
参考答案:C
本题解析:
试题分析:加NaOH固体,会消耗盐酸,使生成氢气的总量减小,A错误;加固体硝酸钠,溶液中有H+、NO3-相当于硝酸,与镁反应生成NO,不再生成氢气,B错误; 加CH3COOK固体,会得到CH3COOH,溶液中C(H+)减小,反应速率减慢,氢气的总量不变,C正确;加硫酸,会使生成的氢气增多,D错误。
考点:考查化学反应速率的影响因素。
本题难度:一般
4、选择题 有X、Y、Z三种物质.常温下分别用Y或Z与X混合时,反应速率几乎相同的是( )
| 选项 | X | Y | Z
①
2mL?5%H2O2?溶液
1mL?1mol?L-1CuSO4溶液
1mL?1mol?L-1FeCl3溶液
②
1mL?1mol?L-1?NaHCO3溶液
1mL?1mol?L-1?HCl溶液
1mL?0.5mol?L-1?H2SO4溶液
③
钠块
10mL?乙醇
10mL?水
④
经过酸洗除锈的铁钉
5mL?海水
5mL?蒸馏水
A.①
B.②
C.③
D.④
参考答案:①硫酸铜和氯化铁都可以作双氧水分解的催化剂,但催化剂不同,导
本题解析:
本题难度:一般
5、选择题 一氧化碳与氢气在催化剂作用下合成甲醇的反应为:CO(g)+2H2(g) CH3OH(g)。在容积均为1L的a、b、c、d、e5个密闭容器中分别充入1mol CO和2mol H2等量混合气体,控温。实验测得相关数据如图,温度分别为300℃、500℃的密闭容器中,甲醇的物质的量与时间的关系;温度分别为T1~T5的密闭容器中,反应均进行到5min时甲醇的体积分数.下列有关说法正确的是 CH3OH(g)。在容积均为1L的a、b、c、d、e5个密闭容器中分别充入1mol CO和2mol H2等量混合气体,控温。实验测得相关数据如图,温度分别为300℃、500℃的密闭容器中,甲醇的物质的量与时间的关系;温度分别为T1~T5的密闭容器中,反应均进行到5min时甲醇的体积分数.下列有关说法正确的是
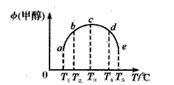 
A.K1 < K2
B.该反应的正反应是气体体积减小的吸热反应
C.将容器c中的平衡态转变到容器d中的平衡态,可采取的措施有升温或减压
D.反应到5min时,a、b两容器中平衡正向移动,d、e两容器中平衡逆向移动
参考答案:C
本题解析:
试题分析:A、图1中,温度升高,甲醇的含量减少,可以判读反应为放热反应,不选A;B、由于反应是放热反应,不选B;C、将容器c中的平衡状态转变到容器d的平衡态,需要降低甲醇的含量,平衡逆向移动,可采取升温或减压,选C;D、反应进行到5分钟,T3达到平衡,a、b没有达到平衡,平衡正向移动,d、e达到了平衡,不选D。
考点:化学平衡图像分析。
本题难度:困难
|