微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 入大量SO3? D.降低体系温度
参考答案:AC
本题解析:根据外界条件对化学反应速率的影响分析,能改变反应速率的措施有温度、压强、浓度、催化剂等.A通入大量氧气,增大反应物的浓度,能增大正反应速率,故A正确.
B、增大容器容积,减小了体系的压强,压强减小,正反应速率减小,故B错误.
C、通入三氧化硫,反应物的浓度不变,生成物的浓度增大,化学平衡向逆反应方向移动,所以正反应速率逐渐增大,故C正确.
D、降低体系的温度,正逆反应速率都减小,故D错误.
本题难度:简单
2、选择题 反应C(s)+H2O(g) CO(g)+H2(g)在一可变容积的密闭容器中进行,下列条件的改变对其反应速率几乎无影响的是
CO(g)+H2(g)在一可变容积的密闭容器中进行,下列条件的改变对其反应速率几乎无影响的是
A.增加水蒸汽的量
B.将容器的体积缩小一半
C.保持体积不变,充入N2使体系压强增大
D.保持压强不变,充入N2使容器容积变大
参考答案:C
本题解析:
试题分析:A改变反应物的浓度,反应速率增大;B体积变小,压强增大,反应速率增大;C体积不变,有效气体的分压强不变,故反应速率不变,选C;D体积变大,有效气体的分压强变小,反应速率变小。
点评:化学平衡与化学速率是历年高考必考知识点,考生在备考过程中要注意分别两者的影响因素。
本题难度:简单
3、填空题 影响化学反应速率的因素很多。在下列事实中,影响反应速率的外界条件分别为:
(1)夏天的食品易霉变,冬天不易发生该现象 ;
(2)在5
参考答案:
本题解析:
本题难度:一般
4、填空题 (5分)(1)某学生欲用铁片与2mol・L-1盐酸反应来制取少量氢气,现欲提高化学反应速率,实验中可采用①???????????????????????;②????????????????????;③_________等方法;(2)碳酸钠溶液与盐酸的反应若欲降低化学反应速率可采取的方法有①?????????????;②________________________。
参考答案:(1)使用铁粉、使用较浓盐酸溶液,加入少量硫酸铜溶液(或铜单
本题解析:考查外界条件对反应速率对影响。在其它条件不变时,增大反应物浓度,或升高温度,或增大反应物的接触面积,或通过原电池反应,或使用催化剂等均可以增大反应速率。
本题难度:一般
5、选择题 在密闭容器中充入一定量的NO2,发生反应2NO2(g) N2O4(g)?△H=-57kJ/mol,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化的曲线如下图所示。下列说法正确的是
N2O4(g)?△H=-57kJ/mol,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化的曲线如下图所示。下列说法正确的是
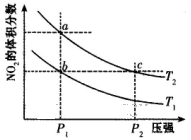
A.a、c两点的反应速率:a>c
B.a、b两点的转化率:a<b
C.a、c两点气体的颜色:a深,c浅
D.由a点到b点,可以用加热的方法
参考答案:B
本题解析:
试题分析:A、a、c两点所在的温度相同,但c点的压强高于a点的压强。压强高,反应速率快,因此反应速率为a<c,A不正确;B、a点NO2的体积分数大于b点NO2的体积分数,这说明a、b两点的转化率是a<b,B正确;C、c点的压强高于a点的压强,压强高,容器的容积小,N2O4的浓度大,所以颜色深浅是a浅,c深,C不正确;D、正方应是放热反应,由a点到b点,NO2的体积分数减小,说明平衡向正反应方向移动,因此不能用加热的方法,应该是降低温度,D不正确,答案选B。
本题难度:一般