微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、简答题 【物质结构与性质】
芦笋中的天冬酰胺(结构如图)和微量元素硒、铬、锰等,具有提高身体免疫力的功效。
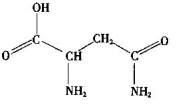
(1)天冬酰胺所含元素中_______(填元素名称)元素基态原子核外未成对电子数最多。
(2)天冬酰胺中碳原子的杂化轨道类型有_______种。
(3)H2S和H2Se的参数对比见下表。
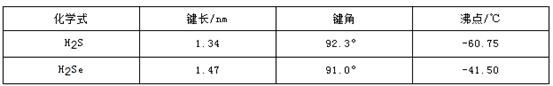
①H2Se的晶体类型为_________,含有的共价键类型为_________。
②H2S的键角大于H2Se的原因可能为____________________。
(4)已知钼(Mo)位于第五周期VIB族,钼、铬、锰的部分电离能如下表所示

A是____________(填元素符号),B的价电子排布式为????????????。
参考答案:(1)氮???
(2)2
(3)①分子晶体,极性
本题解析:
本题难度:一般
2、选择题 a、b、c、d是四种短周期元素。a、b、d同周期,c、d同主族。a的原子结构示意图为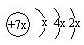 ,b与c形成化合物的电子式
,b与c形成化合物的电子式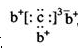 为下列比较中正确的是(???)
为下列比较中正确的是(???)
A.原子半径:a>c>d>b
B.电负性:a>b>d>c
C.最高价含氧酸的酸性:c>d>a
D.第一电离能:d>a>b>c
参考答案:C
本题解析:
本题难度:简单
3、填空题 VA族的氮、磷、砷(As)等元素的化合物在科研和生产中有许多重要用途,请回答下列问题。
(1)砷的基态原子的电子排布式为?????????????。
(2)N、P、As原子的第一电离能由大到小的顺序为?????????????。
(3)NH3的沸点比PH3高,原因是??????;PO43-离子的立体构型为?????。
(4)PH3分子中P原子采用??????杂化。
(5)H3AsO4和H3AsO3是砷的两种含氧酸,请根据结构与性质的关系,解释H3AsO4比H3AsO3酸性强的原因???????????????????????????????。
(6) CuCl2与氨水反应可形成配合物[Cu(NH3)4]Cl2,1mol该配合物中含有σ键的数目为???????????。
参考答案:(1)1s22s22p63s23p63d104s24p3??
本题解析:
本题难度:一般
4、选择题 下列混合物可采用蒸馏法分离的一组是
①乙二醇(沸点:198℃)和乙酸(沸点:117.9℃)
②乙醇中含少量水
③液态N2和O2
④水和盐酸
A.①③④
B.①②③
C.②③④
D.①②③④
参考答案:D
本题解析:剖析:乙二醇和乙酸沸点差异较大,可用蒸馏法将其分离;乙醇和水分离加热蒸馏时应先加入新制的生石灰就可用蒸馏方法将其分离;盐酸沸点较低,也可用蒸馏方法将其与水分离,但得到的是氯化氢气体;N2沸点低于O2,所以先汽化,可分离.
规律总结:蒸馏法通常用于分离两种互溶且熔沸点相差较大的液体混合物,如汽油和苯的分离等.
本题难度:一般
5、选择题 X、Y、Z、M、W为五种原子序数依次增大短周期元素。Y、Z、M是同一周期的元素,且最外层电子数之和为15,Y与M可形成YM 2分子;X与Z形成的气态化合物在标准状况下的密度为0.76 g/L;W的质子数是X、Y、Z、M四种元素质子数之和的1/2。下列说法正确的是
A.原子半径:W>Z>Y>X>M
B.YM2、Y2X2、W2M2均为直线型的共价化合物
C.元素Z和元素M的最高正价的数值之和等于11
D.由X、Y、Z、M四种元素形成的化合物中可能含有离子键
参考答案:D
本题解析:
本题难度:一般