微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、实验题 碱式碳酸铜可表示为:xCuCO3・yCu(OH)2・zH2O,测定碱式碳酸铜组成的方法有多种(Cu
的相对原子质量按63.5计)。
(1)现采用氢气还原法,请回答下列问题:
已知xCuCO3・yCu(OH)2・zH2O与氢气反应的化学方程式为xCuCO3・yCu(OH)2・zH2O+(x+y)H2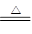 (x+y)Cu+xCO2+(x+2y+z)H2O
(x+y)Cu+xCO2+(x+2y+z)H2O
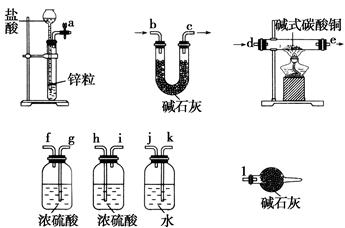
①实验装置用下列所有仪器连接而成,按氢气流方向的连接顺序是(填入仪器接口字母编号):
(a)→( )( )→( )( )→( )( )→( )( )→( )( )→(l);
②称取23.9 g某碱式碳酸铜样品,充分反应后得到12.7 g残留物,生成4.4 g二氧化碳和7.2 g水。该样品的结晶水质量为________g,化学式为________。
(2)某同学以氮气代替氢气,并用上述全部或部分仪器来测定碱式碳酸铜的组成,你认为是否可行?请说明理由_________________________________________________________
参考答案:(1)①k j g(或h) f(或i) d e h(或g)
本题解析:(1)①由实验目的和实验装置知,该实验要测定生成的水、二氧化碳的量,而从a口出来的氢气中含有水蒸气和挥发出来的氯化氢,会对实验有干扰,所以应先用水吸收氯化氢,再用浓硫酸吸收水蒸气,再通入碱式碳酸铜中发生反应,而产生的两种气体应先用浓硫酸吸收水蒸气,再用U形管中的碱石灰吸收二氧化碳,同时要连接上装有碱石灰的球形干燥管,防止空气中的水蒸气和二氧化碳进入U形管而产生误差。②根据所给数据可计算出生成的铜、二氧化碳、水的物质的量分别为0.2 mol、1 mol、0.4 mol,所以可知(x+y)∶x∶(x+2y+z
本题难度:一般
2、选择题 用铜锌合金制成假元宝欺骗行人事件屡有发生。下列不易区别其真伪的方法是
A.测定密度
B.放入硝酸中
C.放入盐酸中
D.观察外观
参考答案:D
本题解析:不同的物质具有不同的密度所以可以根据密度来区分铜锌合金和假元宝,A可以鉴别;铜锌合金中的铜和锌都可以与硝酸反应,产生气泡,若果是金元宝则不能反应,没有气泡产生,B可以鉴别;铜锌合金中的锌可以与盐酸反应产生气泡,C可以鉴别,铜锌合金是黄色的,金也是黄色,所以通过观察外观是不能鉴别的,答案选D。
本题难度:一般
3、填空题 聚合硫酸铁(PFS)是一种新型高效的无机高分子絮凝剂,广泛用于水的处理.用铁的氧化物为原料来制取聚合硫酸铁,为控制水解时Fe3+的浓度,防止生成氢氧化铁沉淀,原料中的Fe3+必须先还原为Fe2+.实验步骤如下:
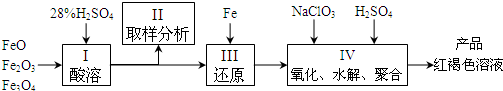
(1)用98%的硫酸配制28%的硫酸,所需的玻璃仪器除量筒外,还有______.
(a)玻璃棒 (b)烧杯?? (c)烧瓶
(2)步骤II取样分析溶液中Fe2+、Fe3+的含量,目的是______和确定氧化Fe2+所需NaClO3的量:
(a)?控制溶液中Fe2+与Fe3+含量比 (b)?确保铁的氧化物酸溶完全??? (c)?确定下一步还原所需铁的量
(3)完成步骤IV中的氧化还原反应:补充产物并配平:
______?Fe2++______ClO3-+______H+=______Fe3++Cl-+______
(4)聚合硫酸铁溶液中SO42?与Fe3+物质的量之比不是3:2.根据下列提供选择的试剂和基本操作,测定聚合硫酸铁产品溶液中SO42?与Fe3+物质的量之比.测定时所需的试剂______.
(a)?NaOH (b)?FeSO4 (c)?BaCl2 (d)?NaClO3
需要测定Fe2O3和______的质量(填写化合物的化学式).
参考答案:(1)配制一定量分数硫酸溶液需要的仪器有:胶头滴管、量筒、玻
本题解析:
本题难度:简单
4、推断题 甲、乙、丙三种物质之间有如下转化关系
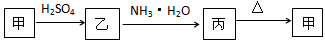
(1)若乙溶液中加入KSCN溶液,有血红色出现,则甲物质是:_____________。写出“甲→乙”转化的离子方程式:________________________。
(2)若甲是不溶于水的白色粉末状物质,既能溶于盐酸又能溶于氢氧化钠溶液,则乙是___________。写出“乙→丙”转化的离子方程式:___________________________。
参考答案:(1)Fe2O3;Fe2O3+6H+==2Fe3++3H2O
本题解析:
本题难度:一般
5、选择题 在pH为4-5的环境中,Cu2+和Fe2+不水解,而Fe3+几乎完全水解。工业上制CuCl2是将浓盐酸用蒸汽加热到80℃左右。在慢慢加入粗氧化铜(含杂质FeO),充分搅拌使之溶解。欲除去所得CuCl2溶液中的杂质离子,下列方法中可行的是
A.加入HNO3将Fe2+氧化成Fe3+,再加水稀释至pH4-5
B.向溶液中通入Cl2,再加入CuO粉末调节至pH4-5
C.向溶液中通入Cl2,在通入NH3调节至pH4-5
D.向溶液中通入H2O2, 再加入CuO粉末调节至pH4-5
参考答案:D
本题解析:在pH为4-5的环境中,Cu2+和Fe2+不水解,而Fe3+几乎完全水解。所以应先把二价铁氧化为三价铁,但氧化的同时又不能引入杂质,故选D
本题难度:困难