微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 已知(l)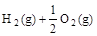 ?=H2O(g)???ΔH1=a kJ・
?=H2O(g)???ΔH1=a kJ・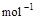
(2)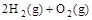 ?=2H2O(g)??ΔH2=b kJ・
?=2H2O(g)??ΔH2=b kJ・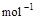
(3)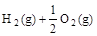 =H2O(l)????ΔH3=c kJ・
=H2O(l)????ΔH3=c kJ・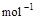
(4)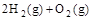 ?=2H2O(l)???ΔH4=d kJ・
?=2H2O(l)???ΔH4=d kJ・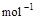
下列关系式中正确的是
A. a<c <0
B.b>d>0
C.2a=b<0
D.2c=d>0
参考答案:C
本题解析:
试题分析:氢气与氧气反应生成水是放热反应,所以ΔH的值是小于0的,故BD错误,H2O(l)变成H2O(g)需要吸收能量,即a大于c,所以A错误,答案为C。
点评:本题考查了反应热的比较,注意要理解ΔH的意义,才能选择出正确的选项。
本题难度:简单
2、选择题 已知298K下反应2Al2O3(s)+3C(s)==4Al(s)+3CO2(g)?? ΔH=+2171kJ・mol-1
△S=+635.5J・mol-1・K-1,则此反应
A.高温下可自发进行
B.任何条件下都可自发进行
C.任何条件下都不可自发进行
D.低温下可自发进行
参考答案:A
本题解析:略
本题难度:简单
3、选择题 能源是当今社会发展的三大支柱之一.有专家指出:如果对燃烧产物如CO2、H2O、N2等能够实现利用太阳能让它们重新组合(如右图),可以节约燃料,缓解能源危机.在此构想的物质循环中太阳能最终转化为( )
A.化学能
B.电能
C.生物质能
D.热能
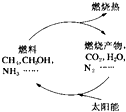
参考答案:由图可知,太阳能首先转化为化学能,其次化学能转化为热能.故选
本题解析:
本题难度:一般
4、选择题 已知碳、一氧化碳、晶体硅的燃烧热分别是△H =-393.5kJ/mol、△H ="-283" kJ/mol和△H ="-989" kJ/mol,则工业冶炼晶体硅反应2C(s)+SiO2(s)=" Si" (s)+2 CO(g) △H =
A.+768 kJ/mol
B.-768 kJ/mol
C.+2342 kJ/mol
D.-2342 kJ/mol
参考答案:A
本题解析:
试题分析:根据碳、一氧化碳、晶体硅的燃烧热分别是△H =-393.5kJ/mol、△H ="-283" kJ/mol和△H ="-989" kJ/mol,可分别得到热化学方程式:①C(s)+O2(g)=CO2(g) △H =-393.5kJ?mol?1, ②CO(g)+1/2O2(g)=CO2(g) △H ="-283" kJ?mol?1,③Si(s)+ +O2(g)=SiO2(g) △H ="-989" kJ/mol,根据盖世定律,反应2C(s)+SiO2(s)=" Si" (s)+2 CO(g
本题难度:一般
5、选择题 已知破坏1 mol H―H键、Cl―Cl键、H―Cl键分别需要吸收436kJ、243kJ、432kJ能量,则由H2与CL2生成1 mol HCL总的过程需要???(???)
A.放热185kJ
B.吸热185kJ
C.放热92.5kJ
D.吸热92.5kJ
参考答案:C
本题解析:略
本题难度:简单