微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 (12分)金属钠在氧气中充分燃烧生成产物是???????色,将所得产物投入水中,产物和水迅速发生反应,写出该反应的化学方程式:??????????????????????????????。向上所得溶液中加入FeSO4溶液,看到的现象:??????????????????????????????????????,此过程中发生的氧化还原反应的化学方程式:??????????????????????????????。
2、实验题 某实验小组欲通过以下实验来探究Na2CO3和NaHCO3两种物质的性质。
(1)称取两种固体各2 g,分别放入两个小烧杯中,再各滴加10 mL 蒸馏水,振荡,测量温度变化;待固体充分溶解,并恢复至室温后,向所得溶液中各滴入2滴酚酞试液。
① 发现Na2CO3固体完全溶解,而NaHCO3固体有剩余,由此得到结论????????????????????????????。
② 同学们在两烧杯中还观察到了其它现象。其中,盛放Na2CO3的烧杯中出现的现象是????(填字母序号)。
A.溶液温度下降? B.溶液温度升高??? C.滴入酚酞后呈浅红色???????D.滴入酚酞后呈红色
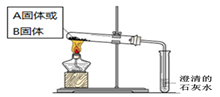
(2)如下面左图所示分别加热A、B固体,发现固体A受热产生的气体能使澄清石灰水变浑浊,但一段时间后浑浊又变澄清。请用化学方程式解释澄清石灰水中发生的现象????????????????????。
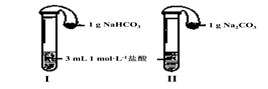
(3)如上图所示,在气密性良好的装置I和II中分别放入试剂,将气球内的固体同时倒入试管中。
两试管中均产生气体,?????????(填“I”或“II”)的反应程度更为剧烈。
② 反应结束后,气球均有膨胀,恢复至室温。下列说法正确的是?????????。
A.装置I的气球体积较大???????????? B.装置II的气球体积较大
C.生成气体的体积根据盐酸计算?????? D.生成气体的体积根据固体计算
(4)将两种固体分别配制成0.5 mol・L-1的溶液,探究与0.5 mol・L-1CaCl2溶液反应的情况
实验方案
| 预测现象
| 预测依据
| 实际结果
|
实验1:向2 mL Na2CO3溶液中滴加1 mL 0.5 mol・L-1CaCl2溶液
| 有白色
沉淀
| Na2CO3溶液中的CO32-浓度较大,能与CaCl2发生反应。
| 有白色沉淀
|
实验2:向2 mL NaHCO3溶液中滴加1 mL 0.5 mol・L-1CaCl2溶液
| 无白色
沉淀
| NaHCO3溶液中的CO32-浓度很小,不能与CaCl2反应。
| 有白色沉淀出现,同时有少量气泡冒出。
?
请写出上述实验过程中发生的反应的离子方程式:
实验1:???????????????????????????????????;实验2:??????????????????????????????????。
3、选择题 将金属元素钠在空气中燃烧,生成Na2O与Na2O2的混合物。取该燃烧产物7.48g溶于水制成1000mL溶液,取出10mL用0.1mol/L的盐酸中和,用去盐酸20mL,由此可知该产物中Na2O的质量分数约为 [ ]
A.16.6%
B.20%
C.80%
D.78.4%
4、选择题 将一小块金属钠投入盛少量 饱和澄清石灰水的试管里,不可能观察到的现象是 饱和澄清石灰水的试管里,不可能观察到的现象是
A.钠熔成小球并在液面上游动
B.有气体生成
C.溶液底部有银白色物质生成
D.溶液变浑浊
5、填空题 (12分)(1)过氧化钠可用作于制氧剂,写出过氧化钠与二氧化碳反应的化学方程式?????????????????????????????????????????
(2)工业上制取漂白粉的化学方程式为______________?????????______。漂白粉露置于空气中失效的原因是(用化学方程式表示):
①________??????????????????????????????????????????????????_,
②___________??????????????????????????????????????________。
|