��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ���и��������У����÷�Һ©�����з������
A������CCl4
B�����CCl4
C���ƾ���ˮ
D�����ͺ�ˮ
2������� ��ʯ���顢ʯ�ҵ�(CaCN2)��������(��H2S)��Ӧ�����ܾ���β�������ܻ��Ӧ�ù㷺��CS(NH2)2(����)���䲿�ֹ����������£�
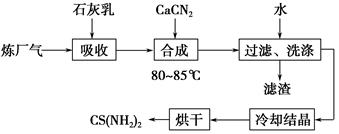
(1)�����£�H2S�������з�Ӧ��2H2S(g)??2H2(g)��S2(g)����ƽ�ⳣ������ʽΪK��________________��
(2)��ʯ��������H2S��ȡCa(HS)2��Ҫ�ڵ����½��У���ԭ����_____________________________________________________��
���˵õ��������������ã���������Ҫ�ɷ���________(�ѧʽ)��
(3)�ϳ������賤ʱ����裬���ڽϸ��¶�(80��85 ��)�½��У���Ŀ����_______________________________________��
Ca(HS)2��CaCN2��ˮ��Һ�кϳ�����Ļ�ѧ����ʽΪ________________________________��
(4)������X�����廥Ϊͬ���칹�壬X����FeCl3��Һ�У���Һ�Ժ�ɫ��X�Ļ�ѧʽΪ________________��
3������� �ȣ�Sr��Ϊ�������ڢ�A��Ԫ�أ��仯������ˮ�Ȼ��ȣ�SrCl2��6H2O����ʵ������Ҫ�ķ����Լ�����ҵ�ϳ�������ʯ����Ҫ�ɷ�ΪSrSO4��Ϊԭ���Ʊ��������������£�
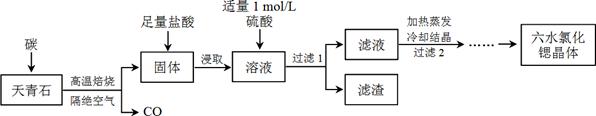
��֪���� �������ȡ����Һ�г�����Sr2+��Cl���⣬����������Ba2+���ʣ�
�� SrSO4��BaSO4���ܶȻ������ֱ�Ϊ3.3��10��7��1.1��10��10��
�� SrCl2��6H2O��Ħ������Ϊ��267 g/mol��
��1������ʯ����ǰ����ĥ���飬��Ŀ����_________________________________________��
��2�������������±��գ���0.5 mol SrSO4��ֻ��S����ԭ��ת����4 mol���ӡ�д���÷�Ӧ�Ļ�ѧ����ʽ��_____________________________________________��
��3��Ϊ�˵õ��ϴ�����ˮ�Ȼ��Ⱦ��壬����2������е�����������_______________��
��4�����������Ŀ����______________________��Ϊ�����ԭ�ϵ������ʣ���Һ��Sr2+��Ũ��Ӧ������_________ mol/L��ע����ʱ��Һ��Ba2+Ũ��Ϊ1��10��5 mol/L����
��5����Ʒ���ȼ�⣺��ȡ1.000 g��Ʒ�ܽ�������ˮ�У������м��뺬AgNO3 1.100��10��2 mol��AgNO3��Һ����Һ�г�Cl�D�⣬����������Ag+��Ӧ�����ӣ�����Cl�D��ȫ�������ú�Fe3+����Һ��ָʾ������0.2000 mol/L��NH4SCN����Һ�ζ�ʣ���AgNO3��ʹʣ���Ag+ ��AgSCN��ɫ��������ʽ������
�ٵζ���Ӧ�ﵽ�յ��������_________________________________________��
�����ζ�������ȥ����Ũ�ȵ�NH4SCN��Һ20.00 mL�����Ʒ��SrCl2��6H2O�������ٷֺ���Ϊ______________������4λ��Ч���֣���
4��ѡ���� ���ӱ��ӵ��Ҵ���Һ�л��ձ��ӣ������в�����
������
�ڹ���
�۾��á���Һ
�ܼ�������������
��ͨ�������CO2
����������NaOH��Һ
����������FeCl3��Һ
�����������Ũ����������ȡ�
������ʵ�������[???? ]
A.�ܢݢ�
B.�ޢ٢ݢ�
C.���
D.��ڢݢ�
5��ʵ���� ��8�֣����ʵ����������л������뿪��
��1�������Թ�����ˮ�Ļ�����CaCO3��ˮ������_______ ��������
��2�����ֻ����ܽ�е����ϴ��Һ�壬�籽�����Ȼ�̼�Ļ�������_______ ��������
��3�������Թ�����ˮ�Ļ�����ʳ�κ�ˮ������_______ ��������
��4�����ֻ������ܵ�Һ�壬��ˮ���ͣ�����_______ ��������