微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 反应N2+3H2═2NH3刚开始时,N2的浓度为3mol/L,H2的浓度为5mol/L.3min后测得NH3浓度为0.6mol/L,则此时间内,下列反应速率表示正确的是( )
A.v(NH3)=0.2mol/(L?s)
B.v(N2)=1.0mol/(L?min)
C.v(H2)=1.67mol/(L?min)
D.v(H2)=0.3mol/(L?min)
2、填空题 在一定温度下将2 mol A和2 mol B两种气体混合于某2L密闭容器中,发生如下反应:3A(g)+B(g) 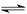 2C(g)+2D(g),2 min末反应达到平衡状态,生成了0.8 mol D,请填写下列空白:
2C(g)+2D(g),2 min末反应达到平衡状态,生成了0.8 mol D,请填写下列空白:
(1)如果缩小反应容器的体积,使压强增大,平衡体系中C的物质的量浓度_____________,C的质量分数___________,容器内气体的平均密度________________,平均相对分子质量________________。(填“增大”、“减小”或“不变”)
(2)如果上述反应在相同条件下从逆反应开始进行,开始加C和D各4/3mol,要使平衡时各物质的物质的量与原平衡相等,则还应加入__________物质___________mol。
3、选择题 在密闭容器中进行如下反应:I2(g)+H2(g)  2HI(g),已知I2、H2、HI的起始浓度分别为0.1mol/L、0.3mol/L、0.2mol/L,在一定条件下当反应达到平衡时,各物质的浓度有可能是(??)
2HI(g),已知I2、H2、HI的起始浓度分别为0.1mol/L、0.3mol/L、0.2mol/L,在一定条件下当反应达到平衡时,各物质的浓度有可能是(??)
A.HI为0.4mol/L
B.H2为0.15mol/L
C.I2为0.2mol/L
D.HI为0.35mol/L
4、填空题 (15分)Ⅰ.在一个容积固定为2L的密闭容器中,发生反应:aA (g) + bB(g)  pC(g)?△H=?反应情况记录如下表:
pC(g)?△H=?反应情况记录如下表:
时间/(min)
| n(A)/( mol)
| n(B)/( mol)
| n(C)/( mol)
|
0
| 1
| 3
| 0
|
第2 min
| 0.8
| 2.6
| 0.4
|
第4 min
| 0.4
| 1.8
| 1.2
|
第6 min
| 0.4
| 1.8
| 1.2
|
第8 min
| 0.1
| 2.0
| 1.8
|
第9 min
| 0.05
| 1.9
| 0.3
请根据表中数据仔细分析,回答下列问题:
(1)第2min到第4min内A的平均反应速率V(A)=????????????????mol?L-1? min-1
(2)由表中数据可知反应在第4min到第6min时处于平衡状态,若在第2min、第6min、第8 min时分别改变了某一个反应条件,则改变的条件分别可能是:
①第2min????????????????????????????或??????????????????????????????????;
②第6min??????????????????????????????????????;
③第8 min?????????????????????????????????????。
(3)若从开始到第4 min建立平衡时反应放出的热量为235.92kJ则该反应的△H=???????。
(4)反应在第4 min建立平衡,此温度下该反应的化学平衡常数K=??????????????.
Ⅱ.已知:常温下,A酸的溶液pH=a, B碱的溶液pH=b
(1)若A为盐酸,B为氢氧化钡,且a=3,b=11,两者等体积混合,溶液的pH为??????????????。
A.大于7????????????? B.等于7????????????C. 小于7
(2)若A为醋酸,B为氢氧化钠,且a=4,b=12,那么A溶液中水电离出的氢离子浓度为
????????????mol?L-1,B溶液中水电离出的氢离子浓度为?????????????mol?L-1。
(3)若A的化学式为HR,B的化学式为MOH,且a+b=14,两者等体积混合后溶液显碱性。则混合溶液中必定有一种离子能发生水解,该水解反应的离子方程式为:
?????????????????????????????????????????????????????????????。
5、选择题 一定温度下,在容积为2L的恒容密闭容器中充入4 mol N2O3,发生反应:N2O3(g)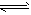 N2O(g)+O2(g); N2O(g)+O2(g);
N2O3(g)+O2(g)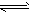 N2O5(g),达到平衡时,测得c(N2O5)为0.7 mol/L,c(O2)为0.5 mol/L,则 [???? ] N2O5(g),达到平衡时,测得c(N2O5)为0.7 mol/L,c(O2)为0.5 mol/L,则 [???? ]
A.c(N2O3)=0.8 mol/L
B.c(N2O3)=0.2 mol/L
C.c(N2O)=0.5 mol/L
D.c(N2O) =1.2 mol/L
|