微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、简答题 现有下列短周期元素性质的数据:
????元素编号
元素性质 | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧
原子半径
(10-10m)
0.74
1.02
1.52
1.10
0.99
1.86
0.75
1.43
|
最高或最
低化合价
+6
+1
+5
+7
+1
+5
+3
-2
-2
-3
-1
-3
回答下列问题:
(1)元素③在周期表中位置是______;?元素④与元素⑦相比较,气态氢化物较稳定的是______(填化学式);
(2)元素①是______(写元素符号),元素⑥是______(写元素符号),二者按照原子个数比为1:1形成的化合物与水反应的化学方程式为______;
(3)元素⑤与元素②的非金属性强弱顺序为______(写元素符号),元素⑤的单质加入到元素②的氢化物的水溶液中,反应的化学方程式为______;
(4)用电子式表示元素①氢化物的形成过程______;写出元素⑦氢化物的电子式______;写出实验室制元素⑤单质的化学反应方程式______.
参考答案:+1价的③、⑥,一定是碱金属Li和Na,而原子半径⑥>③,故
本题解析:
本题难度:一般
2、选择题 下列有关化学用语的说法中不正确的是
[???? ]
A.-OH与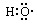 都表示羟基 都表示羟基
B.CH4Si的结构式: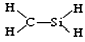
C.CH4分子的球棍模型:
D.次氯酸分子的电子式: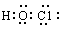
参考答案:B
本题解析:
本题难度:简单
3、选择题 氯化硼的熔点为-107℃,沸点为12.5℃,在其分子中键与键之间的夹角为120°,它能水解,有关叙述正确的是( )
A.氯化硼分子呈正三角形,属非极性分子
B.氯化硼中心原子采用?sp杂化
C.氯化硼分子中含非极性键
D.其分子空间结构类似NH3
参考答案:A.三氯化硼中的硼为sp2杂化,无孤对电子,分子中键与键之间
本题解析:
本题难度:一般
4、选择题 下列物质中,属于含有共价键的离子化合物的是( )
A.KOH
B.Br2
C.MgCl2
D.H2S
参考答案:A
本题解析:
本题难度:简单
5、填空题 ⅤA族的氮、磷、砷(As)、锑(Sb)等元素在化合物中常表现出多种氧化态,含ⅤA族元素的化合物在科研和生产中有许多重要用途。请回答下列问题:
(1)N、P、As原子的第一电离能由大到小的顺序为???????????(用元素符号表示)。
(2)As原子核外M层电子的排布式为?????????????????????????????????。
(3)叠氮化钠(NaN3)用于汽车安全气囊中氮气的发生剂,写出与N互为等电子体的分子的化学式???????(任写一种即可)。
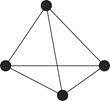
图1
(4)白磷(P4)的结构如图1所示,P原子的轨道杂化方式是???????。
(5)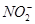 可以与许多金属离子形成配合物,例如[ Co(NO2)6]3-,它可以用来检验K+,其反应如下:3K++[Co(NO2)6]3-=K3[Co(NO2)6]↓(亮黄色)。 可以与许多金属离子形成配合物,例如[ Co(NO2)6]3-,它可以用来检验K+,其反应如下:3K++[Co(NO2)6]3-=K3[Co(NO2)6]↓(亮黄色)。
①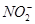 的立体构型是???????。 的立体构型是???????。
②在K3[Co(NO2)6]中,中心离子的配位数为???????。
(6)天然氨基酸的命名常用俗名(根据来源与性质),例如,最初从蚕丝中得到的氨基酸叫丝氨酸(HOCH2CHCOOHNH2)。判断丝氨酸是否存在手性异构体????????(填“是”或“否”)。
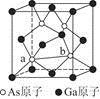
图2
(7)砷化镓为第三代半导体,以其为材料制造的灯泡寿命长,耗能少。已知立方砷化镓晶胞的结构如图2所示,其晶胞边长为cpm,则密度为???????g・cm-3(用含c的式子表示,设NA为阿伏加德罗常数的值),a位置As原子与b位置As原子之间的距离为???????pm(用含c的式子表示)。
参考答案:(1)N>P>As
(2)3s23p63d
本题解析:(1)同一主族元素的原子半径越大,越易失去电子,电离能越小。(3)等电子体指原子总数相等,价电子总数相等的粒子。(4)白磷分子中每个P原子有一个孤电子对,形成了3个σ键,故采取sp3杂化。(5)NO中氮原子的孤电子对数为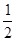 ×(5+1-2×2)=1,与O原子形成了2个σ键,采取sp2杂化, ×(5+1-2×2)=1,与O原子形成了2个σ键,采取sp2杂化, 本题难度:一般 本题难度:一般
|