????����
���� | ��A | ��A | ��A | ��A | ��A | ��A | ��A | 0��
2
��
��
��
3
��
��
��
��
��
4
��
��1��������ǿ�Ļ�����ĵ���ʽ�ǣ�______��
��2��д���ܵ�����������ˮ����͢ߵ�����������ˮ���ﷴӦ�����ӷ���ʽ______
��3���õ���ʽ��ʾԪ�آ���Ļ�������γɹ��̣�______���û���������______������ۡ������ӡ��������
�ο��𰸣���1��������ǿ��Ԫ�ض�Ӧ�Ľ����Ľ�������ǿ��ӦΪ�ܣ���KԪ��
���������
�����Ѷȣ�һ��
4������� (1)п��һ����Ҫ�Ľ���,п���仯�������Ź㷺��Ӧ�á�
��ָ��пԪ�������ڱ��е�λ��:������������,����������,������������?
��NH3�����е�ԭ�ӵ��ӻ��������Ϊ��������,��̬��ԭ�ӵĺ�������Ų�ʽ������?
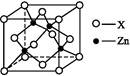
����ͼ��ʾп��ij�ǽ���Ԫ��X�γɵĻ����ᄃ��,����Zn��Xͨ�����ۼ����,�û�����Ļ�ѧʽΪ��������;�û�����ľ����۵�ȸɱ��ߵö�,ԭ��������?
(2)������Ϊһ�������Դ,���������Ĵ�������,C60������������ϡ�
����֪���ʯ�е�C��C�ļ���Ϊ154.45 pm,C60��C��C����Ϊ140~145 pm,��ͬѧ�ݴ���ΪC60���۵���ڽ��ʯ,����Ϊ�Ƿ���ȷ��������,��������������?
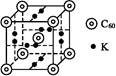
�ڿ�ѧ�Ұ�C60��K������һ��������һ�ָ���ϩ������,�侧������ͼ��ʾ,�������ڵ���ʱ��һ�ֳ����塣�����ʵ�Kԭ�Ӻ�C60���ӵĸ�����Ϊ����������?
�ۼ�C60��,��ѧ���ֺϳ���Si60��N60��C��Si��Nԭ�ӵ縺���ɴ�С��˳��������������Si60������ÿ����ԭ��ֻ�����ڵ�3����ԭ���γɹ��ۼ�,��ÿ����ԭ������㶼����8�����ȶ��ṹ,��Si60�����Цм�����ĿΪ����������?
�ο��𰸣�(1)���ġ���B��ds����sp3�ӻ���1s22s22p3����
���������(1)�ٴ�K��ʼ������ZnΪ12,��������Ų�ʽ[Ar]3d104s2;�۾����к���X�ĸ���=8��+6��=4,Zn�ĸ���Ϊ4;���Zn��Xͨ�����ۼ���Ͽ�֪�þ�������ԭ�Ӿ���;(2)��Si����������Ϊ4,��3����ԭ���γ�3���Ҽ�,����1��������3����ԭ�����е�һ���γɦм�,����һ����ԭ���γɵĦм�Ϊ��,һ��Si60�����к���60��Siԭ���γ�30���м�
�����Ѷȣ�һ��
5��ѡ���� ���л�ѧ������д��ȷ���ǣ�������
A�������Ļ�ѧʽΪKAlSO4?12H2O
B�������ӵĽṹʾ��ͼΪ��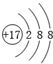
C������ĵ��뷽��ʽ��H2SO4�TH2++SO42-
D������Ļ�ѧʽ��NaCO3
�ο��𰸣�A�������к���2����������ӣ������Ļ�ѧʽΪKAl��SO4��
���������
�����Ѷȣ�һ��
|