微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 用NA表示阿伏加德罗常数的,下列叙述正确的是
A.1.8g重水(D2O)中含NA个中子
B.标准状况下,1mol SO3 的体积约为22.4L
C.常温常压下,46gNO2与N2O4的混合气体中含有的原子总数为3NA
D.足量的铜与含2 mol H2SO4的浓硫酸充分反应,可生成NA个SO2分子
参考答案:C
本题解析:
A.不正确,1.8g重水(D2O)中含1.8g ÷20g/mol×10NA=0.9NA个中子; B.不正确,标准状况下, SO3 为固体; C.正确; D.不正确,铜与稀H2SO4不反应;选C。
本题难度:一般
2、选择题 设NA表示阿伏加德罗常数的值,下列叙述不正确的是
A.标准状况下,11.2 L四氯化碳所含分子数为0.5NA
B.0.1molNa2O2与足量CO2反应,转移电子数为0.1NA
C.1L 1 mol・L-1的FeCl3溶液中Fe3+的数目小于NA
D.在标准状况下,11.2L氖气中含有氖原子数为0.5NA
参考答案:A
本题解析:
答案:A
A、不正确,标准状况下,四氯化碳为液态;
B、正确,Na2O2中两-1价的氧,一个升高一个降低;
C、正确,Fe3+水解;
D、正确,氖分子是单原子分子。
本题难度:一般
3、选择题 质量分数为a%,物质的量浓度为c mol・L-1的NaCl溶液,蒸发溶剂,恢复到原来的温度,若物质的量浓度变为2c mol・L-1,则质量分数变为(蒸发过程中没有晶体析出,且NaCl溶液的密度大于1g/mL)
A.等于2a%
B.大于2a%
C.小于2a%
D.无法确定
参考答案:C
本题解析:
试题分析:质量分数为a%,物质的量浓度为c mol?L-1的NaCl溶液,设密度是ρ1,所以c=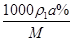 质量分数为a%,物质的量浓度为2c mol?L-1的NaCl溶液,设密度是ρ2,质量分数是w%,所以2c=
质量分数为a%,物质的量浓度为2c mol?L-1的NaCl溶液,设密度是ρ2,质量分数是w%,所以2c=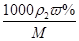 ,整理得
,整理得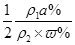 氯化钠的密度小于水的密度,浓度越大,密度越小,所以ρ1>ρ2,即w%<2a%.答案选C.
氯化钠的密度小于水的密度,浓度越大,密度越小,所以ρ1>ρ2,即w%<2a%.答案选C.
考点:溶质的质量分数
本题难度:一般
4、填空题 (9分)填写下列表格:
物质
| 分子数
| 质量/g
| 物质的量/mol
| 摩尔质量/ g・mol -1
|
氮气
| ?
| 14
| ?
| ?
|
H2SO4
| 3.01×1023
| ?
| ?
| ?
|
H2O
| ?
| ?
| 2
| ?
?
参考答案:
?
?
?
?
?
?
本题解析:
试题分析:根据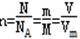 计算。 计算。
(1)n(N2)=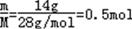 =0.5mol,N(N2)=n?NA=0.5mol×6.02 =0.5mol,N(N2)=n?NA=0.5mol×6.02
本题难度:一般
5、选择题 下列溶液中溶质的物质的量浓度为1mol/L的是( )
A.将40 g NaOH溶解在1L水中
B.将1 L 10mol/L的浓盐酸加入9 L水中
C.将22.4 L HCl气体溶于水配成1 L溶液
D.将10g NaOH溶解在少量水中,再加蒸馏水直到溶液体积为250mL
参考答案:D
本题解析:
试题分析:物质的量浓度是用单位体积的溶液中含有溶质的物质的量来表示的溶液组成。A是溶剂的体积,不是溶液的体积。错误。B物质的微粒间有间隔,所以体积不能相加,1 L 10mol/L的浓盐酸加入9 L水中得到的溶液体积不是10L。错误。C气体的体积受温度的影响较大,不指名体积是在什么条件下的没有意义。错误。DC(NaOH)=(m/M)/V=(10g/40g/mol)÷0.25L=1mol/L.正确。
考点:考查物质的量浓度的有关计算的知识。
本题难度:一般
|