0.1mol/L
����˵����ȷ���ǣ���?��
A.��c(K+)��ͬ???????????????? B.��c(Cl��)��ͬ???????? C.��ȫ��ͬ?????????????? D.��ȫ��ͬ
�ο��𰸣�C
����������������ʶ���ɼ���ѧʽ��֪��������Ũ�ȶ���0.7mol/L��������Ũ�ȶ���0.3mol/L�����Դ�ѡC��
�����Ѷȣ�һ��
2��ѡ���� ��NAΪ�����ӵ�������ֵ������˵����ȷ����(����)
�ٳ��³�ѹ�£�17 g��(��14CH3)��������������Ϊ9NA
�ڳ��³�ѹ�£�6.4 g Cu��40 mL 10 mol��L��1ŨHNO3���ã�����NO2���ӵ���ĿΪ0.2NA
��1.6 g�����к��е�C��H����ĿΪ0.1NA
��ij�¶�ʱ��1 L pH��6�Ĵ�ˮ�к���1.0��10��6NA��H��
��7.8 g �к��е�̼̼˫����ĿΪ0.3NA �к��е�̼̼˫����ĿΪ0.3NA
��20 g������������ԭ����ĿΪNA
��25��ʱ��pH��12��NaHCO3��Һ�к���OH������ĿΪ0.01NA
�ຬNA�������ӵ�Na2O2����ˮ�γ�1 L��Һ����Ũ��Ϊ1 mol��L��1
A���٢ڢ�
B���ܢ�
C���ۢݢ�
D���ڢۢݢ�
�ο��𰸣�B
�������������14C��������Ϊ8����17 g��14CH3��������������Ϊ8NA���ٴ������ŷ�Ӧ�Ľ��У�ŨHNO3���ϡ����NO��������NO2������С��0.2NA���ڴ���1 mol�����к���4 mol C��H����1.6 g����Ϊ0.1 mol���京�е�C��H����ĿΪ0.4NA���۴�����pH����lg c(H��)֪������ȷ�� �����Ѷȣ�һ�� �����Ѷȣ�һ��
3��ѡ���� �谢���ӵ�������NA������ֵΪnA,����˵����ȷ���ǣ�??��
A��1molCl2������Fe��Ӧ��ת�Ƶĵ�����Ϊ3nA
B��1.5 mol NO2������H2O��Ӧ��ת�Ƶĵ�����ΪnA
C�����³�ѹ�£�46 g��NO2��N2O4������庬�е�ԭ����Ϊ3nA
D��0.10mol Fe��������ˮ������Ӧ���ɵ�H2������Ϊ0.10nA
�ο��𰸣�B��C
���������Fe������ʹFe3+��ԭΪFe2+��A����3NO2+H2O==2HNO3+NO����֪B��ȷ��C�У��ɰ�N2O4����2NO2������1moLNO2��������3molԭ�ӣ�Ҳ�����ü��˷���������ȫ��NO2��ȫ��N2O4���ǣ�Ҳ�ɵó������3Fe+4H2O===Fe3O4+4H2�����ɷ��̿�֪D����
�����Ѷȣ�һ��
4������� (6��)ͬ��ͬѹ�£�ͬ�����N2��SO2������֮��Ϊ????????????�����ʵ���֮��Ϊ???????????��ԭ������֮��Ϊ???????????��Ħ������֮��Ϊ???????????������֮��Ϊ????????????���ܶ�֮��Ϊ???????????��
�ο��𰸣���1��1:1��2��1:1 ��3��2:3��4��7:16 ��5��
����������������ʵ������йؼ��㡣
���ݰ����ӵ����ɿ�֪��ͬ��ͬѹ�£�ͬ�����N2��SO2������֮��Ϊ1:1�����Ը���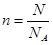 ��֪�����ʵ���֮��Ϊ1:1�����ݻ�ѧʽ��֪��ԭ������֮��Ϊ1��2:1��3��2:3�����ߵ���Է��������ֱ���28��64������Ħ������֮��Ϊ28�U64��7:16���������ʵ�����ͬ����������֮����7:1 ��֪�����ʵ���֮��Ϊ1:1�����ݻ�ѧʽ��֪��ԭ������֮��Ϊ1��2:1��3��2:3�����ߵ���Է��������ֱ���28��64������Ħ������֮��Ϊ28�U64��7:16���������ʵ�����ͬ����������֮����7:1
�����Ѷȣ�һ��
5��ѡ���� ��O2��SO2��SO3��������Ϊ2��4��5ʱ�����ǵ����ʵ���֮��Ϊ[???? ]
A��2��4��5??
B��1��2��3
C��1��1��1??
D��2��2��3
�ο��𰸣�C
���������
�����Ѷȣ���
|