微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 决定主族元素在元素周期表中所处位置的是该元素原子的[???? ]
A.质量数
B.中子数
C.次外层电子数
D.电子层数和最外层电子数
2、选择题 下列关于元素周期表和元素周期律的说法中错误的是[???? ]
A.Li、Na、K元素的原子核外电子层数随着核电荷数的增加而增多 ??
B.第二周期元素从Li到F,非金属性逐渐增强 ??
C.因为Na比K容易失去电子,所以Na比K的还原性强 ??
D.O与S为同主族元素,且O比S的金属性强
3、选择题 元素在周期表中的位置,反映了元素的原子结构和元素的性质,下列说法正确的是[???? ]
A.同一元素不可能既表现金属性,又表现非金属性
B.第三周期元素的最高正化合价等于它所处的主族序数
C.短周期元素形成离子后,最外层电子都达到8电子稳定结构
D.同一主族的元素的原子,最外层电子数相同,化学性质完全相同
4、选择题 短周期主族元素A、B、C、D,原子序数依次增大。A、C的原子序数的差为8,A、B、C三种元素原子的最外层电子数之和为15,B原子最外层电子数等于A原子最外层电子数的一半。 下列叙述正确的是[???? ]
A.原子半径:A<B<C<D
B.非金属性:A>C
C.最高价氧化物对应水化物的酸性:D<C
D.单质B常温下能溶于浓硝酸
5、填空题 在温度t1和t2下,X2(g)和H2反应生成HX的平衡常数如下表
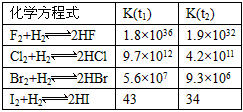
⑴已知t2>t1,HX的生成反应是________反应(填“吸热”或“放热”)。
⑵HX的电子式是________。
⑶共价键的极性随共用电子对偏移程度的增大而增强,HX共价键的极性由强到弱的顺序是________。
⑷X2都能与H2反应生成HX,用原子结构解释原因:________________。
⑸K的变化体现出X2化学性质的递变性,用原子结构解释原因:________________,原子半径逐渐增大,得电子能力逐渐减弱。
⑹仅依据K的变化,可以推断出:随着卤素原子核电荷数的增加,________(选填字母)。
a. 在相同条件下,平衡时X2的转化率逐渐降低
b. X2与H2反应的剧烈程度逐渐减弱
c. HX的还原性逐渐减弱
d. HX的稳定性逐渐减弱