微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 根据现行元素周期表的排布规律,如果第七周期排满,下列预测正确的是[???? ]
A.第七周期共有50种元素
B.第七周期最后一种元素不与任何物质发生反应
C.第七周期ⅦA族元素的原子在化学反应中可以得到1个电子
D.第七周期任何一种元素的原子最外层上不超过8个电子
2、简答题 实验题:
某化学兴趣小组做了如下三个实验:
实验A:集气瓶中放青色、未熟的水果(蔬菜),盖上玻璃片;
实验B:集气瓶中放青色、未熟的水果(蔬菜),通入一定量的乙烯;
实验C:集气瓶中放青色、未熟的水果(蔬菜),瓶底放少量KMnO4固体,盖上玻璃片.
请根据所学化学知识完成下列问题:
(1)预期实验结果:水果成熟的先后顺序是______(用序号填写)
(2)解释你的预期结果的原因______.
为探究?Na、Mg、Al的金属活动性顺序,某课外小组同学进行了如下实验:
| 实验步骤 | 1将一小块金属钠放入滴有酚酞溶液的冷水中;
2将一小段用砂纸打磨后的镁带放入试管中,加入少量水,加热至水沸腾,冷却后,向试管中滴加酚酞溶液;
3将一小段镁带投入稀盐酸中;
4将一小片铝投入稀盐酸中.
实验现象
A剧烈反应,迅速生成大量的气体
B浮在水面上,熔成小球,不断游动,小球渐小最终消失,溶液变红
C反应不剧烈,产生无色气体
D有气体产生,溶液变成红色
(1)请在下表中填写与实验步骤对应的实验现象序号:
| 实验步骤 | 1 | 2 | 3 | 4
实验现象
(2)请写出钠与水反应的方程式______.
(3)请你补充该小组同学用原子结构理论对上述实验结论的解释:
同周期元素从左到右核电荷数逐渐增多,原子半径逐渐______,失电子能力逐渐______,因此______性逐渐减弱.
3、选择题 下列各组元素中,按最高正价递增的顺序排列的是
A.C、N、O、F
B.K、Mg、C、S
C.F、Cl、Br、I
D.Li、Na、K、Rb
4、选择题 下列叙述不正确的是( )
A.NaOH的碱性介于KOH和Mg(OH)2之间
B.Li、Na、K、Rb元素金属性依次增强
C.Na+、Mg2+、Al3+的离子半径依次增大
D.H2SiO3、H2CO3、H2SO4酸性依次增强
5、推断题 A-F六种元素中,除C外其他均为短周期元素,它们的原子结构或性质如下表所示

请回答下列问题:
(1)A在元素周期表中的位置是___________;A与E形成的化合物的电子式是___________。
(2)C的某种氯化物的浓溶液可以腐蚀印刷电路板上的金属铜,此反应的离子方程式是_____________________________。
(3)B的单质与D的氢化物在一定条件下反应生成BD和另一产物的化学方程式是___________________。
(4)F的盐酸盐水溶液呈酸性,原因是___________________(用离子方程式表示);F的单质与C、D形成的相对分子质量为160的化合物在一定条件下反应的化学方程式是____________________。
(5)A与F形成的合金是重要的工业材料。某同学仅使用天平和下图所示的装置,粗略测定某些数据即可求出该合金中A元素的含量。(装置中因空气质量引起的误差忽略不计)
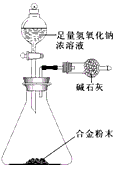
①实验需要测定三个物理量:合金的质量m以及a和b。a是_______;b是________。
②合金中A元素的质量分数是___________(用含m、a、b的式子表示)。
|
|