微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下表各组物质之间通过一步反应就能实现如?

?所示转化的是( )
| 物质选项 | a | b | c | m
A
N2
NO
HNO3
O2
B
Cl2
FeCl3
FeCl2
Fe
C
Na2CO3
NaHCO3
NaOH
CO2
D
CH3CH2OH
CH3CHO
CH3COOH
O2
|
A.A
B.B
C.C
D.D
参考答案:B
本题解析:
本题难度:一般
2、推断题 (1)物质X、Y是中学化学中的常见物质,X既能与稀硫酸反应,又能与氢氧化钠溶液反应。
①若X为氧化物,X的化学式是________;
②若X与稀硫酸反应生成无色无味的气体A,与浓氢氧化钠溶液加热反应生成气体B。等物质的量的A和B在水溶液中反应又生成X。X与足量稀氢氧化钠溶液反应的离子方程式是____________;
③若X为金属单质,写出X与氢氧化钠溶液反应的化学方程式___________;若Y为非金属单质,Y不能与 浓硫酸或稀硫酸反应,却能与某种酸反应放出氢气,并与氢氧化钠溶液反应放出氢气。写出Y与氢氧化钠溶液反应的化学方程式并用单线桥法标明电子的转移________________。
(2)在宇航器中,可以不断地将座舱内的空气通过盛有金属过氧化物(以过氧化钠为例)的容器,以除去 A。反应的化学方程式是________________。科学家设计出新的航天飞船内的空气更新系统。其中的一步反应是A 和氢气在200℃~ 250℃,镍作催化剂的条件下,生成甲烷和另一种物质。该反应的化学方程式
是________________。
参考答案:(1)①Al2O3;②NH4++HCO3-+2OH-=NH3・H2O+CO32-+H2O;③2Al+2NaOH+2H2O=2NaAlO2+3H2↑ ; (2)2CO2+2Na2O2=2Na2CO3+O2;CO2+4H2
(2)2CO2+2Na2O2=2Na2CO3+O2;CO2+4H2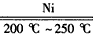 CH4+2H2O
CH4+2H2O
本题解析:
本题难度:一般
3、填空题 已知在不同条件下有如下转化关系:A+B→C+D
A、B、C、D分别代表中学化学中常见的物质(或粒子)请根据下列要求填空(有多种情况的,只写其中的一种情况);
(1)若A是金属单质,C是固态非金属单质,B、D为化合物,则化学方程式为______.
(2)若A、B、C、D均为10电子粒子,则离子方程式为______.
(3)若A、B是易溶物质,C、D是难溶物质,则A、B的化学式为______.
参考答案:(1)若A是金属单质,C是固态非金属单质,B、D为化合物,Mg与二氧化碳反应生成MgO与碳,符合转化关系,反应方程式为:2Mg+CO2点燃.2MgO+C,
故答案为:2Mg+CO2点燃.2MgO+C;
(2)若A、B、C、D均为10电子粒子,铵根离子与氢氧根离子生成氨气与水,符合转化关系,反应方程式为:NH4++OH-△.NH3↑+H2O,
故答案为:NH4++OH-△.NH3↑+H2O;
(3)若A、B是易溶物质,C、D是难溶物质,Ba(OH)2、CuSO4之间的反应或Ba(OH)2、MgSO4之间的反应,符合转化关系,
故答案为:Ba(OH)2、CuSO4或Ba(OH)2、MgSO4.
本题解析:
本题难度:简单
4、实验题 聚合硫酸铁又称聚铁,化学式为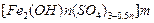 ,广泛用于污水处理。
,广泛用于污水处理。
某化学兴趣小组在实验室利用硫酸厂烧渣(主要成分为铁的氧化物及少量FeS、Si02等)
制备聚铁和绿矾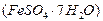 的过程如下:
的过程如下:

(1) 验证固体W焙烧后产生的气体含有SO2的方法是?。
(2) 实验室制各、收集干燥的SO2,所需仪器如下。装置A产生SO2,按气流方向连接各
仪器接口,顺序为a→?→?→?→?→f,装置D的作用是?,装置E中NaOH溶液的作用是?。

(3) 制备绿矾时,内溶液X中加入过量?,充分反应后,经?
操作得到溶液Y,再经浓缩,结晶等步骤得到绿矾。
(4)溶液Z的pH影响聚铁中铁的质量分数,用PH试纸测定溶渡pH的操作方法为?
?。
参考答案:(1) 将气体通入品红溶液,溶液褪色,加热恢复原色(合理即可)(3分)
(2) decb(2分)防止倒吸(2分)?吸收多余的SO2(2分)
(3) 铁屑(2分)过滤(2分)
(4) 将一小块pH试纸放在洁净干燥的表面皿上(或点滴板)上,用玻璃棒蘸取少量待测液沾在试纸上,与标准比色卡对照(3分)
本题解析:略
本题难度:一般
5、填空题 如图是中学化学中常见物质的转化关系,部分物质和反应条件略去.

(1)单质B的化学式是______,写出物质A的一种用途______.
(2)写出单质B与强碱溶液反应的离子方程式______,写出由沉淀J生成?H溶液的离子方程式______.
(3)写出白色沉淀L变为红褐色沉淀G的化学反应方程式______.
参考答案:红棕色固体A为Fe2O3,氧化物D能与NaOH反应,应为Al2O3,则B为Al,C为Fe,F为H2,E为FeCl2,L为Fe(OH)2,G为4Fe(OH)3,H为NaAlO2,I为AlCl3,
J为Al(OH)3,
(1)由以上分析可知B为Al,A为Fe2O3,常用于制油漆等,故答案为:Al;制油漆等;
(2)Al与氢氧化钠等强碱溶液反应生成氢气,反应的离子方程式为2Al+2OH-+2H2O=2AlO2-+3H2↑,Al(OH)3具有两性,可与NaOH反应,反应的离子方程式为Al(OH)3+OH-=AlO2-+2H2O,
故答案为:2Al+2OH-+2H2O=2AlO2-+3H2↑;Al(OH)3+OH-=AlO2-+2H2O;
(3)Fe(OH)2不稳定,可被氧化生成Fe(OH)3,反应的化学方程式为4Fe(OH)2+2H2O+O2=4Fe(OH)3,
故答案为:4Fe(OH)2+2H2O+O2=4Fe(OH)3.
本题解析:
本题难度:一般