微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 20℃时,H2S的饱和溶液1L,浓度约0.1?mol・L-1,其电离方程式第一步为:H2S H++HS-;第二步:HS-
H++HS-;第二步:HS- H++S2-,若使溶液H+、S2-浓度同时减小,可采取的措施是(? )
H++S2-,若使溶液H+、S2-浓度同时减小,可采取的措施是(? )
A.加入适量NaOH固体
B.加入适量水
C.通入适量SO2
D.加入适量CuSO4固体
参考答案:BC
本题解析:(1)加水时溶液浓度降低,使溶液中H+、S2-的浓度降低。(2)通入适量的SO2发生反应2H2S+SO2 3S↓+2H2O,使H2S溶液浓度降低,H+、S2-浓度减小。
3S↓+2H2O,使H2S溶液浓度降低,H+、S2-浓度减小。
本题难度:一般
2、填空题 (11分)
(I)在甲烧杯中放入盐酸,乙烧杯中放入醋酸,两种溶液的体积和pH都相等,向两烧杯中同时加入质量不等的锌粒,反应结束后得到等量的氢气;则
(1) 烧杯中放入锌的质量大(填“甲”或“乙”);
(2) 烧杯中的酸过量(填“甲”或“乙”);
(3)反应开始后乙烧杯中的c(H+)始终比甲烧杯中的c(H+) (填“大”或“小”)。
(II)物质的量浓度相同的等体积的两份溶液A和B,A为盐酸,B为醋酸,分别和等质量的Zn反应,则下列说法正确的是:
①产生的H2质量一定相同 ②产生H2的质量一定不同
③仅有一份溶液中存在锌,则一定是盐酸 ④等倍数稀释后的反应速率A>B
⑤产生等量H2所需时间A>B ⑥产生等量H2,盐酸和醋酸一定都有剩余
(III)向体积都为1L,pH都等于2的盐酸和醋酸溶液中投入0.3g Zn,则下图中比较符合客观事实的曲线是 。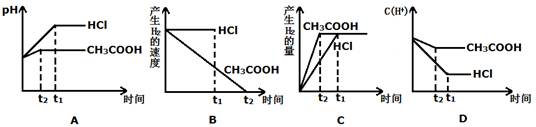
参考答案:(11分)
(Ⅰ)(1)甲 (2)乙 (3)大 (每空2分)
(Ⅱ)③⑤ (2分)
(Ⅲ)ACD (3分)
本题解析:
试题解析:(I)(1)盐酸为强酸,醋酸为弱酸。体积和pH相等,可得n(HCl)<n(CH3COOH)。由于金属跟盐酸、醋酸的反应都是按1:2的比例进行反应的。因此与盐酸反应的锌应过量。
(2)得到相同质量的氢气,则反应掉的酸的物质的量相等,因此乙中的醋酸应剩余。
(3)反应后甲烧杯中的溶质为ZnCl2,乙烧杯中的溶质为(CH3COO)2Zn和CH3COOH;乙烧杯中的溶液为酸性,因此应开始后乙烧杯中的c(H+)始终比甲烧杯中的c(H+)大。
(Ⅱ)物质的量浓度相同的等体积的两份溶液A和B,A为盐酸,B为醋酸,分别和等质量的Zn反应。⑴若锌完全反应,则产生的H2相等;若醋酸完全反应,则产生的H2不相等。因此①②错误。⑵由于加入的锌的质量相等,而溶液中n(HCl)<n(CH3COOH),因此若有一份溶液中的锌有剩余,则应是盐酸中的锌有剩余,故③正确。⑶等倍稀释后,由于稀释促进了醋酸的水解,醋酸中c(H+)增大,因此反应速率增大,故④错误。⑷由于随着反应的进行,盐酸中c(H+)不断减小,而对于醋酸溶液中,c(H+)几乎保持不变,因此产生等量的H2所需的时间A>B,故⑤正确。⑸若产生等量的H2,可以是两种酸都有剩余,也可以是醋酸有剩余,故⑥错误。综上,说法正确的有③⑤。
(Ⅲ) 向体积都为1L,pH都等于2的盐酸和醋酸溶液中投入0.3g Zn,反应后溶液的溶质分别为“ZnCl2和ZnCl2、CH3COOH”,因此A正确。对于选项B、对于产生H2的速率,应是与盐酸反应的会越来越慢;与醋酸反应的,其反应速率基本保持不变,故B错误。选项C、锌的质量相等,其完全反应,因此产生H2的质量想的,再结合对选项B的分析,可知,C图像表示的正确。选项D、随着反应的进行,盐酸中c(H+)不断减小,但醋酸会不断电离出H+,因此其浓度减小的较慢,因此选项D说法正确。综上,答案选ACD。
考点:电解质溶液;弱酸的电离
点评:本题考查电解质溶液的相关知识,是高考的常见考题,掌握弱酸的电离是解题的关键。对于此类题型,应加强训练总结,以求达到举一反三的效果。
本题难度:一般
3、填空题 某二元弱酸溶液按下式发生一级和二级电离:
H2A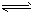 H++HA-
H++HA-
HA- H++A2-。
H++A2-。
已知相同浓度时的电离度,a(H2 A)>a(HA-),设有下列四种溶液:
A.0. 01mol/L的H2A溶液
B.0. 01mol/L的NaHA溶液
C.0. 02mol/L的HCl与0.04mol/L的NaHA溶液等体积混合液
D.0. 02mol/L的NaOH与0.02mol/L的NaHA溶液等体积混合液
据此填写下列空白(填代号):
(1)c(H+)最大的是____,最小的是____。
(2)c(H2A)最大的是____,最小的是____。
(3)c(A2-)最大的是____,最小的是____。
参考答案:(1)A ;D
(2)C ;D
(3)D ;A
本题解析:
本题难度:一般
4、选择题 (2我c4?广州一模)对于常温下我.cmol?L-c氨水和我.cmol?L-c醋酸,下列说法正确的是( )
A.0.1mol?L-1氨水,溶液的pH=13
B.0.1mol?L-1氨水加水稀释,溶液中c(H+)和c(OH-)都减小
C.0.1mol?L-1醋酸溶液中:c(H+)=c(CH3COO-)
D.0.1mol?L-1醋酸与0.1mol?L-1 NaOH溶液等体积混合所得溶液中:c(Na+)>c(CH3COO-)>c(OH-)>c(H+)
参考答案:A.一水合氨是弱电解质,在水溶液里部分电离,所以氨水溶液中存在一水合氨电离平衡,则0.3mo3?3-3氨水,溶液的pH<33,故A错误;
B.加水稀释促进一水合氨电离,氢氧根离子增多t数小于溶液体积增大倍数,所以溶液中氢氧根离子浓度减小,温度不变,水的离子积常数不变,则氢离子浓度增大,故B错误;
C.任何电解质溶液中都存在电荷守恒,根据电荷守恒得c(H+)=c(CH3COO-)+c(OH-),故C错误;
D.等物质的量的醋酸和氢氧化钠混合,二者恰好反应生成醋酸钠,醋酸钠为强碱弱酸盐,其溶液呈碱性c(OH-)>c(H+),根据电荷守恒得c(Na+)>c(CH3COO-),盐类水解较微弱,所以c(CH3COO-)>c(OH-),该溶液中离子浓度大小顺序是c(Na+)>c(CH3COO-)>c(OH-)>c(H+),故D正确;
故选D.
本题解析:
本题难度:一般
5、选择题 下列物质属于电解质的是
A.蔗糖
B.熔融NaOH
C.氯水
D.铜
参考答案:B
本题解析:分析:在水溶液里或熔融状态下能导电的化合物是电解质,在水溶液里或熔融状态下都不导电的化合物是非电解质.
解答:A.蔗糖在水溶液里或熔融状态下都不导电,属于非电解质,故A错误;
B.熔融NaOH能电离出自由移动的离子,属于电解质,故B正确;
C.氯水是混合物,既不是电解质也不是非电解质,故C错误;
D.铜是单质,所以铜既不是电解质也不是非电解质,故D错误.
故选B.
点评:本题考查了电解质的判断,难度不大,注意电解质和非电解质都必须是化合物,单质和混合物既不是电解质也不是非电解质.
本题难度:简单