微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、实验题 (12分)NO很容易与许多分子迅速发生反应,科学家发现在生物体中不断地产生NO,用于在细胞和细胞间传递信息;NO还参与心血管系统、免疫系统以及中枢和外围神经系统的调控。
(1)实验室用金属铜和稀硝酸制取NO的离子方程式为
________________________________________________________________。
(2)NO是有毒气体,某学生为防止污染,用分液漏斗和烧杯装配了一套简易的、能随开随用、随关随停的NO气体发生装置,如图甲所示。
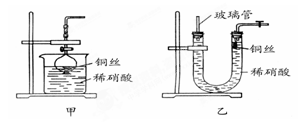
打开分液漏斗的活塞使反应进行,在分液漏斗中实际看到的气体是红棕色的,原因是_________________________________(写化学方程式)。
(3)为证明铜丝与稀硝酸反应生成的确实是NO,某学生另设计了一套如图乙所示的装置制取NO。反应开始时,可以在U形管右端观察到无色的NO气体。长玻璃管的作用是_______________________________________。
(4)假设实验中12.8 g Cu全部溶解,需要通入标准状况下________L O2才能使NO全部溶于水。
(5)用金属铜制取硝酸铜,从节约原料和防止环境污染的角度考虑,下列4种方法中最好的是________(填“甲”“乙”“丙”或“丁”),理由是__________________________________。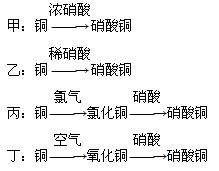
参考答案:(1)3Cu+8H++2NO3-=3Cu2++4H2O+2NO↑?(2)2NO+O2=2NO2
(3)接收被气体压出U形管的液体,防止稀硝酸溢出?(4)2.24L
(5)?丁?制取相同质量的Cu(NO3)2,丁所消耗的HNO3的量最少(原料的利用率最高)且不产生污染环境的气体? (每空2分,共12分)
本题解析:(1)硝酸是氧化性酸,和铜反应的方程式为3Cu+8H++2NO3-=3Cu2++4H2O+2NO↑。
(2)NO极易被氧气氧化生成红棕色的NO2,方程式为2NO+O2=2NO2。
(3)由于反应中生成的NO难溶于水,导致压强增大,所以长玻璃导管的作用是接收被气体压出U形管的液体,防止稀硝酸溢出。
(4)12.8g铜是0.2mol,失去电子是0.4mol;由于最终NO又生成硝酸,说明铜失去的电子被氧气得到,根据电子的得失守恒可知,氧气的物质的量是0.1mol,标准状况下的体积是2.24L。
(5)甲乙中均产生大气污染物,丙中原子利用率不高,且氯气有毒,所以正确的答案选丁。
本题难度:一般
2、选择题 常温下,下列各组物质不能用一种试剂通过化学反应区别的是(?)
A.MnO2 CuO FeO
B.(NH4)2SO4 K2SO4 NH4Cl
C.AgNO3 KNO3 Na2CO3
D.Na2CO3 NaHCO3 K2CO3
参考答案:D
本题解析:A中MnO2、CuO、FeO可以用浓HCl区别,其中MnO2和浓HCl混合加热产生黄绿色气体,CuO和浓HCl生成蓝色溶液,FeO和浓HCl生成浅绿色溶液。B中(NH4)2SO4、K2SO4、NH4Cl可以用Ba(OH)2溶液区别,其中(NH4)2SO4和Ba(OH)2混合既产生白色沉淀,又能产生刺激性气味气体,K2SO4和Ba(OH)2混合产生白色沉淀,NH4Cl和Ba(OH)2混合产生刺激性气味气体。C中AgNO3、KNO3、Na2CO3可用HCl区别,其中AgNO3和HCl混合产生白色沉淀,KNO3和HCl混合没有明显现象,Na2CO3和HCl混合产生气体。D中三溶液性质相近,无法用一种试剂通过化学反应区别。
本题难度:简单
3、选择题 ag铜与含bg硝酸的溶液恰好反应,若a∶b= 4∶10.5,则反应中被还原硝酸的质量为
A.bg
B.b/2g
C.3b/4g
D.b/4g
参考答案:D
本题解析:因为铜与硝酸反应时,硝酸的浓度不同,其还原产物是不同的。此题用逆向思维,首先考虑未被还原的硝酸,再换算出被还原的



本题难度:一般
4、选择题 对于下列事实的解释错误的是
A.在蔗糖中加入浓硫酸后出现发黑现象,说明浓硫酸具有脱水性
B.浓硝酸在光照下颜色变黄,说明浓硝酸不稳定
C.常温下,浓硝酸可以用铝罐贮存,说明铝与浓硝酸不反应
D.氨水可使酚酞试剂变为红色,说明氨水显碱性
参考答案:C
本题解析:A.在蔗糖中加入浓硫酸后出现发黑现象,说明浓硫酸具有脱水性,正确;
B.浓硝酸在光照下颜色变黄,是硝酸分解生成的二氧化氮溶于其中的结构,说明浓硝酸不稳定。正确;
C.常温下,浓硝酸可以用铝罐贮存,是铝遇到浓硝酸发生了钝化,并不是不反应;错误;
D.氨水可使酚酞试剂变为红色,说明氨水显碱性。正确;故选C。
点评:浓硫酸具有吸水性和脱水性;二者的区别是前者吸收的是现成的水,后者是把物质中的氢和氧元素按照1:2的水分子的组合脱去,就是说该物质中没有水。
本题难度:简单
5、选择题 对于氨水的组成的叙述正确的是
[? ]
A.只含有氨分子和水分子
B.只含有一水合氨分子和水分子
C.只含有氨分子、水分子和一水合氨分子
D.含有氨分子、水分子、一水合氨分子、铵根离子和氢氧根离子
参考答案:D
本题解析:
本题难度:简单