微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 (6分)二氧化硒(Se)是一种氧化剂,其被还原后的单质硒可能成为环境污染物,通过与浓HNO3或浓H2SO4反应生成SeO2以回收Se。完成下列填空:
(1)Se和浓HNO3反应的还原产物为NO和NO2,且NO和NO2的物质的量之比为1:1。写出Se和浓HNO3的反应方程式?。
(2)已知:Se+2H2SO4(浓) 2SO2↑+SeO2+2H2O
2SO2↑+SeO2+2H2O
2SO2+SeO2+2H2O Se+2SO42-+4H+
Se+2SO42-+4H+
SeO2、H2SO4(浓)、SO2的氧化性由强到弱的顺序是?。
(3)回收得到的SeO2的含量,可以通过下面的方法测定:
①SeO2+KI+HNO3 Se+I2+KNO3+H2O(未配平)
Se+I2+KNO3+H2O(未配平)
②I2+2Na2S2O3 Na2S4O6+2NaI
Na2S4O6+2NaI
实验中,准确称量SeO2样品0.1500g,消耗0.2000 mol・L-1的Na2S2O3溶液25.00 mL,所测定的样品中SeO2的质量分数为?。
参考答案:6分)(1)Se+2HNO3(浓)==H2SeO3+NO↑+NO2↑
或Se+2HNO3(浓)="=" SeO2+NO↑+NO2↑+H2O(2分)
(2)H2SO4(浓)> SeO2> SO2?(2分)?(3)0.925(2分)
本题解析:利用题中信息可知Se和浓HNO3反应,Se被氧化成+4价的H2SeO3,HNO3被还原为NO和NO2,利用电子守恒和题中限定条件(Se和浓HNO3反应的还原产物为NO和NO2,且NO和NO2的物质的量之比为1:1)可知方程式:Se+2HNO3(浓)==H2SeO3+NO↑+NO2↑。利用氧化性:氧化剂>氧化产物,结合方程式可得出:SeO2、H2SO4(浓)、SO2的氧化性由强到弱的顺序是H2SO4(浓)> SeO2> SO2,
(3)可以化合价升降法配平,即Se由+4降至0价,化合价变化单位为4,I由―1升至0价,化合价变化单位为1,根据化合价变化总数相等,则KI的系数为4,SeO2系数为1,然后配平其它原子,在反应1中I-失去电子,SeO2得到电子。根据方程式:
第一个反应方程式得SeO2---2I2
再结合第二个方程式,可知SeO2---2I2---4Na2S2O3
1? 4
X? 0.2000 mol/L×0.025 L
x= 1/4×0.2000 mol/L×0.025 L
m(SeO2)= 1/4×0.2000 mol/L×0.025 L×111 g/mol
即样品中SeO2质量分数为m/0.1500 =0.925
点评:熟练掌握氧化还原反应的相关概念和计算。理解电子守恒法在计算中应用。
本题难度:一般
2、选择题 宁夏的硒砂瓜现今已享誉区内外,西瓜富含硒元素,有延年益寿、抗衰老、抗癌作用,因之得名“硒砂瓜”。二氧化硒(Se)是一种氧化剂,其被还原后的单质硒可能成为环境污染物,通过与浓HNO3或浓H2SO4反应生成SeO2以回收Se。在回收过程当中涉及到如下两个化学反应①SeO2+4KI+4HNO3 Se+2I2+4KNO3+2H2O;
Se+2I2+4KNO3+2H2O;
②Se+2H2SO4(浓) 2SO2↑+SeO2+2H2O下列有关叙述正确的是
2SO2↑+SeO2+2H2O下列有关叙述正确的是
A.SeO2、H2SO4(浓)、I2的氧化性由强到弱的顺序是H2SO4(浓)> SeO2> I2。
B.①中Se是氧化产物,I2是还原产物
C.反应①中KI是氧化剂,SeO2是还原剂
D.反应①中每有0.6 mol I2生成,转移电子数目为2.4NA
参考答案:A
本题解析:在氧化还原反应中氧化剂的氧化性大于氧化产物的,所以SeO2、H2SO4(浓)、I2的氧化性由强到弱的顺序是H2SO4(浓)> SeO2> I2,所以A正确;反应①中,Se的化合价降低,I的化合价升高,所以2是氧化剂,是还原剂,是还原产物,2是氧化产物,、都不正确;反应①中每有0.6 mol I2生成,转移电子1.2mol,D不正确,答案选A。
本题难度:简单
3、选择题 已知:X2、Y2、Z2、W2四种物质的氧化性由强到弱的顺序是W2>Z2>X2>Y2,下列氧化还原反应能够发生的是(?)
A.2NaW+Z2=2NaZ+W2
B.2NaX+Z2=2NaZ+X2
C.2NaY+W2=2NaW+Y2
D.2NaZ+X2=2NaX+Z2
参考答案:BC
本题解析:该题看似考查了如何去判断反应是否可以发生的问题,实质就是氧化性、还原性强弱的判断。判断物质的方法有多种,但的是具体反应判断物质的氧化性、还原性强弱。根据氧化性:氧化剂>氧化产物;还原性:还原剂>还原产物的规律,可知反应A中氧化性:
Z2>W2,和题目所给信息相反,不能发生;反应B中氧化性:Z2>X2,能发生;反应C中氧化性:W2>Y2,能发生;反应D中氧化性:X2>Z2,和题目所给信息相反,不能发生。
本题难度:简单
4、选择题 以元素化合价升降的观点分析下列各化学反应,其中不属于氧化还原反应的是
[? ]
A.Mg+2HCl===MgCl2+H2↑
B.H2+Cl2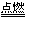 2HCl
2HCl
C.CuO+H2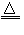 Cu+H2O
Cu+H2O
D.CaCl2+Na2CO3===CaCO3↓+2NaCl
参考答案:D
本题解析:
本题难度:简单
5、选择题 将SO2气体与足量Fe2(SO4)3溶液完全反应后,再加入K2Cr2O7溶液,发生如下两个化学反应:
①SO2+2Fe3++2H2O=SO42-+2Fe2++4H+
②Cr2O72-+6Fe2++14H+=2Cr3++6Fe3++7H2O
下列有关说法错误的是
A.氧化性Cr2O72->Fe3+>SO2
B.Cr2O72-能将Na2SO3氧化成Na2SO4
C.每有1 mol K2Cr2O7参加反应,转移电子的数目为3NA
D.若6.72 L SO2(标准状况)参加反应,则最终消耗0.1 mol K2Cr2O7
参考答案:C
本题解析:A、在氧化还原反应中氧化剂的氧化性强于氧化产物的氧化性,所以根据反应SO2+2Fe3++2H2O=SO42-+2Fe2++4H+可知,Fe3+做氧化剂,SO42-为氧化产物,SO2为还原剂,所以氧化性:Fe3+>SO42->SO2。根据反应Cr2O2- 7+6Fe2++14H+=2Cr3++6Fe3++7H2O可知,Cr2O72-为氧化剂,Fe3+为氧化产物,所以氧化性是Cr2O72->Fe3+,因此氧化性强弱顺序是Cr2O72->Fe3+>SO2,A正确;B、Cr2O72-具有强氧化性,能把Na2SO3氧化成Na2SO4,B正确;C、反应中Cr元素的化合价从+6价降低到+3价,所以每有1 mol K2Cr2O7参加反应,转移电子的数目为6NA,C不正确;D、6.72 L SO2(标准状况)的物质的量=6.72L÷22.4L/mol=0.3mol,反应中失去0.3mol×2=0.6mol电子。1mol K2Cr2O7在反应中得到6mol电子,所以若6.72 L SO2(标准状况)参加反应,则最终消耗0.1 mol K2Cr2O7,D正确,答案选C。
本题难度:一般