微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、推断题 A、B、C、D均为短周期元素,A和B同周期相邻,A和C同主族相邻,三种元素的原子序数之和为31。D元素与A、B、C三元素既不同周期,又不同主族。请回答:
(1)元素符号:A______,B______,C______,D______。
(2)A、B、D组成的离子化合物D4B2A3,其水溶液的pH小于7,原因是(用离子方程式表示)
____________________________。
(3)B、D形成的化合物液态时可发生电离(可由A、D形成的化合物电离推知),电离产生的阴离子的电子式为________________。
参考答案:(1)O;N;S;H
(2)NH4++H2O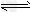
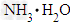 +H+
+H+
(3)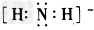
本题解析:
本题难度:一般
2、选择题 在新研制的超导材料中,铊(Tl)是主要组成元素之一。已知铊为第ⅢA族原子序数最大的金属元素。则下列关于铊元素性质的推测中不正确的是
[? ]
A.铊是银白色较软的金属
B.Tl(OH)3与Al(OH)3相似,也是两性氢氧化物
C.铊可以形成氧化物Tl2O3
D.铊与酸反应比铝剧烈
参考答案:B
本题解析:
本题难度:一般
3、选择题 在某稀溶液中含有0.2mol HNO3和x mol H2SO4,向其中加入19.2g铜粉,充分反应后产生的气体在标准状况下的体积为4.48L,则x值至少为
A.0.6
B.0.4
C.0.3
D.0.2
参考答案:
C
本题解析:
本题考查铜与NO3-及H+的反应。铜与稀H2SO4不反应,但可与稀HNO3生成NO气体和Cu(NO3)2,由于H2SO4能提供H+,与Cu(NO3)2中电离出的NO3-还可以形成HNO3溶液,继续溶解铜。所以本题应以离子方程式求解:3Cu + 8H+ +2NO3-? 3Cu2+ + 2NO↑+4H2O,NO气体为0.2mol,根据N守恒,知HNO3的物质的量为0.2mol,反应中共耗H+为0.8mol,所以,由H2SO4提供的H+的物质的量为0.6mol,H2SO4即为0.3mol。
3Cu2+ + 2NO↑+4H2O,NO气体为0.2mol,根据N守恒,知HNO3的物质的量为0.2mol,反应中共耗H+为0.8mol,所以,由H2SO4提供的H+的物质的量为0.6mol,H2SO4即为0.3mol。
本题难度:一般
4、选择题 学生甲和学生乙完成了下列实验,其中实验现象完全相同的是(?)
?
| 学生甲
| 学生乙
|
A
| 向NaHCO3溶液中逐滴加入盐酸
| 向盐酸中逐滴加入NaHCO3溶液
|
B
| 向AlCl3溶液中滴加NaOH溶液
| 向NaOH溶液中滴加入AlCl3溶液
|
C
| 向FeCl2溶液中滴加KSCN溶液,再通入Cl2
| 向FeCl2溶液中通入Cl2,再滴加KSCN溶液
|
D
| 向BaCl2溶液中通入SO2
| 向BaCl2溶液中通入SO3
|
?
参考答案:A
本题解析:A、向NaHCO3溶液中逐滴加入盐酸现象为有气体生成,向盐酸中逐滴加入NaHCO3溶液现象为有气体生成,现象完全相同,正确;B、向AlCl3溶液中滴加NaOH溶液现象为先生成白色沉淀后消失,向NaOH溶液中滴加入AlCl3溶液,现象为一开始白色沉淀即现即失,最后生成白色沉淀,现象不同,错误;C、向FeCl2溶液中滴加KSCN溶液,溶液颜色无变化,再通入Cl2溶液变血红色;向FeCl2溶液中通入Cl2,溶液由浅绿色变为黄色,再滴加KSCN溶液,溶液变为血红色,现象不同,错误;D、向BaCl2溶液中通入SO2,无现象,向BaCl2溶液中通入SO3生成白色沉淀,现象不同,错误。
本题难度:一般
5、选择题 下列各组实验过程中,现象不是先出现沉淀后沉淀又溶解的是
A.在澄清石灰水中不断地通入CO2
B.在FeSO4溶液中不断地滴加NaOH溶液
C.在AlCl3溶液中不断地滴加NaOH溶液
D.在Fe(OH)3胶体中不断地滴加稀H2SO4溶液
参考答案:B
本题解析:A、先生成CaCO3,后生成Ca(HCO3)2,澄清石灰水先变浑浊后变澄清,错误;B、先生成Fe(OH)2,后生成Fe(OH)3,溶液中先生成白色沉淀,后变为灰绿色沉淀,最后变为红褐色沉淀,正确;C、先生成Al(OH)3,后生成NaAlO2,错误;D、氢氧化铁胶体遇电解质溶液先变为Fe(OH)3沉淀,再与酸中和变为硫酸铁溶液,错误。
本题难度:一般