微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、简答题 A、B、C、D四种物质都含有一种共同的元素,A是常见的金属,C的溶液呈现黄色,A、B、C、D之间有如图所示转化关系.
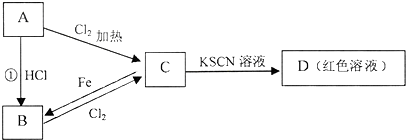
试回答下列问题:
(1)A是______,C是______.
(2)C的溶液与NaOH溶液混合后产生的现象是______.
(3)反应①的反应类型是______.
(4)从A、B、C三种物质中任选一种,从它们所含共同元素的价态上预测所选物质具有氧化性或还原性,并设计实验验证.
预测性质______;
主要操作______;
可能的现象______.
参考答案:由C生成D的反应现象可知C为FeCl3,A是常见的金属,应为Fe,则B为FeCl2,
(1)由以上分析可知A为Fe,C为FeCl3,故答案为:Fe;FeCl3;
(2)FeCl3与NaOH反应生成Fe(OH)3,为红褐色沉淀,故答案为:产生红褐色沉淀;
(3)反应为Fe+2HCl=FeCl2+H2↑,为置换反应,故答案为:置换;
(4)根据化合价中Fe元素为+3价,为最高价态,具有氧化性,可加成Fe,发生2FeCl3+Fe=3FeCl2,溶液颜色由黄色溶液逐渐变成浅绿色,
故答案为:选取C物质,它具有氧化性;取少量黄色的C的溶液置于试管中,向其中加入几枚无锈铁钉,振荡;黄色溶液逐渐变成浅绿色.
本题解析:
本题难度:一般
2、填空题 (8分)如图所示,甲、乙、丙是三种常见单质,X、Y、Z是常见化合物,它们之间有如下转化关系:

⑴若甲是短周期金属单质,乙、丙是短周期非金属单质,X、Y、Z中只有一种是离子晶体,
试推断:
①X的电子式是______________________________。
②X与甲反应的化学方程式____________________________________。
⑵若甲是气体单质,丙通常是液体,Y和Z具有相同的阳离子,X与Z含有相同的阴离子,试推断:
①写出Z的化学式_______________________。
②写出X与足量的甲在溶液中完全反应的离子方程式:________________________?_ 。
参考答案:⑴①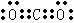 (2分)?②2Mg+CO2==2MgO+C(2分)
(2分)?②2Mg+CO2==2MgO+C(2分)
⑵①FeBr3(2分)?②3Cl2+2Fe2++4Br-==2Fe3++2Br2+6Cl-(2分)
本题解析:由框图可知反应甲+X→丙+Y属于置换反应。
(1)若甲为短周期金属,乙、丙是非金属,在常见金属能置换非金属的反应中只有镁和二氧化碳符合,故甲是镁,X是二氧化碳,丙是碳、Y是MgO。碳和二氧化碳反应生成CO,Z是CO。碳不完全燃烧生成CO,乙是氧气。
(2)在常见的单质液体中只有单质溴(金属汞不常见,很少涉及到),即丙是单质溴。Y和Z具有相同的阳离子,根据转化关系可知X中也含有该元素,故该元素是变价的金属元素,常见的变价金属是铁,乙是单质铁,因此Z是FeBr3,则X是FeBr2。能把FeBr2氧化生成FeBr3和单质溴的单质气体应氯气,即甲是氯气。
本题难度:一般
3、简答题 A-J是中学化学中常见的几种物质,它们之间的转化关系如图所示.已知常温下A为固体单质,B为淡黄色粉末,C、F、I为气态单质,E在常温下为液体,且E可由C、F化合生成,J可作禽流感、SARS等病毒的杀菌消毒剂.
(1)写出E的电子式:______.
(2)写出反应⑦的离子方程式:______.
(3)向AlCl3溶液中加入少量固体B,写出反应的化学方程式:______.
(4)以Pt为电极电解滴加有少量酚酞的H饱和溶液,则阳极的电极反应式为:______.
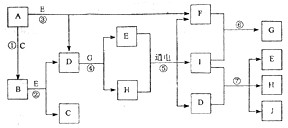
参考答案:B为淡黄色粉末,应为Na2O2,则A为Na,C为O2,E在常温下为液体,应为H2O,则D应为NaOH,F为H2,J可作禽流感、SARS等病毒的杀菌消毒剂,应为NaClO,为I和NaOH的反应产物,则气态单质I为Cl2,H为NaCl,G应为HCl,则
(1)E为H2O,为共价化合物,电子式为
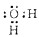
,故答案为:
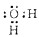
;
(2)反应⑦为Cl2和NaOH溶液的反应,反应的离子方程式为Cl2+2OH-=Cl-+ClO-+H2O,故答案为:Cl2+2OH-=Cl-+ClO-+H2O;
(3)向AlCl3溶液中加入少量固体Na2O2,反应原理是过氧化钠与水反应:2Na2O2+2H2O=4NaOH+O2↑,
进而发生:AlCl3+3NaOH=Al(OH)3↓+3NaCl,反应的总方程式为可写为4AlCl3+6Na2O2+6H2O=4Al(OH)3↓+12NaCl+3O2↑,
故答案为:4AlCl3+6Na2O2+6H2O=4Al(OH)3↓+12NaCl+3O2↑;
(4)以Pt为电极电解滴加有少量酚酞的NaCl饱和溶液,阳极发生氧化反应,氯离子失去电子生成氯气,电极反应式为
2Cl--2e-=Cl2,故答案为:2Cl--2e-=Cl2.
本题解析:
本题难度:一般
4、填空题 (8分) 在室温下,单质A、B、C分别为固体、黄绿色气体、无色气体,在合适反应条件下,它们可以按下列框图进行反应。又知E溶液是无色溶液。请回答:
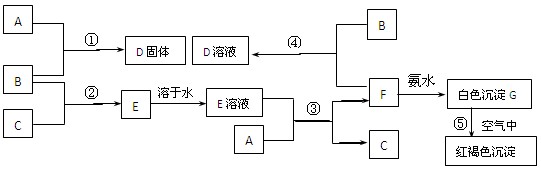
(1)? (用化学式填空)
A是______________B是________________
(2)反应①的化学方程式为___________________________________________
反应③的离子方程式为___________________________________________
反应⑤的化学方程式为___________________________________________________
参考答案:(1) A:Fe? B:Cl2? (2)?① 2Fe + 3Cl2 ="=" 2FeCl3?③ Fe +2H+ ="=" Fe2+? + H2↑
⑤ 4Fe(OH)2 + O2 + 4H2O ="=" 4Fe(OH)3
本题解析:本题是无机框图题,根据是寻找突破点。B是黄绿色气体,则B是氯气。白色沉淀G能在空气中转化为红褐色沉淀,所以G是氢氧化亚铁。因此单质A是铁,又因为C是无色气体,所以C是氢气,D是氯化亚铁,E是氯化氢,F是氯化亚铁。
本题难度:一般
5、简答题 现有中学常见金属单质A、B、C、I和气体甲、乙、丙及物质D、E、F、G、H.它们之间能发生下列反应(图中有些反应的产物和反应条件没有全部标出)
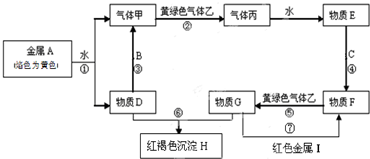
请根据以上信息回答下列问题:
(1)物质E的名称为______、H的化学式为______.
(2)写出过量C与乙反应的化学方程式:______.
写出反应⑦的离子方程式:______.
(3)实验室检验物质F中阳离子的方法及现象是:______.
(4)实验室中将物质F与物质D混合,得到物质J,J转化为H的现象是:______.
参考答案:金属单质A的焰色反应为黄色,则A是Na,Na和水反应生成NaOH和H2,所以甲是H2,D是NaOH,NaOH和金属单质B反应生成氢气,则B是Al,黄绿色气体乙是Cl2,氢气在氯气中燃烧生成丙,则丙是HCl,E是盐酸,H是Fe(OH)3,盐酸和金属单质C反应生成F,F被氯气氧化生成G,G和NaOH反应生成Fe(OH)3,则G是FeCl3,F是FeCl2,C是Fe,红色金属单质I为Cu,
(1)通过以上分析知,E的名称是盐酸,H的化学式为Fe(OH)3,故答案为:盐酸;Fe(OH)3;
(2)C是Fe,乙是Cl2,Fe在氯气中燃烧生成氯化铁,反应方程式为:2Fe+3Cl2△.2FeCl3,氯化铁和铜反应生成氯化亚铁和氯化铜,离子方程式为:2Fe 3++Cu=2Fe2++Cu 2+,
故答案为:2Fe+3Cl2△.2FeCl3;2Fe 3++Cu=2Fe2++Cu 2+;
(3)F中阳离子是Fe2+,亚铁离子能被氯水氧化生成铁离子,铁离子和无色硫氰化钾溶液反应生成络合物而使溶液呈血红色,则亚铁离子的检验方法为:向F的溶液中滴入KSCN溶液,溶液无明显现象,再滴入氯水溶液变为血红色,
故答案为:向F的溶液中滴入KSCN溶液,溶液无明显现象,再滴入氯水溶液变为血红色;
(4)FeCl2和NaOH反应生成Fe(OH)2白色沉淀,Fe(OH)2不稳定易被氧化生成红褐色Fe(OH)3,所以看到的现象是:白色沉淀迅速转化为灰绿色,最终变为红褐色,
故答案为:白色沉淀迅速转化为灰绿色,最终变为红褐色.
本题解析:
本题难度:简单