微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
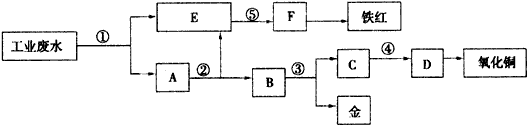
1、推断题 某厂的酸性工业废水中含有一定量的Fe3+、Cu2+、Au3+等离子。有人设计了图中的工艺流程,利用常用的酸、碱和工业生产中的废铁屑从废水中回收金,并生产一定量的铁红和氧化铜。
填写下面空白:
(1)请写出图中下列标号处需加入的相应物质:②_______ 、④________、⑤________。
(2)写出①处发生反应的离子方程式:_______________、______________、______________、__________________;写出③处发生反应的化学方程式:____________________。
(3)分别写出铁红和氧化铜在工业上的一种主要用途:铁红_______;氧化铜________。
参考答案:(1)②稀硫酸或稀盐酸;④氢氧化钠;⑤氢氧化钠
(2)①Fe+2H+=Fe2++H2↑;2Fe3++Fe=3Fe2+;Cu2++Fe=Cu+Fe2+;2Au3++3Fe=2Au+3Fe2+
③3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O
(3)用作红色涂料;用作制造铜盐的原料
本题解析:
本题难度:一般
2、简答题 A、B、C、D为同一周期的四种元素,原子序数依次增大,已知0.2摩A与酸充分反应时,在标况下可生成2.24升氢气;B的氧化物既可溶于强酸又可溶于强碱溶液;C、D阴离子的电子层结构与氩原子相同,C的气态氢化物与C的低价氧化物反应,又可得到C的单质.试回答:
(1)A、B、C、D的元素符号分别为______、______、______、______.
(2)用电子式表示A与C形成化合物的过程:______.
(3)写出B的氧化物与A的氢氧化物反应的离子方程式:______.
(4)写出实验室制备D的单质的化学反应方程式:______.
参考答案:A、B、C、D为同一周期的四种元素,原子序数依次增大,B的氧化物既可溶于强酸又可溶于强碱溶液,则B为铝元素;0.2摩A与酸充分反应时,在标况下可生成2.24升氢气,A为金属,氢气的物质的量为0.1mol,令A的化合价为x,根据电子转移守恒,0.2x=0.1mol×2,解得x=1,所以A处于ⅠA族,故A为钠元素;C、D阴离子的电子层结构与氩原子相同,原子序数C<D,故C为硫元素,D为氯元素,硫化氢与二氧化硫反应生成硫单质,符合题意.
故A为钠元素,B为铝元素;C为硫元素,D为氯元素.
(1)由上述分析可知,A为Na;B为Al;C为S;D为Cl.
故答案为:Na、Al、S、Cl.
(2)A为钠元素,C为硫元素,A与C形成化合物为Na2S,用电子式表示Na2S形成化合物的过程为
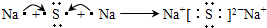
.
故答案为:
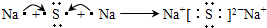
.
(3)B的氧化物为Al2O3,A的氢氧化物NaOH,氧化铝与氢氧化钠反应生成偏铝酸钠与氢气,二者反应的离子方程式为Al2O3+2OH-=AlO-+H2O.
故答案为:Al2O3+2OH-=AlO-+H2O.
(4)D为氯元素,单质为氯气,实验室制备氯气的化学反应方程式MnO2+4HCl(浓)??△?.??MnCl2+Cl2↑+H2O.
故答案为:MnO2+4HCl(浓)??△?.??MnCl2+Cl2↑+H2O.
本题解析:
本题难度:一般
3、填空题 下列实验流程图中,X为第三周期两种重要单质的氧化物的混合物.反应②、④是工业上的重要反应,部分物质及反应条件没有列出.
请回答下列问题:
(1)写出A、E、B的化学式:
A______,E______,B______.
(2)写出C溶液转化为C固体的过程中,HCl气流的作用:______.
(3)写出①、③、④反应的化学方程式,(若是离子反应写离子方程式)
①______;
③______;
④______.
(4)将SO2气体分别通入下列溶液写出对应的实验现象
①BaCl2溶液______;
②Ba(NO3)2溶液______;
⑨FeCl3溶液______.
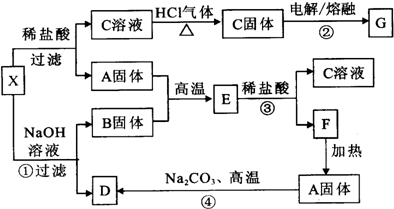
参考答案:X中两种氧化物混合物中,A能与NaOH溶液反应但不能与盐酸反应,应为SiO2,可知D为Na2SiO3,B固体可与盐酸但不能与NaOH溶液反应,生产C固体可用电解法冶炼金属,应为MgCl2,可知B为MgO,G为Mg,E为MgSiO3,F为H2SiO3,
(1)由上述分析可知,A为SiO2,E为MgSiO3,B为MgO,故答案为:SiO2;MgSiO3;MgO;
(2)因镁离子水解,则C溶液转化为C固体的过程中,HCl气流的作用抑制氯化镁水解,故答案为:抑制氯化镁水解;
(3)①的离子反应为SiO2+2OH-=SiO32-+H2O,故答案为:SiO2+2OH-=SiO32-+H2O;
③的离子反应为MgSiO3+2H+=H2SiO3↓+Mg2+,故答案为:MgSiO3+2H+=H2SiO3↓+Mg2+;
④的化学反应为SiO2+Na2CO3高温.Na2SiO3+CO2↑,故答案为:SiO2+Na2CO3高温.Na2SiO3+CO2↑;
(4)①因盐酸的酸性大于亚硫酸的酸性,则二者不反应,现象为无明显现象,故答案为:无明显现象;
②二者发生氧化还原反应生成硫酸钡沉淀和NO,则观察到产生白色沉淀,有无色气体产生,该气体遇空气变为红棕色,
故答案为:产生白色沉淀,有无色气体产生,该气体遇空气变为红棕色;
③二者发生氧化还原反应生成亚铁离子,则观察到溶液由棕黄色变为浅绿色,故答案为:溶液由棕黄色变为浅绿色.
本题解析:
本题难度:一般
4、选择题 由短周期元素组成的中学常见无机物A、B、C、D、E、X存在如下图转化关系(部分生成物和反应条件略去)
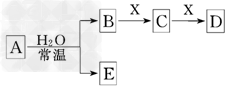
下列推断不正确的是
[? ]
A.若X是Na2CO3,C为含极性键的非极性分子,则A一定是氯气,且D和E不反应
B.若A是单质,B和D的反应是OH-+HCO3-===H2O+CO32-,则E一定能还原Fe2O3
C.若D为CO,C能和E反应,则A一定为Na2O2,其电子式为
D.若D为白色沉淀,与A的摩尔质量相等,则X一定是铝盐
参考答案:A
本题解析:
本题难度:一般
5、推断题 下列物质均是中学化学常见物质,转化关系图中C、E均是常见金属单质,D?是红棕色金属氧化物粉末。
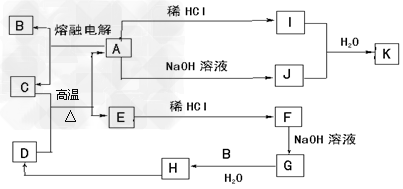
请回答下列问题
(1)写出下列物质的化学式?A______B______C_______?
(2)写出I+J?→?K的离子方程式__________________
(3)写出G→H的化学反应方程式_______________________
参考答案:(1)Al2O3;O2;Al
(2)Al3+?+?3AlO2-?+?6H2O?==?4Al(OH)3↓
(3)4Fe(OH)2?+?O2?+?2H2O?==?4Fe(OH)3
本题解析:
本题难度:一般