微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、简答题 工业上生产硫酸时,将SO2氧化为SO3是关键一步.
(1)某温度下,2?SO2(g)+O2(g)?2SO3(g);△H=-196kJ?mol-1.开始时在10L的密闭容器中加入4.0mol?SO2(g)和5.0mol O2(g),当反应达到平衡时共放出热量196kJ,该温度下平衡常数K=?.
(2)一定条件下,向一带活塞的密闭容器中充入2mol SO2和1mol O2,发生下列反应:2SO2(g)+O2(g)?2SO3(g)达到平衡后改变下述条件,SO2、O2、SO3气体平衡浓度都比原来增大的是?.
A.保持温度和容器体积不变,充入2mol?SO3
B.保持温度和容器体积不变,充入2mol?N2
C.保持温度和容器体积不变,充入0.5mol?SO2和0.25mol?O2
D.保持温度和容器内压强不变,充入1mol?SO3
E.升高温度?
F.移动活塞压缩气体
(3)某人设想以右上图所示装置用电化学原理生产硫酸,写出通入SO2的电极的电极反应式:?.
(4)在0.1mol?L-1的(NH4)2SO4溶液中,离子浓度由大到小的顺序是?.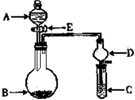
参考答案:(1)某温度下,SO2(g)+12O2(g)?SO3(g);△H=-98kJ?mol-1.开始时在10L的密闭容器中加入4.0mol SO2(g)和5.0mol O2(g),当反应达到平衡时共放出热量196kJ,消耗二氧化硫物质的量为:19698=2mol,平衡三段式得到
? 2?SO2(g)+O2(g)?2SO3(g);△H=-196kJ?mol-1.
起始量(mol)? 4? 5? 0?
变化量(mol)? 2? 1? 2? 196KJ
平衡量(mol)? 2? 4? 2
该温度下平衡常数K=c2(SO3)c2(SO2)c(O2)=(2mol10L)2(2mol10L)2×4mol10L=2.5L/mol
故答案为:2.5L/mol
(2)A.保持温度和容器体积不变,充入2mol SO3,平衡向逆反应分析移动,则SO2、O2、SO3气体平衡浓度都比原来增大,故A正确;
B.保持温度和容器体积不变,充入2mol N2,对平衡移动没有影响,各物质的浓度不变,故B错误;
C.保持温度和容器体积不变,充入0.5mol SO2和0.25mol O2,平衡向正反应方向移动,则SO2、O2、SO3气体平衡浓度都比原来增大,故C正确;
D.保持温度和容器内压强不变,充入1mol SO3,处于等效平衡状态,浓度不变,故D错误;
E.升高温度,平衡向逆反应分析移动,SO3的浓度减小,故E错误;
F.移动活塞压缩气体,体积减小,各物质的浓度都增大,故F正确.
故答案为:A、C、F;
(3)原电池负极发生氧化反应,SO2被氧化生成SO42-,负极电极反应式为SO2+2H2O-2e-=SO42-+4H+,
故答案为:SO2+2H2O-2e-=SO42-+4H+;
(4)在0.1mol?L-1的(NH4)2SO4溶液中,硫酸铵溶液中铵根离子水解溶液呈酸性,离子浓度由大到小的顺序是c(NH4+)>c (SO42-)>c (H+)>c (OH-);
故答案为:c(NH4+)>c?(SO42-)>c?(H+)>c?(OH-);
本题解析:
本题难度:一般
2、选择题 下列事实能用同一原理解释的是
[? ]
A.?SO2和Cl2都能用于漂白?
B. 苯酚、乙烯都能跟溴水反应
C. 苏打、小苏打水溶液的pH都大于7?
D.?I2,?NH4Cl晶体受热都逐渐消失
参考答案:C
本题解析:
本题难度:一般
3、选择题 下列事实不能用勒夏特列原理解释的是
[? ]
A.开启啤酒瓶后,瓶中立刻泛起大量泡沫
B.由H2、I2蒸气、HI组成的平衡体系加压后颜色变深
C.向氯水中加CaCO3后,溶液漂白性增强
D.在含有[Fe(SCN)]2+的红色溶液中加铁粉,振荡静置,溶液颜色变浅或褪去
参考答案:B
本题解析:
本题难度:一般
4、选择题 一定条件下,将3molA和1molB两种气体混合于固定容积为2L的密闭容器中,发生如下反应:3A(g)+B(g)?xC(g)+2D(s).2min末该反应达到平衡,生成0.8molD,并测得C的浓度为0.2mol/L.下列判断正确的是( ? )
A.该条件下此反应的化学平衡常数约为0.91(L/mol)3
B.A的平均反应速率为0.3mol/(L?s)
C.B的转化率为60%
D.若混合气体的密度不再改变时,该反应不一定达到平衡状态
参考答案:A
本题解析:
本题难度:简单
5、选择题 可逆反应2SO2(气)+O2(气)?2SO3(气)在向逆反应进行时,正反应速率和逆反应速率( )
A.大于
B.小于
C.等于
D.不能确定
参考答案:B
本题解析:
本题难度:简单