微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 在体积相同的A和B两个带活塞的玻璃容器中,如分别注入1/4容积颜色相同的NO2(存在2NO2?N2O4平衡)和Br2蒸气,然后将活塞同时向外拉出到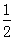 处(快速)过一会儿可以看出( )
处(快速)过一会儿可以看出( )
①A中颜色比B中浅;②A中颜色比B中深;
③A和B颜色深浅相同;④A和B颜色都比开始时浅.
A.①②
B.②③
C.②④
D.③④
参考答案:C
本题解析:
本题难度:简单
2、选择题 一定温度下的可逆反应:A(s)+2B(g)2C(g)+D(g)△H<0.现将1molA和2molB加入甲容器中,将4molC和2molD加入乙容器中,此时控制活塞P,使乙的容积为甲的2倍,t1时两容器内均达到平衡状态(如图1所示,隔板K不能移动).下列说法正确的是( )

A.保持温度和活塞位置不变,在甲中再加入1molA和2molB,达到新的平衡后,甲中C的浓度是乙中C的浓度的2倍
B.保持活塞位置不变,升高温度,达到新的平衡后,甲中B的体积分数增大,乙中B的体积分数减小
C.保持温度不变,移动活塞P,使乙的容积和甲相等,达到新的平衡后,乙中C的体积分数是甲中C的体积分数的2倍
D.保持温度和乙中的压强不变,t2时分别向甲、乙中加入等质量的氦气后,甲、乙中反应速率变化情况分别如图2和图3所示(t1前的反应速率变化已省略)
参考答案:D
本题解析:
本题难度:一般
3、填空题 某化学反应2A(g)B(g)+D(g)在四种不同条件下进行,反应器均为相同恒容密闭容器,B、D起始浓度为0.反应物A的浓度(mol?L-1间(min)的变化情况如下表:
实验
序号 | | 0 | 10 | 20 | 30 | 40 | 50 | 60
1
800℃
1.0
0.80
0.67
0.57
0.50
0.50
0.50
2
800℃
C2
0.60
0.50
0.50
0.50
0.50
0.50
3
800℃
C3
0.92
0.75
0.63
0.60
0.60
0.60
4
820℃
1.0
0.40
0.25
0.20
0.20
0.20
0.20
|
根据上述数据,完成下列填空:
(1)在实验1中,反应在10~20分钟内用A表示的平均速率为______.
(2)在实验2中,A的初始浓度C2=______mol?L-1,反应经20分钟就达到平衡,可推测实验2中还隐含的条件是______.
(3)设实验3的反应速率为υ3,实验1的反应速率为υ1,则υ3______υ1(填>、=、<),且C3=______mol?L-1.
(4)由上述实验,可推测该反应是______反应(选填“吸热”或“放热”).理由是:______.
(5)1~4组实验中,A的平衡转化率最大的是第______组.
(6)在实验2中,50min后,若将容器体积增大1倍,则达平衡时B的浓度为______mol?L-1;该反应的平衡常数K______(填“不变”或“增大”或“减小”).
参考答案:(1)反应在10~20分钟内用A表示的平均速率为v=△C△t=(0.80-0.67)mol/L(20-10)min=0.013mol/(L?min),
故答案为:0.013mol/(L?min);
(2)根据实验1、2数据分析,温度相同,达平衡后A的物质的量浓度相同,且B、D起始浓度为0,所以两组实验中A的起始浓度相同为1.0mol?L-1 ;温度相同,达平衡后A的物质的量浓度相同,但达平衡时2组的时间较短,所以只能是加入催化剂;
故答案为:1.0;催化剂;
(3)实验1、3比较,温度相同,10min-20min时,实验3的浓度减少量都大于实验1的,所以实验3的反应速率大于实验1的,即v3>v1;
实验1可知40min时反应达到平衡
2A(g)?B(g)+D(g)
起始(mol?L-1) 1.00 0
反应(mol?L-1) 0.50 0.25 0.25
平衡(mol?L-1) 0.50 0.25 0.25
该温度下平衡常数K=C(D)C(B)C2(A)=0.25×0.250.502=14;
实验3的温度与实验1的温度相同,温度不变,平衡常数不变;
2A(g)?B(g)+D(g)
起始(mol?L-1) C3 0 0
反应(mol?L-1) 0.6 0.30 0.30
平衡(mol?L-1) C3-0.60 0.30 0.30
该温度下平衡常数K=C(D)C(B)C2(A)=0.30×0.30(C3-0.60)2=1;
解得:C3=1.2;
故答案为:>;1.2;
(4)实验4与实验1比,温度升高,达平衡时A的平衡浓度减小;温度升高,化学平衡向吸热方向移动,所以正反应是吸热反应;
故答案为:吸热;比较实验4与实验1,可看出升高温度,A的平衡浓度减小,说明升高温度平衡向正反应方向移动,故正反应是吸热反应.
(5)2A(g)?B(g)+D(g)
起始(mo l?L-1)C2 0 0
反应(mol?L-1) 0.50 0.25 0.25
平衡(mol?L-1) C2-0.50 0.25 0.25
该温度下平衡常数K=C(D)C(B)C2(A)=0.25×0.25(C2-0.50)2=14;
解得:C2=1.0;
1~4组实验中,第4组A的平衡转化率最大为1.0-0.201.0×100%=80%,故答案为:4;
(6)由(5)知,在实验2中,平衡时B的浓度为0.25mol/L,50min后,若将容器体积增大1倍,平衡不移动,浓度为原来的一半,即0.125mol/L;由于温度不变,所以该反应的平衡常数不变,故答案为:0.125mol/L;不变.
本题解析:
本题难度:简单
4、选择题 下列事实不能用勒夏特列原理解释的是
[? ]
A.工业生产硫酸的过程中使用过量的氧气,以提高二氧化硫的转化率
B.合成氨工厂通常采用20MPa~50MPa压强,以提高原料的利用率
C.在实验室里,可用碳酸钙粉末和稀硫酸制得二氧化碳气体
D.实验室用排饱和食盐水的方法收集氯气
参考答案:C
本题解析:
本题难度:一般
5、选择题 下列反应能用勒夏特列原理解释的是
[? ]
A.由SO2和O2反应制SO3需使用催化剂
B.燃烧粉碎的黄铁矿矿石有利于SO2的生成
C.硫酸生产中用98.3%的硫酸吸收SO3,而不用H2O或稀硫酸吸收SO3
D.用N2和H2合成氨需采用高压
参考答案:D
本题解析:
本题难度:一般