微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列说法不正确的是
A.元素周期表中,除第一和第七周期外,第n周期所含非金属元素(包括稀有气体元素)的种数均为(8-n)
B.SiCl4、PCl3分子中各原子最外层均达到8电子稳定结构
C.M层电子数为奇数的主族元素所在族的序数与该元素原子的M层电子数不一定相等
D.由ⅠA族和ⅥA族短周期元素形成的原子个数比为1∶1,电子总数为38的化合物,是含有共价键的离子型化合物
参考答案:C
本题解析:M层电子数为奇数的主族元素所在族的序数与该元素原子的M层电子数一定是相等的,选项C不正确,其余都是正确的,其中D中化合物是过氧化钠,答案选C。
本题难度:一般
2、选择题 已知某短周期元素原子的第三电子层上排布有5个电子,则该元素在周期表中的位置是
A.第二周期ⅣA族
B.第二周期ⅤA族
C.第三周期ⅣA族
D.第三周期ⅤA族
参考答案:D
本题解析:第三电子层上排布有5个电子,则根据核外电子的排布规律可知,该元素在周期表中的位置是第三周期ⅤA族,答案选D。
本题难度:简单
3、填空题 A、B、C属于周期表前4周期的元素,它们的原子序数依次增大。A、B属于同一周期,A、C是生活中常见的金属元素。C的原子序数是A的2倍,B的单质常温下为黄色粉末。
(1)C在周期表中位于?周期?族。
(2)在加热条件下B单质与C单质反应的化学方程式是?。
(3)A的氧化物是某矿物的主要成分,由该矿物提取A元素的第一步是用NaOH溶液处理矿物,使A元素变为可溶性盐,该反应的离子方程式是?。
(4)B与C形成的化合物CB2,在有水存在的条件下用氧气氧化该化合物,得到强酸性溶液,低温下从该强酸性溶液中还可结晶出浅绿色的C的低价盐,该氧化还原反应的化学方程式是?。
参考答案:
(1)四(1分);Ⅷ
(2)S+Fe FeS
FeS
(3)Al2O3+2OH-=2AlO2-+H2O
(4)2FeS2+7O2+2H2O=2H2SO4+2FeSO4
本题解析:
本题考查元素周期表中元素的推断。关键在于找到熟悉周期表的结构,同时找一题眼进行突破,常温下是黄色粉末的单质只有S,故B是S。生活中常见的金属元素是铁和铝,原子序数分别是26、13,符合题意(C的原子序数是A的2倍),故A是铝,C是铁。
本题难度:一般
4、判断题 判断下列说法中是否正确:(请在空格内打“√”或“×”)
①质子数相同的粒子一定属于同种元素;?(?)
②电子数相同的粒子不一定是同一种元素;?(?)
③一种元素只能有一种质量数;?(?)
④某种元素的相对原子质量取整数,就是其质量数;?(?)
⑤质子数相同,电子数也相同的粒子,不可能是一种分子和一种离子; (?)
⑥同位素的性质几乎完全相同?(?)
参考答案:× √ × × √ ×
本题解析:质子数相同的粒子可能是原子或原子团,不一定是同一种元素。因为质子数等于电子数,所以电子数相同的粒子也不一定是同一种元素。大部分元素都有同位素,所以质量数不止一种。忽略电子的质量,将核内所有质子和中子的相对真理取近似整数相加,所得数值叫质量数。对于中性微粒质子数等于电子数,当质子数和电子数不易相等时,则一定是离子。所以质子数相同,电子数也相同的粒子,不可能是一种分子和一种离子。同位素的化学性质是几乎完全相同,而不是所有的性质。
本题难度:一般
5、填空题 以下列出的是一些原子的2p能级和3d能级中电子排布的情况。试判断,哪些违反了泡利不相容原理,哪些违反了洪特规则。
(1)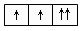 ?(2)
?(2) ?(3)
?(3) 
(4) (5)
(5)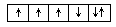 (6)
(6)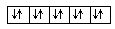
违反泡利不相容原理的有?,违反洪特规则的有?。
参考答案:(1);(2)、(4)、(5)(各1分)
本题解析:在一个原子轨道里,最多只能容纳2个电子,而且它们的自旋状 态相反,称为泡利不相容原理,所以违反泡利不相容原理的有(1);当电子排布在同一个能级的不同轨道时,基态原子中的电子总是单独优先占据一个轨道,而且自旋状态相同,称为洪特规则,所以违反洪特规则的有(2)、(4)、(5)。
点评:该题是基础性试题的考查,也是高考中的常见考点,难度不大。该题的关键是明确泡利不相容原理和洪特规则的含义,然后结合题意灵活运用即可。
本题难度:简单