| 高考省级导航 | |
|
|
| 高考省级导航 | |
|
|
|
高考化学必考知识点《盐类水解的原理》高频考点巩固(2017年模拟版)(四)
参考答案:B 本题解析:A.该反应为弱酸的电离方程式,故A错误;B.铵根离子和水反应生成弱电解质一水合氨和氢离子,为水解反应,故B正确;C.碳酸根离子分两步水解,第一步水解方程式为CO32-+H2O?HCO3-+OH-,故C错误;D.氢溴酸为强电解质,所以溴离子不是弱根离子,在水溶液里溴离子不水解,故D错误; 本题难度:一般 2、填空题 (12分)完成下列各题: 参考答案: 本题解析: 本题难度:困难 3、选择题 下列所述事实与化学(离子)方程式不相符的是 |
参考答案:A
本题解析:A、非金属性的比较可通过最高价含氧酸的酸性的强弱来比较,盐酸的酸性大于碳酸,但盐酸是Cl元素的非含氧酸,不能用来与碳酸的酸性作比较,来判断非金属性的强弱,错误;B、根据氧化剂的氧化性大于氧化产物的氧化性,在该反应中氧化剂是过氧化氢,氧化产物是铁离子,所以能说明氧化性H2O2 > Fe3+,正确;C、稀硫酸与氢氧化钠反应生成硫酸钠和水,可用H+(aq)+OH―(aq)==H2O(l)表示,所以稀硫酸与NaOH稀溶液反应生成1mol水,放出的热量为57.3 kJ,正确;D、醋酸根离子在水中发生水解反应,生成醋酸,可以说明醋酸是弱酸,正确,答案选A。
考点:考查对离子方程式的理解,非金属性、氧化性的比较
本题难度:一般
4、选择题 下列化合物中,既能发生消去反应生成烯烃,又能发生水解反应的是( ? )
A.CH3Cl
B.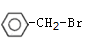
C.
D.
E.
?
?
?
参考答案:DE
本题解析:
本题难度:简单
5、填空题 已知某溶液中只存在OH-、H+、NH4+、Cl-,某同学推测其离子浓度大小顺序可能有如下四种关系①c(Cl-)>c(NH4+)>c(H+)>c(OH-) ②c(NH4+)>c(OH-)>c(Cl-)>c(H+)
③c(NH4+)>c(Cl-)>c(OH-)>c(H+) ④c(Cl-)>c(H+)>c(NH4+)>c(OH-)
填写下列空白:
(1)若溶液中只溶解一种溶质,则该溶质是 ,若四种离子的关系符合③,则溶质为 若四种离子的关系符合④,则溶质为 。
(2)将pH相同的NH4Cl溶液和HCl溶液稀释相同的倍数,则下面图象正确的是(填图象符号)________。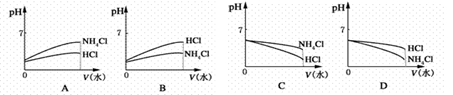
(3)若该溶液是由体积相等的稀盐酸和氨水混合而成,且恰好呈中性,则混合前c(HCl)________c(NH3・H2O)(填“大于”“小于”或“等于”)。
(4)在浓度均为0.1mol/L①CH3COONH4 ②NH4HSO4 ③NH4Cl ④(NH4)2SO4溶液中,NH4+浓度由大到小的顺序为 (填序号)
(5)已知:0.5 mol液态肼(N2H4)与足量的液态双氧水反应,生成氮气和水蒸气,放出256.65 kJ的热量.反应的热化学方程式为: 。
参考答案:(1)NH4Cl;NH4Cl、NH3・H2O;HCl、NH4Cl;(2)B(3)小于(4)④>②>③>①(5)N2H4(l)+2H2O2(l)=N2(g)+4H2O(g) △H=-513.3kJ・mol-1。
本题解析:(1)根据溶液中离子种类,此溶液中的溶质可能是NH4Cl,NH4Cl、NH3・H2O,HCl、NH4Cl,只有一种溶质只能是NH4Cl;③c(NH4+)>c(Cl-)>c(OH-)>c(H+),溶液显碱性,溶液中的溶质只能是NH4Cl、NH3・H2O,因为氨水的电离大于铵根的水解;④c(Cl-)>c(H+)>c(NH4+)>c(OH-),溶液显酸性,根据上述分析,溶液中的溶质只能是HCl、NH4Cl;(2)盐酸是强酸,NH4Cl溶液显酸性,是因为NH4+水解产生的,pH相同的NH4Cl溶液和HCl溶液稀释相同倍数,HCl变化大,NH4Cl变化小,B正确;(3)盐酸是强酸,氨水是弱碱,反应后溶液呈现中性,说明c(HCl)<c(NH3・H2O),填“小于”;(4)盐类水解的程度是微弱的,④中c(NH4+)最大,以③中NH4++H20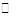 NH3・H2O+H+为研究对象,①相当于向③中加入CH3COO-,而CH3COO-水解呈现碱性,互相促进水解,因此①中c(NH4+)<③,②中的HSO4-是强酸跟,在水溶液中完全电离产生H+,②相当于向①中加入H+,抑制了NH4+的水解,②中c(NH4+)>③,因此c(NH4+)的大小顺序:④>②>③>①(5)N2H4(l)+2H2O2(l)=N2(g)+4H2O(g) ,0.5 molN2H4完全燃烧放出256.65 kJ的热量,消耗1mol时放出513.3 kJ的热量,N2H4(l)+2H2O2(l)=N2(g)+4H2O(g) △H=-513.3kJ・mol-1。
NH3・H2O+H+为研究对象,①相当于向③中加入CH3COO-,而CH3COO-水解呈现碱性,互相促进水解,因此①中c(NH4+)<③,②中的HSO4-是强酸跟,在水溶液中完全电离产生H+,②相当于向①中加入H+,抑制了NH4+的水解,②中c(NH4+)>③,因此c(NH4+)的大小顺序:④>②>③>①(5)N2H4(l)+2H2O2(l)=N2(g)+4H2O(g) ,0.5 molN2H4完全燃烧放出256.65 kJ的热量,消耗1mol时放出513.3 kJ的热量,N2H4(l)+2H2O2(l)=N2(g)+4H2O(g) △H=-513.3kJ・mol-1。
考点:考查离子浓度大小比较、弱电解质的稀释、影 响盐类水解的因素、热化学反应方程式的书写等相关知识。
本题难度:困难
|
||
| 【大 中 小】【打印】 【繁体】 【关闭】 【返回顶部】 | ||
| 下一篇:高中化学知识点总结《燃烧热》考.. | ||