微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列对氯气的性质叙述正确的是( )
A.将干燥的氯气通过干燥的红色纸条时,可以使纸条褪色
B.氯气无漂白性,但通入紫色石蕊试液中可以使之褪色
C.在通常情况下,氯气可以和任何金属反应
D.闻其气味时,可以小心将集气瓶直接放在鼻子下闻
参考答案:A、因干燥的氯气不具有漂白性,则将干燥的氯气通过干燥的红色纸条时,纸条不褪色,故A错误;
B、因氯气与水反应生成的次氯酸,次氯酸具有漂白性,则通入紫色石蕊试液中可以使之褪色,故B正确;
C、在通常情况下,氯气能与活泼金属、较活泼金属发生反应,与极不活泼金属不反应,故C错误;
D、闻氯气时,不能直接放在鼻子下闻,应用手在集气瓶口轻轻扇动来闻气体的气味,故D错误;
故选B.
本题解析:
本题难度:简单
2、计算题 已知Cl2在70℃的NaOH水溶液中,能同时发生两个自身氧化还原反 应,反应完全后测得溶液中NaClO与NaClO3的物质的量之比为4:1。现有49.7g Cl2,将其通入到足量70℃的NaOH水溶液中,反应完全后得到500mL溶液。
应,反应完全后测得溶液中NaClO与NaClO3的物质的量之比为4:1。现有49.7g Cl2,将其通入到足量70℃的NaOH水溶液中,反应完全后得到500mL溶液。
(1)写出Cl2在70℃的NaOH水溶液中符合上述条件的总反应方程式
(2)计算完全反应后生成物NaClO3的物质的量浓度
参考答案:
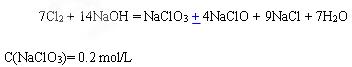
本题解析:略
本题难度:一般
3、简答题 (20分)某校化学实验兴趣小组为了探究在实验室制备Cl2的过程中有水蒸气和HCl挥发出来,同时证明Cl2的某些性质,甲同学设计了如图所示的实验装置(支撑用的铁架台省略),按要求回答问题:
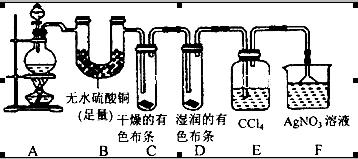
(1)下列方法中,可制得的正确组合是__________。
①MnO2和浓盐酸混合共热;?②MnO2、NaCl和浓硫酸混合共热:
③NaClO和浓盐酸混合;?④K2Cr2O7和浓盐酸混合:
⑤KClO3和浓盐酸混合共热;?⑥KMnO4和浓盐酸混合。
A.①②⑥B.②④⑥C.①④⑥? D.全部可以
(2)写出实验室制取Cl2的离子方程式____________。
(3)若用含有0.2 mol HCl的浓盐酸与足量的MnO2反应制得Cl2的体积(标况下)总是小于1.12L的原因是_________________________________________。
(4)①装置B的作用是__________________________________。
②装置C和D出现的不同现象说明的问题是________________________。
③装置E的作用是_____________________。
(5)乙同学认为甲同学的实验有缺陷,不能确像最终通入AgNO3溶液中的气体只有一种。为了确保实验结论的可靠性,证明最终通入AgNO3溶液中的气体只有一种,乙同学提出应该在装置__________与________之间(填装置字母序号)增加一个装置,增加装置里面的试剂可为____________。
A.湿润的淀粉KI试纸B.氢氧化钠溶液
C.湿润的红色布条? D.饱和的食盐水
参考答案:(20分)
(1)D(2分)
(2)4H++2Cl-+MnO2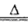 2H2O + Cl2↑+Mn2+;(3分)
2H2O + Cl2↑+Mn2+;(3分)
(3)随着反应的进行,盐酸浓度变稀将不再反应(3分,其他合理答案也给分)
(4)①证明有水蒸气产生,并吸收水蒸气,避免对后面探究氯气的性质实验产生干扰;(3分)
②氯气无漂白性,次氯酸有漂白性(3分)
③吸收氯气(2分)
(5)E,F;(2分) AC(2分)
本题解析:(1)制取氯气的方法由多种,但共同点有1个,都是浓盐酸作还原剂,所以合适的氧化剂与浓盐酸反应可以制取氯气,题目所给方法都可以,答案选D;
(2)实验室制取氯气采用MnO2和浓盐酸混合共热的方法,离子方程式为4H++2Cl-+MnO2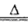 2H2O + Cl2↑+Mn2+;
2H2O + Cl2↑+Mn2+;
(3)二氧化锰与稀盐酸不反应,所以随着反应的进行,盐酸浓度变稀,反应停止,制得Cl2的体积(标况下)总是小于1.12L;
(4)①用无水硫酸铜来检验是否有水产生,若有,则固体颜色由白色变为蓝色,后面的实验要求氯气使干燥的,所以装置B同时还可以吸收水蒸气,避免对后面探究氯气的性质实验产生干扰;
②干燥的有色布条不褪色说明氯气不具有漂白性,湿润的有色布条褪色,说明氯气与水反应产生的次氯酸具有漂白性;
③氯气在水中的溶解度不大,但在有机溶剂中的溶解度较大,所以装置E的作用是吸收多余的氯气;
(5)装置E吸收氯气,但不能证明氯气是否被吸收干净,所以在E、F间应加一个装置,用来检验氯气是否除尽,从而判断通入AgNO3溶液中的气体是否只有一种;检验氯气是否除尽的试剂可以是湿润的淀粉KI试纸,若试纸变蓝,说明氯气未除尽;还可以是湿润的红色布条,若布条褪色,说明氯气未除尽,反之则除尽,答案选AC。
本题难度:一般
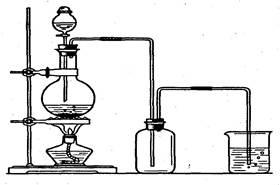
4、实验题 (10分)实验室制取并收集氯气的装置如右图:某同学进行实验时可能有如下操作:
 ?
?
(1)烧瓶中发生反应的化学方程式是:___________________________。
(2)制得的氯气可选用____________来干燥,烧杯中发生反应的离子方程式是_________________。
(3)在实验室里,常用加热食盐晶体和浓硫酸的混合物的方法来制取HCl,HCl是一种无色有刺激性气味的气体,密度比空气大,极易溶于水,它的水溶液叫氢氯酸,即盐酸。
①实验室制取HCl的发生装置可选用制__?___的发生装置(填O2、Cl2、CO2中的一种)。
②收集氯化氢气体时应采用__________法。
 ?
?
③实验室可用__________________________试纸放在瓶口检验HCl是否充满了集气瓶。
④上图哪些装置可作为多余氯化氢的吸收装置?______________________________。
参考答案:(共10分)(1)MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O(2分)
MnCl2+Cl2↑+2H2O(2分)
(2)浓硫酸(1分)? Cl2+2OH-=Cl-+ClO-+H2O(2分)
(3)①Cl2(1分)?②向上排空气 (1分)③湿润的蓝色石蕊试纸 (1分) ④AC(2分)
本题解析:考查氯气的制取与收集
(1)实验原理:MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O
(2)氯气一般用酸性干燥剂浓硫酸来干燥即可;氯气有毒,一般需要用碱液进行吸收: Cl2+2OH-=Cl-+ClO-+H2O
(3)①制取HCl的实验原理为:NaCl+H2SO4(浓)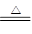 HCl↑+NaHSO4,属于固液加热装置,与制取氯气的装置相同;
HCl↑+NaHSO4,属于固液加热装置,与制取氯气的装置相同;
②HCl极易溶于水,不能用排水法收集;它的密度大于空气,故只能用向上排空气法来收集
③HCl为酸性气体,可采用湿润的蓝色石蕊试纸来检验
④由于HCl极易溶于水,直接导入水中易引起倒吸,故可采用AC装置
本题难度:一般
5、选择题 取少量无机盐溶液,对其中的离子进行检验。下列判断正确的是(? )
A.加入盐酸,产生白色沉淀,则试样中一定有Ag+
B.加入盐酸,产生能使澄清石灰水变浑浊的无色气体,则试样中一定有CO32-
C.加入NaOH溶液微热,产生能使湿润的红色石蕊试纸变蓝的气体,则试样中一定有NH4+
D.加入BaCl2溶液,产生白色沉淀,再加入稀硝酸,沉淀不溶解,则试样中一定有SO42-
参考答案:C
本题解析:向溶液中加入盐酸,产生白色沉淀,溶液中可能含有Ag+、SiO32-、AlO2- (盐酸少量)中的一种或几种离子;加入盐酸,产生能使澄清石灰水变浑浊的无色气体,试样中可能含有CO32-、HCO3-、SO32-、HSO3-中的一种或几种离子;C中产生的气体是氨气,则溶液中肯定含有NH4+;D中除了Ag+会产生干扰外,加稀硝酸酸化也会干扰,因为硝酸能将SO32- (HSO3-)氧化为SO42-。
本题难度:简单