微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 (共11分)工业废水中常含有一定量的Cr2O72-和CrO42-,它们会对人类及生态系统产生很大的伤害,必须进行处理。常用的处理方法有两种。
方法l:还原沉淀法
该法的工艺流程为:
其中第①步存在平衡:2CrO42-(黄色)+2H+ Cr2O72-(橙色)+H2O
Cr2O72-(橙色)+H2O
(1)若平衡体系的pH=2,则溶液显 色。
(2)能说明第①步反应达平衡状态的是 。
A.Cr2O2- 7和CrO2- 7的浓度相同 B.2v(Cr2O2- 7)=v(CrO2- 4) C.溶液的颜色不变
(3)第③步生成的Cr(OH)3在溶液中存在以下沉淀溶解平衡: Cr(OH)3(s)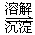 Cr3+(aq)+3OH-(aq)
Cr3+(aq)+3OH-(aq)
常温下,Cr(OH)3的溶度积Ksp=c(Cr3+)?c3(OH-)=10-32,要使c(Cr3+)降至10-5mol/L,溶液的pH应调至 。
方法2:电解法
该法用Fe做电极电解含Cr2O72-的酸性废水,随着电解进行,在阴极附近溶液pH升高,产生Cr(OH)3沉淀。
(4)用Fe做电极的原因为 。
(5)在阴极附近溶液pH升高的原因是(用电极反应式解释) 。溶液中同时生成的沉淀还有 。
参考答案:(共11分)(1)橙 (1分);(2)C(2分); (3)5(2分);
(4)阳极反应为Fe-2e-=Fe2+(2分);提供还原剂Fe2+(1分)
(5)2H+ +2e-=H2↑(2分);Fe(OH)3 (1分)
本题解析:(1)pH=2说明溶液显酸性,平衡向正反应方向移动,Cr2O72―的浓度会增大,所以溶液显橙色。
(2)在一定条件下的可逆反应里,当正反应速率和逆反应速率相等,反应物的浓度与生成物的浓度不再改变时,该可逆反应就到达化学平衡状态。平衡时浓度不再发生变化,但物质之间的浓度不一定相等或满足某种关系,因此选项A不正确;在任何情况下Cr2O72―和CrO42―的反应速率之比总是满足1:2,因此选项B也不正确;颜色的深浅与浓度有关系,溶液颜色不再改变,这说明Cr2O72―和CrO42―的浓度不再发生改变,因此可以说明反应已经达到化学平衡状态,C正确,答案选C。
(3)由溶度积常数的表达式Ksp=c(Cr3+)・c3(OH―)=10-32可知,当c(Cr3+)=10-5mol/L时,c(OH―)=10-9mol/L,所以pH=5。
(4)Cr2O72―要生成Cr(OH)3沉淀,必需有还原剂,而铁做电极时,在阳极上可以失去电子产生Fe2+,阳极方程式为Fe-2e-=Fe2+。
(5)在电解池中阳离子在阴极得到电子,在溶液中由于H+得电子得能力强于Fe2+的,因此阴极是H+放电,方程式为2H++2e-=H2↑。随着电解的进行,溶液中的H+浓度逐渐降低,水的电离被促进,OH-浓度逐渐升高。由于Fe2+被Cr2O72―氧化生成Fe3+,当溶液碱性达到一定程度时就会产生Fe(OH)3沉淀。
考点:考查外界条件对平衡状态的影响、平衡状态的判断;溶解平衡、电化学原理的应用和计算等
本题难度:困难
2、填空题 (9分)盐酸常用于清除金属表面的铜锈铁锈。某同学欲将除锈后的盐酸中的金属元素分步沉淀,查资料获知常温下水溶液中各离子沉淀的pH范围:
离子
| 开始沉淀的pH
| 沉淀完全的pH
|
Fe3+
| 1. 0
| 3. 0
|
Fe2+
| 5. 8
| 8. 8
|
Cu2+
| 4.2
| 6.7
|
(1)若以离子浓度降至1×10-5 mol・L-1为沉淀完全,根据上表数据推算出ksp[Fe(OH)3]=
(2)根据上述数据该同学设计了以下实验流程:
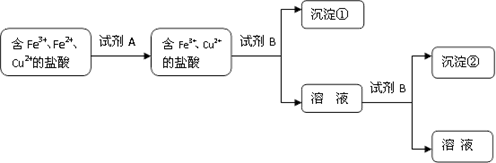
A可能是 ;试剂B的化学式是 ;沉淀②化学式是 。
参考答案:(共9分):(1)1.0×10-38(3分)
(2)双氧水(氯气或氧气或臭氧也给2分)(2分)NaOH(或其它可溶性碱) (2分)Cu(OH)2(2分)
本题解析:(1)根据表格的数据可知Fe3+沉淀完全的溶液的pH="3." 0, c(OH-)=10-11,离子浓度降至1×10-5 mol・L-1为沉淀完全,则ksp[Fe(OH)3]=c(Fe3+)?c3(OH-)=1×10-5×(10-11)3=1×10-38; (2)向含有Fe3+、Fe2+、Cu2+的盐酸溶液中加入双氧水等氧化剂,会把Fe2+氧化为Fe3+,得到含有Fe3+、Cu2+的盐酸溶液,然后向该溶液中加入NaOH溶液,调整溶液的pH=4,这时首先得到Fe(OH)3沉淀,过滤,得到的滤液中再加入NaOH只溶液的pH≥6.7,溶液中的Cu2+就会形成Cu(OH)2沉淀,因此沉淀②是Cu(OH)2。
考点:考查沉淀溶解平衡常数的计算、溶液中杂质离子除去的试剂的选择、沉淀的成分的确定的知识。
本题难度:困难
3、选择题 对于难溶盐MX,其饱和溶液中M+和X-浓度之间的关系为Ksp=c(M+)?c(X-),现将足量的AgCl分别放入下列物质中,AgCl的溶解度由大到小的顺序是(?)
①20mL0.01mol?L-1?KCl溶液;②30mL0.02mol?L-1CaCl2溶液;③40mL0.03mol?L-1HCl溶液;④10mL蒸馏水;⑤50mL0.05mol?L-1AgNO3溶液
A.①>②>③>④>⑤
B.④>①>③>②>⑤
C.⑤>④>②>①>③
D.④>③>⑤>②>①
参考答案:B
本题解析:根据氯化银的溶解平衡可知,溶液中氯离子浓度或银离子浓度越大,氯化银的溶解度就越小。所以根据溶液中氯离子或银离子浓度大小可知,选项B正确,答案选B。
本题难度:一般
4、选择题 下表是五种银盐的溶度积常数(25℃),下列有关说法错误的是
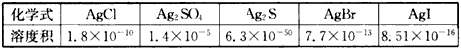
[? ]
A.五种物质在常温下溶解度最大的是Ag2SO4
B.将AgCl溶解于水后,向其中加入Na2S,则可以生成黑色的Ag2S沉淀
C.沉淀溶解平衡的建立是有条件的,外界条件改变时,平衡也会发生移动
D.常温下,AgCl、AgBr和AgI三种物质的溶解度随着氯、溴、碘的顺序逐渐增大
参考答案:D
本题解析:
本题难度:一般
5、选择题 把氢氧化钙放入蒸馏水中,一定时间后达到如下平衡Ca(OH)2(s) Ca2++2OH-加入以下物质,可使
Ca2++2OH-加入以下物质,可使
Ca(OH)2(s)减少的是
[? ]
A.蒸馏水
B.A1C13溶液
C.NaOH溶液
D.CaCl2溶液
参考答案:AB
本题解析:
本题难度:一般