��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� ���������߷ֱ��ʾԪ�ص�ij��������˵�����Ĺ�ϵ��ZΪ�˵������YΪԪ�ص��й����ʣ���

���������Ԫ���й�������������ߵı��������Ӧ�����У�
��1����A��Ԫ�صļ۵�����______?��2����������Ԫ�ص�����ϼ�______
��3��IA������Ԫ�ص����۵�______
��4��������������Na+��Mg2+��Al3+��P3-��S2-��Cl-�����Ӱ뾶______
��5���ڶ���������Ԫ����ԭ����������ԭ�Ӱ뾶�ı仯______
���ڢ�126C?��3919K?��4020Ca?��136C?��147N?��4018Ar�У����������գ�
��1����Ϊͬλ�ص���______��______��
��2����������ȣ������ܻ���ͬλ�ص���______��______��
��3����������ȣ�������������ȵ���______��______��______��______��
�ο��𰸣���1����A��Ԫ�صļ۵�����Ϊ2����˵�������۵��������䣬��ͼB���ϣ�
��ѡ��B��
��2����������Ԫ�ص�����ϼۣ���˵������������ϼ���+1�۵�����+7�������ϡ������0�۽�������ͼC���ϣ�
��ѡ��C��
��3�����������˵������������������������۵㽵�ͣ���ͼA���ϣ�
��ѡ��A��
��4�����Ӳ�ṹ��ͬ���˵����Խ�����Ӱ뾶ԽС���������Ӱ뾶Na+��Mg2+��Al3+��P3-��S2-��Cl-��������������ͬ�����Ӳ�Խ�࣬���Ӱ뾶Խ���������Ӱ뾶Cl-��Na+���������Ӱ뾶P3-��S2-��Cl-��Na+��Mg2+��Al3+����ͼE���ϣ�
��ѡ��E��
��5��ͬ��������Ԫ�أ���ԭ����������ԭ�Ӱ뾶��С����ͼG���ϣ�
��ѡ��G��
��1����������ͬ��������ͬ��ͬһԪ�ز�ͬԭ�ӻ�Ϊͬλ�أ���126C?�͢�136C?��������ͬΪ6����������ͬ���ֱ�Ϊ6��7��Ϊ̼Ԫ�ص�ͬλ�أ�?
��ѡ���ٺ͢ܣ�
��2����4020Ca�͢�4018Ar���������Ϊ40���Dz�ͬԪ�أ����ܻ���ͬλ�أ�
��ѡ���ۺ͢ޣ�
��126C?��3919K?��4020Ca?��136C?��147N?��4018Ar��
��3����136������Ϊ6��������Ϊ13-6=7����147N������Ϊ7��������Ϊ14-7=7��������������ȣ�������������ȣ�
��3919K������Ϊ19��������Ϊ39-19=20����4020Ca������Ϊ20��������Ϊ40-20=20��������������ȣ�������������ȣ�
��ѡ���ܺ͢ݣ��ںۣ͢�
���������
�����Ѷȣ�һ��
2������� ����A��B��C��D��E����Ԫ�أ����ǵ��������������࣮
��A�ĺ˵��������2�����γ��⻯��H2A�����⻯���ڳ�������Һ�壻
��A��B��Ԫ�ؿ��γ�B2A3������û������������ǿ�ᣬ��������ǿ�
��C+���ӱ�B3+���Ӷ�8�����ӣ�
��C��DԪ�ؿ����γɻ�����CD��
��CD����Һ��ͨ��������ӵ�����Һ����ɫ��
�������ڱ���E����C�����������ڣ�E���ʿ�����ˮ��Ӧ������������ӦʱE�ĵ��������ɵ����������ʵ���֮��Ϊ2��1���Իش�
��1��B��______��E��______����дԪ�����ƣ���
��2��B�����ӽṹʾ��ͼ______��D�ĵ��ʷ��ӵĵ���ʽ______��CԪ������������ˮ����ĵ���ʽ______��
��3���õ���ʽ��ʾH2A�γɹ��̣�______
��4��д��CD����Һ��ͨ�����������ӷ���ʽ��______
��5���Ƚ�B��C��E����Ԫ���γɵļ����������Ե�ǿ������B��C��E������ʵ�����ӷ��ű�ʾ�������ԣ�______��
�ο��𰸣�A��B��C��D��E����Ԫ�أ����ǵ��������������࣮
��A�ĺ˵��������2�����γ��⻯��H2A�����⻯���ڳ�������Һ�壬��AΪ��Ԫ�أ�
��A��B��Ԫ�ؿ��γ�B2A3������û������������ǿ�ᣬ��������ǿ���BΪ��Ԫ�أ�
��BΪ��Ԫ�أ�C+���ӱ�B3+���Ӷ�8�����ӣ���CΪ��Ԫ�أ�
��C��DԪ�ؿ����γɻ�����CD����CD����Һ��ͨ��������ӵ�����Һ����ɫ����DΪ��Ԫ�أ�
��CΪ��Ԫ�أ������ڱ���E����C�����������ڣ�E���ʿ�����ˮ��Ӧ������������ӦʱE�ĵ��������ɵ����������ʵ���֮��Ϊ2��1����EΪ+1�۽��������Ԫ��ͬ���壬��EΪCsԪ�أ�
��1��������������֪��B����Ԫ�أ�E���Ԫ�أ��ʴ�Ϊ������藍�
��2��B����Ԫ�أ���������2�����Ӳ㣬����������Ϊ13���������8�����ӣ������ӽṹʾ��ͼ
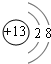
��
DΪ��Ԫ�أ�D�ĵ��ʷ��ӵĵ���ʽΪ
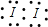
��CΪ��Ԫ�أ�CԪ������������ˮ����ΪKOH������ʽΪ
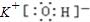
��
�ʴ�Ϊ��

��
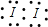
��
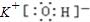
��
��3��AΪ��Ԫ�أ��õ���ʽ��ʾH2O�γɹ���Ϊ
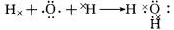
��
�ʴ�Ϊ��
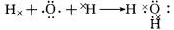
��
��4����������ǿ�����ԣ�KI��Һ��ͨ������������������������Ϊ�ⵥ�ʣ���Ӧ�����ӷ���ʽ2I-+Cl2�TI2+2Cl-���ʴ�Ϊ��2I-+Cl2�TI2+2Cl-��
��5��B����Ԫ�أ�CΪ��Ԫ�أ�D���Ԫ�أ�������Al��K��Cs������B��C��E����Ԫ���γɵļ�����������Al3+��K+��Cs+��
�ʴ�Ϊ��Al3+��K+��Cs+��
���������
�����Ѷȣ�һ��
3��ѡ���� A��B��C��DΪ���ֶ���������Ԫ�أ���ԭ����������������֪A������������������Ӳ�����2����B�ǵؿ��к�����ߵ�Ԫ�أ�Bԭ�ӵ�������������Dԭ��������������2����Cԭ�������ֻ��һ�����ӣ�����˵����ȷ���ǣ�������
A������������Ӧˮ����ļ��ԣ�C��D
B����̬�⻯����ȶ��ԣ�A��B
C������Ԫ���ܹ���ͬһ����
D��ԭ�Ӱ뾶��C��A
�ο��𰸣�A��B��C��DΪ���ֶ���������Ԫ�أ���ԭ��������������B�ǵؿ��к�����ߵ�Ԫ�أ�BΪ��Ԫ�أ�A��ԭ������С����Ԫ�أ�A������������������Ӳ�����2����A��2�����Ӳ㣬������������4����AΪCԪ�أ�Bԭ�ӵ�������������Dԭ��������������2����DԪ��ԭ������������Ϊ2��ԭ������������Ԫ�أ���DΪMgԪ�أ�Cԭ�������ֻ��һ�����ӣ����ڵڢ�A�壬ԭ������������Ԫ�أ���CΪNaԪ�أ�
A��������Na��Mg��������������Ӧˮ����ļ��ԣ�C��D����A����
B���ǽ�����O��S���ǽ�����Խǿ���⻯��Խ�ȶ�������̬�⻯����ȶ��ԣ�A��B����B����
C��O��CԪ�ش��ڵڶ����ڣ�Na��MgԪ�ش��ڵ������ڣ�����Ԫ�ز����ܴ���ͬһ���ڣ���C����
D��ͬ�����������ԭ�Ӱ뾶��С����ԭ�Ӱ뾶Na��Si��ͬ�������϶���ԭ�Ӱ뾶����ԭ�Ӱ뾶Si��C����ԭ�Ӱ뾶Na��C����D���ڣ�
��ѡD��
���������
�����Ѷȣ���
4��ѡ���� M��N����Ԫ�أ���֪Mλ�ڶ����ڣ���M2-��N+�ĵ�����֮��Ϊ8��������˵��һ����ȷ���ǣ�������
A��M��Nԭ�ӵĵ�������֮��Ϊ11
B��M��N��ԭ������֮��Ϊ8
C��M��Nԭ�ӵ�����������֮��Ϊ7
D��M��Nԭ�ӵ�����������֮��Ϊ7
�ο��𰸣��ɼ�����M2-��֪��M���������6�����ӣ�λ�����ڱ��ڢ�A�壬�����ڶ�����Ԫ�أ�����ΪO��S��ԭ�������ֱ�Ϊ8��16��������N+��֪��N�������1�����ӣ�NΪ��A��Ԫ�أ�����ΪH��Li��Na��K��Ԫ�أ�M2-��N+�ĵ�����֮��Ϊ8����������������У�O��K��S��Na��O��Li����
A��M��Nԭ�ӵĵ�������֮�Ϳ���Ϊ8+19=27��16+11=27��8+3=11����A����
B������O��K��ԭ������֮��Ϊ19-8=11������S��Na��ԭ������֮��Ϊ16-11=5������O��Li��ԭ������֮��Ϊ8-3=5����B����
C��M���������6�����ӣ�N�������1�����ӣ�M��Nԭ�ӵ�����������֮��Ϊ7����C��ȷ��
D��M��Nԭ�ӵ�����������֮��Ϊ6-1=5����D����
��ѡC��
���������
�����Ѷȣ�һ��
5��ѡ���� ����������Ԫ��A��B��C��D��ԭ����������������A��DΪͬ��Ԫ�أ�ԭ�Ӱ뾶A��D��C��B��Aԭ�������������Ǵ�����3����B��C�ĺ��������֮����A��D���������֮����ȣ�����˵����ȷ���ǣ�������
A�������Ӱ뾶��B��A
B������������Ӧˮ����ļ��ԣ�B��C
C����̬�⻯����ȶ��ԣ�A��D
D��B��C��D����������ˮ������������Ӧ
�ο��𰸣�����������Ԫ��A��B��C��D��ԭ������������Aԭ�������������Ǵ�����3������A��2�����Ӳ㣬����������Ϊ6����AΪOԪ�أ�A��DΪͬ��Ԫ�أ���DΪSԪ�أ�B��C�ĺ��������֮����A��D���������֮����ȣ���Ϊ8+16=24����ԭ�Ӱ뾶A��D��C��B��B��Cԭ�Ӱ뾶���ӦΪ����Ԫ�أ���֪BΪNaԪ�أ�CΪAlԪ�أ�
A��AΪOԪ�أ�BΪNaԪ�أ�O2-��Na+���Ӳ�ṹ��ͬ���˵����Խ��뾶ԽС����O2-��Na+����A����
B��BΪNaԪ�أ�CΪAlԪ�أ�ͬ����Ԫ�ش����ҽ�������������Ӧ����������ˮ����ļ�������������NaOH��Al��OH��3����B����
C��AΪOԪ�أ�DΪSԪ�أ�ͬ����Ԫ�ش��ϵ��·ǽ������������ǽ���Խǿ����Ӧ���⻯��Խ�ȶ�������A��D����C����
D��B��C��D����������ˮ����ֱ�ΪNaOH��Al��OH��3��H2SO4��Al��OH��3��������������ǿ�ǿ�ᷴӦ���������������ᷴӦ������������ˮ�����߿���������Ӧ����D��ȷ��
��ѡD��
���������
�����Ѷȣ���