微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列有关“核外电子的运动状态”的说法,错误的是
A.各原子轨道的伸展方向按p、d、f的顺序分别为3、5、7
B.核外电子云表示电子在核外单位体积的空间出现的机会多少
C.原子轨道伸展方向与能量大小是无关的
D.原子核外可能有两个电子的运动状态是完全相同的
参考答案:D
本题解析:
答案:D
一个电子的运动状态要从4个方面来进行描述,即它所处的电子层、电子亚层、电子云的伸展方向以及电子的自旋方向。在同一个原子中没有也不可能有运动状态完全相同的两个电子存在,这就是保里不相容原理所告诉大家的。根据这个规则,如果两个电子处于同一轨道,那么,这两个电子的自旋方向必定相反。也就是说,每一个轨道中只能容纳两个自旋方向相反的电子。在不违反泡利原理的条件下,电子优先占据能量较低的原子轨道,使整个原子体系能量处于最低,这样的状态是原子的基态;在能量相等的轨道上,自旋平行的电子数目最多时,原子的能量最低。所以在能量相等的轨道上,电子尽可能自旋平行地多占不同的轨道。
A.各原子轨道的伸展方向按p、d、f的顺序分别为3、5、7正确;
B.核外电子云表示电子在核外单位体积的空间出现的机会多少,正确;
C.原子轨道伸展方向与能量大小是无关的,正确;
D.不正确,根据包利不相容原理,原子核外不可能有两个电子的运动状态是完全相同的。
本题难度:一般
2、填空题 (12分)根据所学物质结构知识,请你回答下列问题:
(1)人们把电子云轮廓图称为原子轨道,S电子的原子轨道都是?形的,P电子的原子轨道都是?形的。
(2)原子序数为24的元素原子中有?个能层,?个能级,?个未成对电子。
(3)硅原子核外电子排布式为?,价电子排布式为?
(4)NCl3常温下为黄色粘稠的油状液体,可用作引爆剂和化学试剂。NCl3分子的VSEPR模型是?,立体构型是?,中心原子采取?杂化方式。
(5)具有(n-1)d10ns2电子构型的元素位于周期表中?区和?族。
参考答案:.(1)球,哑铃?(2)4,7,6?(3)1s22s22p33s23p2,3s23p2
(4)四面体形,三角锥形,SP3 ?(5)ds,ⅡB
本题解析:(1)考查原子轨道的有关判断。根据电子云的形成可知,S电子的原子轨道都是球形的,P电子的原子轨道都是哑铃形的。
(2)原子序数为24的元素是Cr元素,位于第四正确第ⅥB,所以根据构造原理可知,其原子核外电子的排布式是1s22s22p63s23p63d54s1,因此原子中含有4个能层,7个能级和6个未成对电子。
(3)硅原子的原子序数是14,所以根据构造原理可知,硅原子核外电子排布式为1s22s22p33s23p2,其价电子排布式为3s23p2。
(4)根据价层电子对互斥理论可知,该化合物中氮原子含有的孤对电子对数是(5-1×3)÷2=1,所以VSEPR模型是四面体形结构,由于含有1对孤对电子,所以立体构型是三角锥形结构,而氮原子则是sp3杂化。
(5)区的名称来自于按照构造原理最后填入电子的能级的符号,所以具有(n-1)d10ns2电子构型的元素位于周期表中ds区和第ⅡB族。
本题难度:一般
3、填空题 下表是元素周期表一部分,列出了十个元素在周期表中的位置:
?族
周期
| IA
| IIA
| IIIA
| IVA
| VA
| VIA
| VIIA
| 0
|
2
| ?
| ?
| ?
| ⑥
| ⑦
| ?
| ?
| ?
|
3
| ①
| ③
| ⑤
| ?
| ?
| ?
| ⑧
| ⑩
|
4
| ②
| ④
| ?
| ?
| ?
| ?
| ⑨
| ?
|
请用化学用语回答下列问题
(1)在③~⑦元素中,原子半径最大的是? ?(填元素符号);
(2)①~⑩中元素最高价氧化物对应的水化物中酸性最强的是?(填物质化学式),呈两性的氢氧化物是?(填物质化学式);
(3)⑦元素的最高价氧化物对应水化物与其氢化物能生成盐M,M中含有的化学键类型有?;?
(4)用电子式表示元素③与⑧形成化合物的过程?。
(5)写出含有32个电子的元素⑥的氢化物的分子式:?。
(6)写出工业冶炼⑤的化学方程式:?
(7)写出将⑨元素单质从海水中(离子形式存在)提取所涉及到的三个步骤的离子方程式,第一步:Cl2+2Br-=2Cl-+Br2 第二步:??; 第三步Cl2+2Br-=2Cl-+Br2
参考答案:(1)Ca
(2)HClO4、 Al(OH)3?
(3)离子键、(极性)共价键
(4)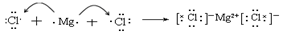
(5)C4H8
(6)2Al2O3 4Al +3O2↑?冰晶石
4Al +3O2↑?冰晶石
(7)Br2+ SO2 +2H2O=4H+ + SO42- + 2Br-
本题解析:①~⑩各元素分别为Na、K、Mg、Ca、Al、C、N、Cl、Br和Ar。(1)电子层数最多的元素,其原子半径最大;(2)元素最高价氧化物对应的水化物酸性最强,则该元素的非金属性最强;(3)M物质为NH4NO3,离子化合物,含有离子键和共价键;(4)元素③与⑧形成化合物氯化镁,离子化合物,故用箭头表示电子的转移;(5)元素⑥的氢化物为CxHy,电子为12x+y=32,x、y之间的关系还应符合烷烃或烯烃或炔烃的通式;(6)Al是活泼金属,工业冶炼需用电解法。
点评:元素周期表及其规律是高考必考知识点,考生在备考中应注意积累掌握短周期元素的结构与性质。
本题难度:一般
4、选择题 己知A、B、C、D、E是短周期中原子序数依次增大的5种元素,B、C同周期,D、E也同周期,D原子最外层电子数与最内层电子数相等,A、B、C、D的原子序数之和是E的两倍,D与C形成的化合物是一种耐高温材料,A、B形成的气态化合物的水溶液呈碱性。下列说法正确的是
A.原子半径:D>B>E>C>A ?B.单质D可用海水作原料获得
C.热稳定性:EA4>A2C ?D.化合物DC与化合物EC2中化学键类型相同
参考答案:B
本题解析:A、B形成的气态化合物的水溶液呈碱性,该氢化物是氨气。又因为A、B、C、D、E是短周期中原子序数依次增大的5种元素,所以A是H,B是N。D原子最外层电子数与最内层电子数相等,D是第三周期元素,所以D是Mg。D与C形成的化合物是一种耐高温材料,所以C是O,该化合物是氧化镁。A、B、C、D的原子序数之和是E的两倍,所以E的原子序数是(1+7+8+12)÷2=14,即E是Si。A、同周期自左向右原子半径逐渐减小,同主族自上而下原子半径逐渐增大,所以原子半径是D>E>B>C>A,A不正确;B、海水中含有大量的镁元素,所以单质Mg可用海水作原料获得,B正确;C、非金属性越强,氢化物的稳定性越强,氧元素的非金属性强于硅元素的,则稳定性是H2O>SiH4,C不正确;D、化合物MgO与化合物SiO2中化学键类型不相同,前者是离子键,后者是极性键,D不正确,答案选B。
本题难度:一般
5、选择题 有科学家认为,随着文明的发展和社会的进步,人类有可能合成出或者从其他星球上发现
原子序数较大的元素,若发现或研制出第175号元素。试根据元素周期表知识推测,这种元素可能存在的位置是(已知:①第n周期最多容纳的元素种数为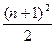 或
或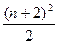 ,n=1,2,3……;②各周期中元素的种类数都是偶数)(? )
,n=1,2,3……;②各周期中元素的种类数都是偶数)(? )
A.ⅡB族
B.第八周期
C.第九周期
D.ⅥA族
参考答案:C
本题解析:根据元素周期表可知,前七周期元素种类总数为2+8+8+18+18+32+32=118,也可由题给公式进行计算:
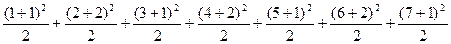 =2+8+8+18+18+32+32=118,
=2+8+8+18+18+32+32=118,
第8周期元素种数为 =50,第九周期的元素种数为
=50,第九周期的元素种数为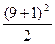 =50。故175号元素应在第九周期,B错误;而第九周期中零族元素的原子序数为218,故ⅡB族及ⅥA族的原子序数应分别为212和216,故A、D项不正确,只能选C。
=50。故175号元素应在第九周期,B错误;而第九周期中零族元素的原子序数为218,故ⅡB族及ⅥA族的原子序数应分别为212和216,故A、D项不正确,只能选C。
本题难度:简单