| 高考省级导航 | |
|
|
| 高考省级导航 | |
|
|
|
高中化学知识点归纳《气体的净化、干燥、吸收与收集》考点强化练习(2017年押题版)(十)
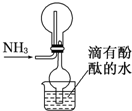 参考答案:A.氨气的密度小于空气密度,且和氧气不反应,所以收集氨气可以采用向下排空气法收集,故A正确; 本题解析: 本题难度:简单 2、实验题 (12分).某学生根据石蜡油在碎瓷片或氧化铝催化作用下能分解得到乙烯的性质,设计下图的实验装置。据图回答: 参考答案:(1)石蜡和氧化铝(或碎瓷片)(2)导气冷凝?(3)将分解产生的气体冷凝? 本题解析:(1)试管①是发生装置,所以盛的是石蜡和氧化铝(或碎瓷片)。 本题难度:一般 3、选择题 下列除杂方法正确的是 参考答案:D 本题解析:略 本题难度:简单 4、实验题 医用氯化钙可用于补钙、抗过敏和消炎等,以工业碳酸钙(含少量Na+、Al3+、Fe3+等杂质)生产医用二水合氯化钙工艺流程为:
(1)CaCO3与盐酸反应的离子方程式?。 (2)除杂操作是加入氢氧化钙,调节溶液的pH为?,目的是除去溶液中少量的Al3+、Fe3+。检验Fe(OH)3是否沉淀完全的实验操作是? ?。 (3)过滤时需用的玻璃仪器有?。滤渣主要成分的化学式?。 (4)酸化时加盐酸的目的为:①?,②防止Ca2+ 在蒸发时发生水解。 (5)为什么蒸发结晶要保持在160℃:?。 (6)测定晶体样品的纯度:若用一定浓度的AgNO3溶液滴定一定质量的晶体样品,所测样品中CaCl2 ・2H2O的质量分数偏高(忽略其它实验误差),可能的原因之一为?。 参考答案:(16分,每空2分) 本题解析:(1)盐酸是强酸,酸性比碳酸强,则难溶于水的碳酸钙易溶于盐酸,生成可溶性的氯化钙、二氧化碳气体和水,将易溶且易电离的化合物改写成离子形式,其余物质都保留化学式,删去实际上未反应的离子,则该反应为CaCO3+2H+=Ca2++CO2↑+H2O;(2)根据表中氢氧化物完全沉淀时的pH可知,除去溶液中少量铁离子和铝离子应使溶液pH介于5.2~7.8之间或者5.2≤pH<7.8,低于3.7时铁离子不能完全变为氢氧化铁沉淀,低于5.2时铝离子不能完全变为氢氧化铝沉淀,高于7.8时,氢氧化铝开始变为偏铝酸根离子,溶液又引入新的杂质;检验氢氧化铁是否沉淀的方法就是检验溶液中是否存在铁离子,由于铁离子遇KSCN溶液变红的特征反应,通常设计的实验方案为:静置,取少量上层清液于小试管中,滴加KSCN溶液,若不显红色,则Fe(OH)3沉淀完全,反之,则Fe(OH)3沉淀不完全;(3)过滤属于化学实验基本操作,也是混合物分离与提纯的常用方法,主要使用烧杯、玻璃棒、普通漏斗等仪器;当溶液pH介于5.2~7.8之间时,铁离子、铝离子完全变为氢氧化铁沉淀、氢氧化铝沉淀,则过滤所得滤渣的成分为Fe(OH)3、Al(OH)3;(4)氢氧化钙是除杂试剂,除杂试剂一定过量,氢氧化钙是强碱,由于目标产物是氯化钙,则酸化时加入盐酸的目的是除去过量的氢氧化钙,将其转化为氯化钙,防止氢氧化钙吸收空气中的二氧化碳,且过量的盐酸受热易挥发逸出(逸出的氯化氢气体可循环利用),不能加硝酸或硫酸酸化,因为它们除去旧杂质时会引入硝酸根离子或硫酸根离子等新杂质;(5)结晶水化合物受热可能失去结晶水,蒸发结晶要控制温度在160℃的原因是,温度太高,二水合氯化钙会失去结晶水;(6)滴定原理为:Ag++Cl-=AgCl↓,若氯离子的物质的量偏大,则测定结果偏高;酸化后所得溶液主要含有氯化钙、氯化钠、氯化氢,蒸发结晶时逸出氯化氢,但是没有除去钠离子,则所得晶体是二水合氯化钙和氯化钠的混合物,氯元素的质量分数:CaCl2>NaCl> CaCl2?H2O >CaCl2?2H2O,因此晶体样品中含有NaCl或二水合氯化钙失去全部或部分结晶水得到的CaCl2或CaCl2?H2O,都能导致所含氯元素的质量分数偏高,则所测样品二水合氯化钙的质量分数偏高。 本题难度:困难 5、填空题 用如图所示装置可以收集以下几种气体(烧瓶位置不动)(填字母,下同); 参考答案:(1)①③⑤;②④⑦?(2)①③⑥? A?(3)B 本题解析:(1)关键装置图可知,若烧瓶是干燥的,由A口进气收集气体,这说明该气体的密度小于空气的,因此符合条件的是氢气、甲烷和氨气,答案选①③⑤;由B口进气收集气体,这说明该气体的密度大于空气的,因此符合条件的是SO2、氯化氢和H2S,NO极易被氧化,不能用排空气法收集,答案选②④⑦。 本题难度:一般 | |||||||||||||
|
||
| 【大 中 小】【打印】 【繁体】 【关闭】 【返回顶部】 | ||
| 下一篇:高中化学知识点归纳《离子共存》.. | ||