微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列溶液中,一定能大量共存的微粒组是
[? ]
A.pH=1的溶液中:K+、Cr2O72-、CH3CH2OH、SO42-
B.含有大量Fe3+的溶液中:Al3+、Cu2+、Cl-、SO42-
C.加入Al能放出H2的溶液中:K+、NH4+、NO3-、Cl-
D.滴加紫色石蕊试液变红的溶液中:K+、Ba2+、NO3-、F-
参考答案:B
本题解析:
本题难度:一般
2、选择题 在强酸性的溶液中,下列各组离子可以大量共存的是
A.K+、Ba2+、Cl-、NO3-
B.Ca2+、Al3+、HCO3-、Cl-
C.Na+、AlO2-、OH-、SO42-
D.K+、NH4+、NO3-、Fe2+
参考答案:A
本题解析:
B.H+和HCO3-在溶液中不能大量共存;
C.H+和OH-在溶液中不能大量共存;
D.H+和NO3-具有强氧化性,能氧化Fe2+。
点评:考查离子共存。离子共存,即不反应,无沉淀,无气体,无弱电解质生成;
本题难度:一般
3、计算题 (8分)现有pH都等于1的盐酸和硫酸,及溶液的浓度都等于0.1 mol・L-1的NaOH和Ba(OH)2溶液,四种溶液以等体积混合时,求所得溶液的pH。
参考答案:12.4
本题解析:假设溶液的体积均为1 L,混合后溶液的总体积为4 L。
n总(H+)=n盐酸(H+)+n硫酸(H+)="0.1" mol・L-1×1 L+0.1 mol・L-1×1 L="0.2" mol
n总(OH-)=nNaOH(OH-)+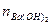 (OH-)="0.1" mol・L-1×1 L+2×0.1 mol・L-1×1 L="0.3" mol
(OH-)="0.1" mol・L-1×1 L+2×0.1 mol・L-1×1 L="0.3" mol
混合后,n混(OH-)="0.3" mol-0.2 mol="0.1" mol
所以c(OH-)="0.1" mol/4 L="0.025" mol・L-1
c(H+)=KW/0.025 mol・L-1=4×10-13 mol・L-1
pH=13-2lg2=12.4。
本题难度:一般
4、填空题 某溶液中可能含有Na+、H+、CO32-、HCO3-、NO3-、SO42-、Cl-、OH-离 子中的几种或全部,①取少量该溶液,加入过量氢氧化钡溶液,产生白色沉淀,该沉淀在盐酸中完全溶解;②另取少量该溶液,加入氯化铵并加热,有剌激性气味的气体X产生,该气体能使湿润的红色石蕊试纸变蓝;③在做②实验后的溶液中,加入硝酸酸化的硝酸银溶液,有白色沉淀产生。
子中的几种或全部,①取少量该溶液,加入过量氢氧化钡溶液,产生白色沉淀,该沉淀在盐酸中完全溶解;②另取少量该溶液,加入氯化铵并加热,有剌激性气味的气体X产生,该气体能使湿润的红色石蕊试纸变蓝;③在做②实验后的溶液中,加入硝酸酸化的硝酸银溶液,有白色沉淀产生。
(1)该溶液中肯定大量存在的离子为?;
(2)写出②的离子方程式:?。
(3)X与第三周期所有非金属元素的氢化物比较,熔沸点偏高,原因是:?。
(4)与X含相同元素的另一简单化合物Y,其所含元素质量比为7:1或者1:7,1gY液态时完全燃烧,生成液态水和另一单质时,放出QkJ的热量,则Y燃烧的热化学方程式为:?。
参考答案:(1) (3分)? Na+、CO32-、OH-(无Na+不给分);
(2)? NH4++OH-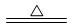 NH3↑+H2O。
NH3↑+H2O。
(3) 氨分子间形成了氢键。
(4) (3分)? N2H4(l)+O2(g) ="?" N2(g)+2H2O(l);△H=-32QkJ/mol。
本题解析:略
本题难度:一般
5、选择题 氯化钡有剧毒,致死量为0.3g,万一不慎误服,应大量吞服
鸡蛋清及适量解毒剂,此解毒剂是()
A? AgNO3? B? CuSO4? C? MgSO4? D? NA2CO3?
参考答案:C
本题解析:略
本题难度:简单