��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ����ʵ�鷽���������ǣ�������
A������ˮ����NH4Cl��NaOH��NaCl���ֹ���
B���������۳�ȥFeCl2��Һ�е�������CuCl2
C�����ó���ʯ��ˮ����Na2CO3��Һ��NaHCO3��Һ
D��Ϊȷ�ⶨ������NaOH��Һ��Ӧ���к��ȣ�������ͼ�����ʵ����������
�ο��𰸣�A��NH4Cl��NaOH��NaCl���ֹ��嶼������ˮ������ˮ����Ӧ��û�����Ե����������𣬹ʴ���
B�������û�ͭ����ӦΪ��Fe+Cu2+�TFe2++Cu����û�������µ����ʣ���B��ȷ��
C��Na2CO3��NaHCO3���������ʯ��ˮ��Ӧ����̼��Ƴ�������Ӧ�ֱ�Ϊ��CO32-+Ca2+�TCaCO3����HCO3-+Ca2++OH-�TH2O+CaCO3������C����
D���ⶨ�к���ʱ��Ϊʹ�����ַ�Ӧ������������ӷ�������ʵ��������������ҺӦ��������D����
��ѡB��
���������
�����Ѷȣ�һ��
2��ʵ���� �����15�֣���ʽ̼��ͭ��Cu2(OH)2CO3����һ����;�㷺�Ļ���ԭ�ϣ�ʵ�����Է�ͭмΪԭ����ȡ��ʽ̼��ͭ���ⶨ��Ʒ���ʵIJ������£�
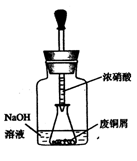
����һ����ͭм������ͭ
��ͼ10���ý�ͷ�ι���ȡŨHNO3�����ӵ���ƿ�ڵķ�ͭм��(��ͭм����)����ַ�Ӧ����ˣ��õ�����ͭ��Һ��
���������ʽ̼��ͭ���Ʊ�
����Թ��м���̼������Һ������ͭ��Һ��ˮԡ������70�����ң���0.4 mol��L?��NaOH��Һ����pH��8.5�������ã����ˣ�����ˮϴ�ӣ���ɣ��õ���ʽ̼��ͭ��Ʒ��
���������ⶨ��Ʒ�м�ʽ̼��ͭ����
1�����գ�ȡn g��Ʒ�����������г������
�ⶨ������̼������?
���ݶ�����̼����������Ʒ�м�ʽ̼��ͭ������
���������գ�
��1������һ��ͼװ����NaOH��Һ��������?����Ӧ�������ƿ�ڵ���Һ�У����˺���NaOH�⣬����??(��д��ѧʽ)��
��2�������
��д����Ӧ�����ӷ���ʽ?
��������pH����8.5���ƵIJ�Ʒ��������?���������٣����䣩
��3����������
��д����ʽ̼��ͭ�ֽⷽ��ʽ
�����ȷ����Ʒ�ֽ���ȫ��?
�۲�����2�е�ʵ�鲽��?
����ʵ������Ʒ�м�ʽ̼��ͭ��������100%�����ܵ�ԭ����?
�ο��𰸣���1�����յ�������? NaNO3? NaNO2
��2��CO32����2Cu2����2OH��= Cu2(OH)2CO3?����
��3�� �� Cu2(OH)2CO3="=" 2CuO��CO2����H2O
�����պ���ȴ����������������������
��ʹ��������������ͨ��ʢ��Ũ����ϴ��ƿ����ʯ�Ҹ���ܢ�ʯ�Ҹ���ܢ�����ʯ�Ҹ���ܢ����ص��������Ƕ�����̼������
�ܲ�Ʒ�к���̼��ͭ���ʣ�����������˶�����̼��ˮ��
�����������1��ͭ�����ᷴӦ�����������������Ⱦ��������Ӧ��ȥ�����������������������Ʒ�Ӧ��
NaOH+NO+NO2=NaNO2+ H2O? 2NaOH+2NO2=NaNO2+ NaNO3+H2O
���Է�Ӧ����Һ�к���NaOH��NaNO2�� NaNO3��
��2��pHֵ���߲���������ͭ���ʣ����²�Ʒ�������٣���3����Ʒ�ֽ����������̼��ˮ�������ⶨ������̼�������ȳ���ˮ������ͬʱ��ֹ�����ж�����̼��ˮ��������ʯ�����գ���Ʒ�м�ʽ̼��ͭ��������100%��˵������ܢ���������ƫ�����Ǻ��в���������̼�������̼��ͭ��Ҳ������ˮ����û����ȫ���ն�������ܢ����գ�������ж�����̼��ˮ�ȱ�����ܢ����ա�
�����Ѷȣ�һ��
3��ѡ����
A��NaOH ��Һ
B��Na2CO3��Һ
C��NaHCO3����Һ
D������ʯ��ˮ
�ο��𰸣�C
���������NaOH��Ca(OH)2���Ǽ������ʣ�CO2��SO2���ܱ�ȫ�����գ�Na2CO3��Һ����SO2���ã���Na2CO3�����Σ�Ҳ����CO2����������ʽ��NaHCO3��
�����Ѷȣ���
4��ʵ���� �������ᴿ�����е㲻ͬ��Һ������ķ���������ʱҪע����Щ�������
?
�ο��𰸣��¶ȼ�Ӧ����֧�ڡ���ƿ�ײ�Ҫ��ʯ��������ȴˮҪ�ͽ��߳���
�������������ʱ�¶ȼƲ����IJ�����Һ�¶ȣ������������¶ȣ������¶ȼƵ�ˮ����Ӧ�÷���������ƿ��֧�ܳ��ڴ������������ƿ����ֱ�Ӽ��ȣ���Ҫ��ʯ�������������ȴʱ��ȴˮҪ�ͽ��߳���Ϊ��ֹҺ�����ʱ���ҵĵ�����Ӧ�ü������Ƭ�����С�
�����Ѷȣ���
5��ѡ���� Ϊ�ﵽԤ�ڵ�ʵ��Ŀ�ģ����з������е��ǣ�������
A�����ܽ⡢���˵ķ����ᴿ�����������ᱵ��̼�ᱵ
B��Ϊ��С�к͵ζ�����ƿ����ϴ������ɺ����ʹ��
C������ˮ�����顢���Ȼ�̼���Ҵ�������ɫ��Һ
D���������������������м���NaOH��Һ�ٷ�Һ���ᴿ��������
�ο��𰸣�A�����ᱵ��̼�ᱵ��������ˮ��ֱ�����ܽ⡢���˵ķ������ܳ�ȥ���ɼ�������������ܽ���ٹ��ˣ���A����
B����ƿ�����Ƿ�����ʵ������û��Ӱ�죬��B����
C�����顢���Ȼ�̼��������ˮ���������ܶȱ�ˮС�����Ȼ�̼�ܶȱ�ˮ���Ҵ���ˮ���ܣ���ˮ�ɼ��𣬹�C��ȷ��
D������������NaOH��Һ�з���ˮ�⣬Ӧ�ñ���̼������Һ���룬��D����
��ѡC��
���������
�����Ѷȣ���