微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列仪器使用前必须检查是否漏水的是?
A.分液漏斗
B.漏斗
C.蒸发皿
D.长颈漏斗
参考答案:A
本题解析:略
本题难度:简单
2、选择题 下列物质不需密封保存的是
A.浓硝酸
B.氯化亚铁溶液
C.镁条
D.氯水
参考答案:C
本题解析:A、浓硝酸具有挥发性,需要密封保存,故A错误;B、氯化亚铁容易被空气中的氧气氧化,需要密封保存,故B错误; C、镁条表面的氧化膜可以保护镁不被继续氧化,故不需要密封保存,故C正确; D、氯水中溶解的氯气易挥发,需要密封保存,故D错误;故选C.
本题难度:简单
3、选择题 用下列实验装置进行的实验,能达到相应实验目的的是
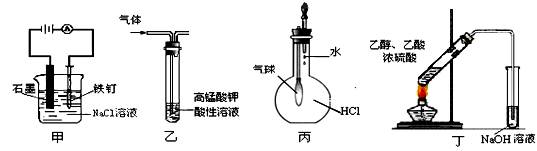
A.装置甲:防止铁钉生绣? B.装置乙:除去乙烯中混有的乙炔
C.装置丙:验证HCl气体在水中的溶解性? D装置丁:实验室制取乙酸乙酯
参考答案:C
本题解析:A为电解池,铁为阳极,将放电失电子而生锈;乙烯、乙炔均可被氧化;制取乙酸乙酯时不应用NaOH吸收,酯会碱性条件下水解
本题难度:一般
4、实验题 (8分)实验室里常见到右图所示仪器,该仪器为两头密封的玻璃管,中间带有一根玻璃短柄。该仪器可进行多项实验。当玻璃管内装有碘晶体时,用此仪器可进行碘升华实验,具有装置简单、操作方便、现象明显、没有污染,可反复使用等优点。
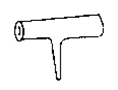
(1)用此仪器不能反复进行的实验是?(填序号)?
A.NH4Cl固体受热分解
B.KMnO4晶体受热分解
C.白磷和红磷一定温度下互相转变
D.无水CuSO4和胆矾的互变实验