��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ijԪ�ص�ԭ��������Ӳ��Ų���5s25p1,��Ԫ�ػ��仯���ﲻ���ܾ��е������� ��?��
A����Ԫ�ص����ǵ���
B����Ԫ�ص�����һ���������������ᷴӦ
C����Ԫ�ص�����ϼ۳�+5��
D����Ԫ�ص��������ˮ�����Լ���
�ο��𰸣�C
�����������Ԫ�ص�ԭ��������Ӳ��Ų���5s25p1��֪��Ԫ�������ڱ���λ�ڵ������ڵ�IIIA�塣��In������Ԫ�������ɣ�ͬһ�����Ԫ�أ����ϵ��£�����ԭ�Ӻ�����Ӳ��������࣬ԭ�Ӱ뾶������Ԫ�صĽ���������ǿ���ǽ�������������˸�Ԫ���ǽ���Ԫ�أ��ǵ��塣A��ȷ��������Ա�Alǿ����˸�Ԫ�ص�����һ���������������ᷴӦ��B��ȷ�����ڸ�Ԫ�ص�ԭ�ӵ��������3�����ӣ���������ϼ۳�+3�ۣ�C����D�����ڸ�Ԫ�صĽ����Ա�Alǿ��Ԫ�صĽ�����Խǿ��������������Ӧ��ˮ����ļ��Ծ�Խǿ����˸�Ԫ�ص��������ˮ�����Լ��ԡ�D��ȷ��ѡ��ΪC��
�����Ѷȣ�һ��
2��ѡ���� ���и��������У������ʡ�����������˳�����е���
A.ͭ��������ˮ
B.�������ɱ���Ũ����
C.��ʯ�ҡ���ʯ�ҡ��ռ�
D.���ˮ��������
�ο��𰸣�B
�����������������ͬһ��Ԫ����ɵĴ�������������ɲ�ͬ��Ԫ��֮����ɵĴ������������ɲ�ͬ���ʵķ�����ɵ����ʣ�
�����Ѷȣ���
3��ѡ���� ����˵����ȷ���ǣ�?��
A��������Ԫ���⣬������Ԫ�ص�����ϼ�����ֵ�϶����ڸ�Ԫ��������������
B����֪MgCO3��KSP=6.82��l0-6�����ں��й���MgCO3��MgCl2��Na2CO3��Һ�У�����c(Mg2+) =c(CO32��)����c(Mg2+)��c(CO32��) = 6.82��10��6 mol2.L-2
C��Ksp(AB2)С��Ksp(CD)��˵��AB���ܽ��С��CD���ܽ��
D�������£���ӦC(s)��CO2(g)==2CO(g)�����Է����У���÷�Ӧ�Ħ�H>0
�ο��𰸣�D
���������A����Ԫ������������ϼۣ�����B�����c(Mg2+)��c(CO32��) = 6.82��10��6 mol2.L-2��ȣ��������ܽ�ƽ��ᷢ���ƶ�������C�����ʵ����Ͳ�ͬ������ͨ��Ksp(AB2)��Ksp(CD)��С���ж��գ�����D�������£���ӦC(s)��CO2(g)==2CO(g)�����Է����У��÷�Ӧ���������ӵģ������÷�Ӧ�Է����У�Ҫʹ��Ӧ�����Է����У���÷�Ӧ�϶����㦤H>0����ȷ��
�����Ѷȣ�һ��
4��ѡ���� ��֪�˵������С��18��X��Y��Z��W����Ԫ��ԭ�ӵĵ��Ӳ�����ͬ����ԭ�Ӱ뾶��������������������������ǿ����
A��HXO4
B��H2YO4
C��H3ZO4
D��H4WO4
�ο��𰸣�A
������������Ӳ�����ͬ��˵��λ��ͬһ���ڡ�ͬ������������ԭ�Ӱ뾶��С���ǽ���������ǿ����Ϊԭ�Ӱ뾶�������������Էǽ�����ǿ��˳����X��Y��Z��W���ǽ�����Խǿ������������ˮ���������Խǿ����ѡA��
�����Ѷȣ�һ��
5��ѡ���� ������Ԫ��X��Y��Z��W��Ԫ�����ڱ��е����λ����ͼ��ʾ������Yԭ�ӵ�����������������Ӳ�����3��������˵����ȷ����
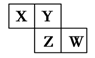
A��Ԫ��Y��Ԫ��Z����������ϼ���ͬ
B�����������Ӱ뾶�Ĵ�С˳��Ϊ��r(W)��r(Y)��r(Z)
C����̬�⻯������ȶ���˳��Ϊ��X��Y��Z
D��Ԫ��W������������Ӧˮ�����������ǿ
�ο��𰸣�D
���������
��ȷ�𰸣�D
X�DN,Y�DO,Z�DS,W�DCl��
A��O�� S��������۷ֱ�Ϊ+2��OF2����+6;
B�����������Ӱ뾶�ɴ�С��S2�D? Cl�D? O2�D?
C����̬�⻯������ȶ���˳��Ϊ��H2O >NH3 >H2S
D����ȷ��HClO4������ǿ
�����Ѷȣ�һ��