微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 一定量的稀盐酸跟过量锌粉反应时,为了减缓反应速率又不影响生成H2的总量,可采取的措施是
[? ]
A.加入少量稀NaOH溶液?
B.加入少量CH3COONa固体
C.加入少量CuSO4固体?
D.升温
参考答案:B
本题解析:
本题难度:一般
2、实验题 (13分)Ⅰ.某学校研究性学习小组开展“不同条件对化学反应速率影响的探究”课题,选用4 mL 0.01 mol・L-1KMnO4溶液与2 mL 0.1 mol・L-1 H2C2O4溶液进行实验,改变条件如下:
组别
| 10%硫酸的体积(mL)
| 温度/℃
| 其他物质
|
①
| 2 mL
| 20
|
|
②
| 2 mL
| 20
| 10滴饱和MnSO4溶液
|
③
| 2 mL
| 30
|
|
④
| 1 mL
| 20
| 1 mL蒸馏水
|
(1)如果研究催化剂对化学反应速率的影响,使用实验 和 (用①~④表示,下同);如果研究温度对化学反应速率的影响,使用实验 和 。
(2)对比实验①和④,可以研究 对化学反应速率的影响,实验④中加入1 mL蒸馏水的目的是 。
Ⅱ.该小组查阅资料得知:C2O42-+MnO4-+H+→ CO2↑+Mn2++H2O(未配平),欲利用该反应测定某草酸钠(Na2C2O4)样品中草酸钠的质量分数。该小组称量1.34 g草酸钠样品溶于稀硫酸中,然后用0.200 mol・L-1的酸性高锰酸钾溶液进行滴定(其中的杂质不跟高锰酸钾和稀硫酸反应)。
(1)滴定前是否要滴加指示剂? (填“是”或“否”),请说明理由 。
(2)滴定时用 (填a或b)滴定管盛装KMnO4标准溶液。
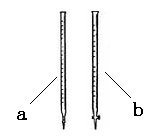
(3)达到终点时消耗了15.00 mL的高锰酸钾溶液,样品中草酸钠的质量分数为 。
参考答案:Ⅰ.(1)①和② (1分) ; ①和③ (1分)
(2)硫酸的浓度或氢离子浓度(2分); 确保①和④组对比实验中c(KMnO4)、c(H2C2O4)浓度不变或确保溶液总体积不变 (2分)
Ⅱ.(1)否 ,KMnO4溶液呈紫色,达滴定终点紫色不再褪去。(2分)
(2)b (2分) (3)75% (3分)
本题解析:Ⅰ.(1)要研究催化剂对化学反应速率的影响,则其它条件应该是相同的,所以应该用实验①和②。同样要研究温度对化学反应速率的影响,其它条件也应该是相同的,所以应该用实验①和③。
(2)对比实验①和④可知硫酸的浓度是不同的,所以可以研究硫酸的浓度或氢离子浓度对化学反应速率的影响。由于实验①中硫酸的体积是2ml,所以为确保①和④组对比实验中c(KMnO4)、c(H2C2O4)浓度不变或确保溶液总体积不变,需要加入1ml水。
Ⅱ.(1)由于酸性KMnO4溶液呈紫色,达滴定终点紫色不再褪去,所以不需要另加指示剂。
(2)酸性高锰酸钾溶液具有强氧化性,能腐蚀橡胶,所以应该用酸式滴定管。
(3)15.00 mL高锰酸钾的物质的量是0.2000mol/L×0.015L=0.003mol,得到电子是0.003mol×5=0.015mol,所以根据电子得失守恒可知,草酸钠的物质的量是0.015mol÷2=0.0075mol,质量是0.0075mol×134g/mol=1.005g,因此质量分数为1.005g÷1.34g×100%=75%。
本题难度:困难
3、选择题 化学反应速率最主要取决于?(?)。
A.是否使用催化剂
B.反应物的性质
C.反应的温度
D.反应的压强
参考答案:B
本题解析:化学反应速率最主要取决于反应物的性质,即内因,B正确,强于选项都是外因,答案选B。
点评:该题的关键是明确影响反应速率的因素分为内因和外因两种,但决定性因素是内因,有利于培养学生的逻辑推理能力和灵活应变能力。
本题难度:简单
4、选择题 已知:Na2S2O3+H2SO4=Na2SO4+SO2↑+S↓+H2O,下列各组实验中,反应速率最快的是
组号
| 反应温
度/℃
| Na2S2O3
| H2SO4
| H2O体积/mL
|
体积/mL
| 浓度/mol・L-1
| 体积/mL
| 浓度/mol・L-1
|
A
| 10
| 5
| 0.2
| 5
| 0.1
| 10
|
B
| 10
| 5
| 0.1
| 5
| 0.1
| 10
|
C
| 30
| 5
| 0.1
| 5
| 0.1
| 10
|
D
| 30
| 5
| 0.2
| 5
| 0.2
| 10
|
?
参考答案:D
本题解析:在相同条件下,温度越高、反应物的浓度越大,反应速率越快,据此可以判断。A、B中温度均小于C、D中温度,反应速率不是最快的。C和D相比反应物的浓度是D中大于C中,因此反应速率最快的是实验D组,答案选D。
本题难度:一般
5、选择题 某一达到化学平衡状态的可逆反应:mA(g)+nB(g) pC(g)+qD(g),如图2-27表示A的转化率α(A)同温度、压强的关系。分析该图示可以得出的结论是(?)
pC(g)+qD(g),如图2-27表示A的转化率α(A)同温度、压强的关系。分析该图示可以得出的结论是(?)
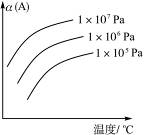
图2-27
A.正反应吸热,m+n>p+q
B.正反应吸热,m+n<p+q
C.正反应放热,m+n>p+q
D.正反应放热,m+n<p+q
参考答案:A
本题解析:由图所示:压强不变时升温,α(A)增大,说明升温使平衡向正反应方向移动,则正反应为吸热反应;当温度不变时,加压也使α(A)增大,说明加压使平衡向正反应方向移动。则正反应为气体总体积缩小的反应,即m+n>p+q。
本题难度:简单