微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、实验题 (8分)用如下图所示(夹持仪器省略)的装置进行实验,将液体A逐滴加入到固体B中,回答下列问题:
①下图中D装置在实验中的作用是__________________________________________;
②若A为浓盐酸,B为KMnO4,C为淀粉KI溶液,旋开E后,C中的现象为____________________,反应的化学方程式是______________________________________;
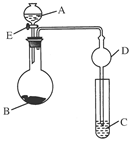
③若A为浓硫酸(70%),B为Na2SO3,C为酸性KMnO4溶液,旋开E后,C中的现象为________________________________________________________________________,
反应的化学方程式是_______________________________________________;
④若A为30%H2O2溶液,B为MnO2;C为H2S饱和溶液,旋开E后,C中的现象为________________________________________________________________________,
反应的化学方程式是__________________________________________________;
⑤若A为稀盐酸,B为大理石,C为Na2SiO3溶液,旋开E后,C中的现象为________________,反应的化学方程式是__________________________________;
⑥上图所示装置有多种用途,请举例(除题中之外):A为________,B为________,C中盛________,旋开E后,C中的现象为________________,反应的化学方程式是________________________________________________________________________。
参考答案:①防止溶液倒吸"②溶液先变蓝后褪色"2KI+Cl2===2KCl+I2、5Cl2+I2+6H2O===2HIO3+10HCl"③高锰酸钾溶液的紫红色褪去"5SO2+2H2O+2KMnO4===K2SO4+2MnSO4+2H2SO4"④溶液中产生淡黄色固体O2+2H2S===
2S↓+2H2O"⑤产生白色胶状沉淀"CO2+H2O+Na2SiO3===Na2CO3+H2SiO3↓"⑥浓氨水"生石灰"硝酸银溶液和葡萄糖溶液"试管壁上出现银镜 CH2OH(CHOH)4CHO+
2Ag(NH3)2OHCH2OH(CHOH)4COOH+2 Ag↓+4NH3↑+H2O
本题解析:同一装置,多种用途,考查学生灵活运用知识的能力、开拓学生视野。
本题难度:一般
2、实验题 无水氯化铝是白色晶体,易吸收水分,在178℃升华,装有无水氯化铝露置于潮湿空气中会爆炸并产生大量白雾,工业上由金属与氯气作用或由无水氯化氢气体与熔融Al作用而制得,某课外活动小组在实验室内通过下列装置(如下图)制取少量纯净的无水氯化铝。

试回答以下问题:
(1)装置A中反应的化学方程式??
(2)为使实验成功,A和B间需要加适当的装置,请将它画在框内,并注明其中盛放的药品。如果A产生的气体直接进入B中,实验产生的不良后果是?。
(3)进行实验时,应先点燃(填写字母,下同)?处的酒精灯,然后再点燃?
?处的酒精灯。
(4)在C处可以收集到纯净的氯化铝,原因是?。
(5)装置D的作用是?。
参考答案:(1)MnO2+4HCl(浓) 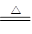 MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O
(2)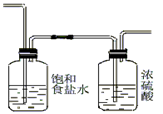 AlCl3与H2O反应而爆炸;(3)A ; B (4) AlCl3易升华
AlCl3与H2O反应而爆炸;(3)A ; B (4) AlCl3易升华
(5)吸收多余的Cl2且防止水蒸气进入C使AlCl3发生水解
本题解析:(1)浓盐酸和二氧化锰在加热条件下能发生氧化还原反应生成氯化锰、氯气、水,所以装置A中反应的化学方程式为MnO2+4HCl(浓) 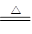 MnCl2+Cl2↑+2H2O。
MnCl2+Cl2↑+2H2O。
(2)浓盐酸具有挥发性,所以生成的氯气中含有氯化氢和水蒸气。氯化氢和铝能反应生成氢气,氢气和氯气混合会发生爆炸。另外氯化铝极易吸水,无水氯化铝露置于潮湿空气中会爆炸并产生大量白雾,所以在通过B之前需要除去氯化氢和水蒸气,使用的试剂分别是饱和食盐水和浓硫酸。
(3)由于装置中还含有空气,因此要利用氯气将空气排除,以及防止空气氧化金属铝,所以进行实验时,应先点燃A处的酒精灯,然后再点燃B处的酒精灯。
(4)由于AlCl3易升华,所以在C处可以收集到氯气。
(5)氯气有毒,污染环境,所以需要尾气处理;另一方面氯化铝极易吸水,因此碱石灰的的主要是吸收多余的Cl2且防止水蒸气进入C使AlCl3发生水解。
点评:该题是高考中的常见考点和题型,属于中等难度试题的考查,试题综合性强,侧重对学生能力的培养和解题方法的指导与训练,旨在考查学生灵活运用基础知识解决实际问题的能力,有利于培养学生的逻辑推理能力和规范严谨的实验设计能力,提高学生的学科素养。该类试题综合性强,理论和实践的联系紧密,有的还提供一些新的信息,这就要求学生必须认真、细致的审题,联系所学过的知识和技能,进行知识的类比、迁移、重组,全面细致的思考才能得出正确的结论。
本题难度:一般
3、实验题 溴苯是一种常用的化工原料。实验室制备溴苯的实验步骤如下:
步骤1:在a中(装置如右下图所示)加入15mL无水的苯和少量铁屑,再将b中4.0mL液溴慢慢加入到a中,充分反应。
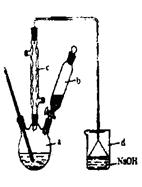
步骤2:向a中加入10mL水,然后过滤除去未反应的铁屑。
步骤3:滤液依次用10mL水8mL 10%的NaOH溶液,10mL水洗涤,分液得粗溴苯。
步骤4:向分出的粗溴苯中加入少量的无水氯化钙、静置、过滤即得粗产品。
?
| 苯
| 溴
| 溴苯
|
密度/gcm-3
| 0.88
| 3.10
| 1.50
|
沸点/℃
| 80
| 59
| 156
|
水中的溶解度
| 微溶
| 微溶
| 微溶
|
(1)仪器a的名称是?。
(2)将b中的液溴慢慢加入到a中,而不能快速加入的原因是?。
(3)仪器c的作用是冷凝回流,回流的主要物质有?。(填化学式)
(4)步骤3中第一次用10mL水洗涤的主要操作步骤为?。
(5)步骤4得到的粗产品中还含有杂质苯。已知苯、溴苯的有关物理性质如左上表,则要进一步提纯粗产品,还必须进行的实验操作名称是?。
(6)若步骤4的粗产品经进一步精制得到6.5mL的溴苯。则该实验中溴苯的产率是?。
参考答案:(1)三颈烧瓶(2)防止反应放出的热使C6H6、Br2挥发而影响产率
(3)C6H6、Br2
(4)将滤液置于分液漏斗中,加入10 mL水,充分振荡后静置分液(分离出上层物质待用)
(5)蒸馏(6)80%
本题解析:(1)根据仪器的构造可知,应该是三颈烧瓶。
(2)由于反应是放热的,且苯和液溴都是易挥发的,所以目的是防止反应放出的热使C6H6、Br2挥发而影响产率。
(3)根据(2)的分析可知,回流的物质是C6H6、Br2。
(4)溴苯不溶于水,所以操作是将滤液置于分液漏斗中,加入10 mL水,充分振荡后静置分液(分离出上层物质待用)。
(5)苯、溴苯的沸点相差较大,通过蒸馏即可。
(6)苯的质量是15×0.88=13.2g,液溴是3.1×4=12.4g。所以根据方程式可知,苯是过量的,因此应该生成溴苯是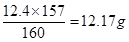 。实际生成溴苯是6.5×1.5=9.75g,所以产率是
。实际生成溴苯是6.5×1.5=9.75g,所以产率是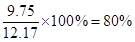
本题难度:一般
4、实验题 (11分)某课外活动小组欲制取次氯酸钠和氯化钠的混合溶液,为提高次氯酸钠含量,采用如图所示装置。图中瓶乙盛饱和食盐水,瓶丙盛浓硫酸,分液漏斗A中盛浓盐酸。(据资料显示:Cl2与NaOH在不同温度下,产物不同。在较高温度下易生成NaClO3)
试回答:
(1)烧瓶B中盛________,试管C中盛________。
(2)有同学认为可以省去某些装置,你认为怎样:
①能否省去乙装置________(填“能”或“不能”),理由是
________________________________________________________________________;

②能否省去丙装置________(填“能”或“不能”),理由是
_____________________________________________________________________________________。
(3)有同学认为还必须添加某些装置,你认为怎样?________(填“需要”或“不需要”),如果你认为需要,请指出该装置的作用是_______________________________________________。
(4)丁装置中冰水的作用是____________________________________________________________。
参考答案:(1)MnO2"NaOH溶液
(2)①不能 HCl气体进入C中,消耗NaOH,降低NaClO的产量
②能"少量水蒸气进入C中,不影响反应
(3)需要"防止氯气污染空气
(4)防止氯气与NaOH溶液在较高温度时发生其他反应
本题解析:本题主要考查次氯酸钠和氯化钠的混合液的制取,涉及到对实验装置的分析与讨论。(1)装置甲是制取氯气的装置,B中是MnO2,C中是氢氧化钠溶液;(2)①乙装置的作用是除去Cl2中混有的HCl,HCl气体进入C中,与氢氧化钠反应,影响次氯酸钠的产量;②丙装置的作用是干燥Cl2,其实在这里Cl2不需要干燥;(3)Cl2有毒,需要添加尾气处理装置;(4)冰水的作用是控制温度。
本题难度:一般
5、计算题 (5分)实验室用8.7g的MnO2与足量的浓盐酸制取氯气:求生成氯气的体积(标准状况)和被氧化的HCl的物质的量。
参考答案:(5分)
MnO2+4HCl=Mn Cl2+Cl2↑+2H2O?被氧化的HCl
87?22.4? 2
8.7? V (Cl2)?n(HCl)
V (Cl2)="2.24L?"
n(HCl)=0.2mol
本题解析:略
本题难度:一般