微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 美国宇航局科学家2010年3月1日说,美国雷达发现,月球北极40多个陨石坑含有6亿吨水冰。对下列实验指定容器中的水,其解释没有体现水的主要作用的是
[? ]
实验装置
解释
A.
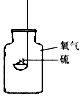
硫在氧气中燃烧
集气瓶中的水:吸收放出的热量
B.

测定空气中氧气含量
量筒中的水:通过水体积的变化测出氧气体积
C.

铁丝在氧气中燃烧
集气瓶中的水:冷却溅落熔融物,防止集气瓶炸裂
D.

排水法收集氢气
集气瓶中的水:水先将集气瓶中的空气排尽,后便于观察氢气何时收集满
参考答案:A
本题解析:
本题难度:简单
2、实验题 15分)某兴趣小组同学设计了如下装置(其中夹持仪器、加热仪器及冷却水管没有画出),用加热苯甲酸、浓H2SO4和乙醇混合物的方法来制备苯甲酸乙酯,并检验反应的部分副产物。且苯甲酸乙酯的沸点为213℃,乙醚的沸点为34.6℃。

⑴关闭活塞a、接通竖直冷凝管的冷凝水,给A加热30分钟,制备。仪器E的作用是?。
⑵上述反应的副产物可能有:乙醚(CH3CH2-O-CH2CH3)、乙烯、SO2、水等。
①打开活塞a,在竖直冷凝管上方塞上塞子,通过B、C、D装置检验SO2和乙烯。已知C中盛放的试剂是NaOH溶液,B、D中应盛放的试剂依次分别是?。
②有同学拟通过红外光谱仪鉴定所得产物中是否含有“-CH2CH3”,来确定副产物中存在乙醚。请你对该同学的观点进行评价:?。
⑶通过下列实验方案,可以提纯苯甲酸乙酯。
①为除去产品中杂质,先将三口烧瓶中残液倒入盛有冷水的烧杯中,并加入?。
②用分液法可分离上述有机层和水层,分液完成后,取出有机层的操作是?。
③向锥形瓶中加入适量豆粒大小的无水氯化钙干燥剂,至醚层澄清透明;过滤得醚层,然后将醚层加入到干燥的蒸馏烧瓶中蒸馏,蒸馏过程中控制的温度为?。
参考答案:⑴冷凝回流(或导气兼冷凝))?⑵①品红、溴水(或酸性KMnO4溶液或溴的CCl4溶液)?②不可以,产物苯甲酸乙酯也含有“-CH2CH3”?⑶饱和Na2CO3溶液?将有机层从上口倒入一个干燥的锥形瓶中? 34.6℃
本题解析:(1)由于反应中的有机试剂在加热过程中易挥发,为提高产率,冷凝管除导气作用外主要是冷凝回流。
(2)①乙烯检验一般通过溴水褪色或酸性高锰酸钾溶液褪色,SO2的检验一般用品红试剂,而SO2也可使溴水褪色或酸性高锰酸钾溶液褪色,故需要先检验SO2,再用碱液吸收,再检验乙烯
(3)提纯苯甲酸乙酯,可用碱液或饱和Na2CO3溶液除去酸性水溶性物质,再用进行分液,最后再对有机层进行蒸馏分离即可。
本题难度:一般
3、实验题 氢溴酸在医药和石化工业上有广泛用途。下图是模拟工业制备氢溴酸粗产品并精制的流程:
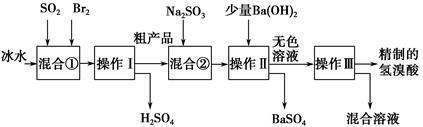
根据上述流程回答下列问题:
(1)混合①中发生反应的离子方程式为________________________________。
(2)混合①中使用冰水的目的是_______________________________________。
(3)操作Ⅲ一般适用于分离________混合物。(填序号)
a.固体和液体? b.固体和固体
c.互不相溶的液体? d.互溶的液体
(4)混合②中加入Na2SO3的目的是____________________________________。
(5)纯净的氢溴酸应为无色液体,但实际工业生产中制得的氢溴酸(工业氢溴酸)带有淡淡的黄色。于是甲乙两同学设计了简单实验加以探究:
甲同学假设工业氢溴酸呈淡黄色是因为其中含有Fe3+,则用于证明该假设所用的试剂为________,若假设成立可观察到的现象为__________________;乙同学假设工业氢溴酸呈淡黄色是因为其中含有________________,其用于证明该假设所用的试剂为____________。
参考答案:(5)KSCN溶液 溶液变成红色 Br2 CCl4(其他合理也可)
本题解析:SO2与Br2在水中发生氧化还原反应,反应放热,为防止溴蒸发,用冰水降温。操作Ⅰ、Ⅲ均是蒸馏,操作Ⅱ是过滤。混合②中加入Na2SO3的目的是除去粗产品中未反应完的溴。检验Fe3+常用KSCN溶液;工业氢溴酸中可能含有溴而呈淡黄色,可用四氯化碳萃取而证明。
本题难度:困难
4、实验题 (6分) 氯气是一种重要的化工原料,在生产和生活中应用十分广泛。在实验室可用二氧化锰固体和浓盐酸制氯气。
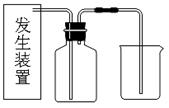
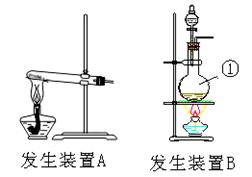 ?
?
(1)请为该实验选择合适的发生装置???(填A或B),写出仪器①的名称?
(2)当集气瓶中收集满氯气时,可以观察到气体呈???色。尾气通常用???吸收。
(3)工业上常用电解饱和食盐水制取氯气,试写出该反应的化学方程式:
?。
参考答案:(1)B 、圆底烧瓶。?(2)黄绿,NaOH溶液。
(3)2NaCl+2H2O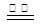 2NaOH+H2↑+Cl2↑
2NaOH+H2↑+Cl2↑
本题解析:(1)实验室制氯气是典型的固液加热制取气体,所以应该选用B装置。仪器①的名称叫圆底烧瓶。(2)氯气是黄绿色气体,尾气用NaOH溶液来吸收。(3)电解饱和食盐水制取氯气的化学方程式为:2NaCl+2H2O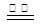 2NaOH+H2↑+Cl2↑
2NaOH+H2↑+Cl2↑
点评:本题考查学生的实验能力,非常基础。
本题难度:一般
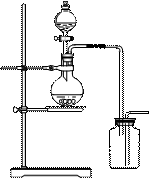
5、实验题 (12分)I.下图是某学生设计的制取和收集某些气体的实验装置(可加热)。
(1)该装置在加入反应物前,应首先进行的实验操作是?。
(2)下列气体的制取中,若用排空气法收集,可使用该装置制备和收集的是(选填编号,下同)__________若用排水法收集(集气瓶中充满水),可使用该装置制备和收集的是? ___________。
①用Zn与稀盐酸反应制H2?
②用CaCO3与稀盐酸反应制CO2?
③用固体NaOH和浓氨水制NH3?
④用Cu与稀HNO3反应制NO
⑤用MnO2与双氧水反应制O2
⑥浓硫酸与铜片反应制SO2
⑦用MnO2与浓盐酸反应制Cl2
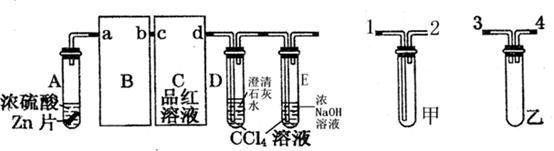
II. 某校化学研究性学习小组对浓硫酸与金属锌的反应进行探究。首先按图组装好实验装置,然后取一定量的浓硫酸与足量Zn充分反应,微热试管A,实验过程中先观察到C、D中均有气泡产生,D中开始出现浑浊,后浑浊消失,随后气泡量逐渐减少,品红溶液褪色,反应较长时间后,C、D中的气泡量又 会明显增加。
会明显增加。
试回答:
(1)从甲、乙中选择合适的装置填入B、C中,并进行正确连接,a接?、?接b,c接?、?接d;
(2)D、E试管中CCl4溶液的作用是防止溶液倒吸,该实验中起到同样作用的装置是____________;
(3)能证明浓硫酸具有强氧化性的实验现象为?;
(4)反应较长时间后气泡量又会明显增加的原因是?;
(5)D中浑浊消失的离子方程式为?。
参考答案:I、(1)检查装置气密性 (1分) (2)①③;①④⑤;(各2分)
II、(1)3或4? 4或3(1分)? 1? 2(1分)
(2)乙(填B也得分)(1分)
(3)C中品红溶液褪色(1分)?
(4)浓H2SO4变成 稀H2SO4,与Zn反应放出H2(1分)
稀H2SO4,与Zn反应放出H2(1分)
(5)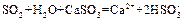 (2分)
(2分)
本题解析:略
本题难度:一般