微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 (4分)A.B.C是三种互不同族也不同周期的短周期元素,原子序数总和为26,它们可以结成一种三原子化合物,这种化合物的化学式是________。
参考答案:HClO(4分)
本题解析:“不同周期”,则三者分别在3个周期,那么一定有H(在第一周期),另两个会分别在2、3周期,
在第2周期的元素原子序数介于3到10之间,在第3周期的元素原子序数介于11到18之间,再利用“两者的原子序数总和为25”,即可求解;
本题难度:一般
2、选择题 下图是部分短周期主族元素原子半径与原子序数的关系图,下列说法正确的是
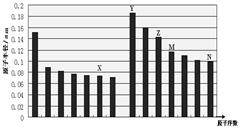
A.最高价含氧酸的酸性:M>N
B.离子半径:X<Y
C.X和Y形成的化合物中一定含有含离子键
D.化合物MX2能与碱反应,不能与任何酸反应
参考答案:C
本题解析:图中14种元素分别位于第二、三周期第IA~VIIA族,由于同周期主族元素的原子半径随原子序数的增大而减小,同主族元素的原子半径随原子序数的增大而增大,则图中X、Y、Z、M、N分别为氧、钠、铝、硅、氯元素。M、N分别是硅、氯,非金属性:Si<Cl,最高价氧化物酸性:H2SiO3<HClO4,故A项错误;X、Y分别为氧、钠,O2―、Na+都具有28电子层结构,离子半径与核电荷数成反比,则氧离子的半径比钠离子的半径大,故B项错误;X、Y分别为氧、钠,二者形成的化合物分别为氧化钠、过氧化钠,Na2O只有离子键、Na2O2既有离子键又有共价键,故C项正确;X、M分别为氧、硅,二者形成的二氧化硅是酸性氧化物,与碱能反应,氢氟酸是唯一能与二氧化硅反应的酸,故D项错误。
本题难度:一般
3、选择题 已知aAn+、bB(n+1)+、cCn-、dD(n+1)-具有相同的电子层结构,关于A、B、C、D四种元素的叙述正确的是
A.这四种离子的电子层结构相同,因而离子的性质也就相同
B.原子序数:b>a>c>d
C.最高价氧化物对应水化物的碱性:B>A
D.气态氢化物的稳定性:D>C
参考答案:B
本题解析:A、这四种离子的电子层结构相同,但离子的性质还与离子的核电荷数有关,错误; B、原子中核电荷数等于核外电子数,阳离子中核外电子数等于核电荷数减去离子所带电荷数,阴离子中核外电子数等于核电荷数加上离子所带电荷数。aAn+、bB(n+1)+、cCn-、dD(n+1)-电子层结构相同,有如下关系: a-n=b-(n+1)=c+n=d+n+1,故b>a>c>d,正确;C、因b>a故在周期表中B的位置在A的后边,B的金属性比A的弱,最高价氧化物对应水化物的碱性: A>B,错误;D、因c>d故在周期表中C的位置在D的后边,C的非金属性比D的强,气态氢化物的稳定性C>D,错误。
本题难度:一般
4、选择题 下列叙述正确的是(?)
A.16 8O2和18 8O2互为同位素,性质相似
B.将MgCI2溶液蒸干灼烧仍得到MgCI2
C.明矾和漂白粉常用于自来水的处理,两者的作用原理相同
D.C(石墨)=C(金刚石) △H>0,所以石墨比金刚石稳定
参考答案:D
本题解析:A中微粒是单质氧气,不是核素,不可能是同位素。氯化镁在溶液中存在水解平衡,加热促进水解,同时促进生成物氯化氢的挥发,进一步促进水解,所以最终得到的是氢氧化镁,灼烧得到氧化镁。明矾溶于水,发生水解。生成的氢氧化铝和悬浮于水中的泥沙形成絮状不溶物沉降下来,水水澄清。漂白粉具有强氧化性,溶于水能杀死水中的细菌等,所以二者的原理是不相同的。反应吸热,说明石墨的能量低于金刚石的,因为能量越低越稳定,所以选项D是正确的。答案选D。
本题难度:一般
5、选择题 X元素原子的质量数为m,核内中子数为n,则Wg X2+?离子含有的电子的物质的量约为(?)
A.(m+n+2)w/m mol
B. (m-n+2)w/m mol
C. (m+n-2)w/m mol
D. (m-n-2)w/m mol
参考答案:D
本题解析:中子数和质子数之和是质量数,所以该原子的质子数是m-n,所以X2+?的电子数为m-n+2。则Wg X2+?离子含有的电子的物质的量约为
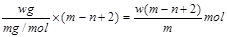 ,因此答案选D。
,因此答案选D。
本题难度:简单