微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、实验题 (14分)如何防止铁的腐蚀是工业上研究的重点内容。为研究铁锈蚀的影响因素,某同学做了如下探究实验:
序号
| 内容
| 实验现象
|
1
| 常温下将铁丝放在干燥空气中一个月
| 干燥的铁丝表面依然光亮
|
2
| 常温下将铁丝放在潮湿空气中一小时
| 铁丝表面依然光亮
|
3
| 常温下将铁丝放在潮湿空气中一个月
| 铁丝表面已变得灰暗
|
4
| 将潮湿的铁丝放在常温的氧气流中一小时
| 铁丝表面略显灰暗
|
5
| 将潮湿的铁丝放在高于常温的氧气流中一小时
| 铁丝表面已变得灰暗
|
6
| 将浸过氯化钠溶液的铁丝放在高于常温的氧气流中一小时
| 铁丝表面灰暗程度比实验5严重
|
回答以下问题:
⑴上述实验中发生了电化学腐蚀的是(填实验序号)?,在电化学腐蚀中,负极反应是_______________?,正极反应是_______________??。
⑵由该实验可知,可以影响铁锈蚀速率的因素是?。
⑶下列对金属制品采取的防护方法不正确的是?(填序号)。
A.在电线的外面包上一层塑料层?
B.在自行车钢圈上镀上一层金属铬
C.在海轮的铁制外壳上焊上铜块
2、选择题 根据下列元素的电离能数据(单位:kJ/mol),你认为最外层有2个电子的是
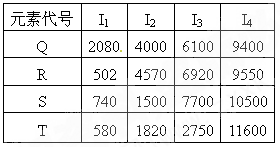
A.Q
B.R
C.S
D.T
3、选择题 右图是模拟电化学反应装置图。下列说法正确的是(?)
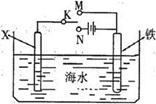
A.若X为碳棒,开关K置于N处,会加快铁的腐蚀
B.若X为锌,开关K置于N处,则X极上有黄绿色气体生成
C.若X为碳棒,开关K置于M处,则铁电极的电极反应式为:Fe-3e-=Fe3+
D.若X为锌,开关K置于M处,则总反应方程式为:2Zn+O2+2H2O=2Zn(OH)2
4、简答题 有关钢铁腐蚀与防护的说法正确的是( )
A.析氢腐蚀和吸氧腐蚀,负极均是Fe发生还原反应Fe-2e→Fe2+
B.镀层破损后,镀锡铁板的镀层仍能对铁制品起保护作用,比镀锌铁板更耐腐蚀
C.在海轮外壳连接锌块,保护外壳不受腐蚀是采用了牺牲阳极的阴极保护法
D.将地下输油钢管与外加直流电源的正极相连以保护它不受腐蚀
5、计算题 (9分)由铜片、锌片和200 mL稀H2SO4组成的原电池中,若锌片发生电化学腐蚀,当铜片上放出3.36 L(标准状况)气体时,硫酸恰好全部作用完。试计算:
(1)产生这些气体消耗了多少克锌?
(2)有多少个电子通过了导线?
(3)200 mL稀H2SO4的物质的量浓度是多少?