��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ��4mol?A�����2mol?B���������Ϊ2L���ܱ������л�ϣ�����һ�������·�����Ӧ��2A��g��+B��g��?xC��g��������2s����A�����ʵ���Ϊ2.8mol��C�����ʵ���Ũ��Ϊ0.6mol/L�����м���˵������2s��������A��ʾ��ƽ����Ӧ����Ϊ0.3mol/��L?s������2s��������B��ʾ��ƽ����Ӧ����Ϊ0.6mol/��L?s������2sʱ����B��ת����Ϊ70%����x=2��������ȷ���ǣ�������
A���٢�
B���٢�
C���ڢ�
D���ۢ�
�ο��𰸣�B
���������
�����Ѷȣ�һ��
2������� ��һ���¶��£�10L�ܱ������м���5.0mol SO2��4.5mol O2����10min��Ӧ��ƽ��ʱO2��Ũ��Ϊ0.30mol/L������㣨д��������̣���
��1��10min��SO2��ת���ʣ�
��2�������ڷ�Ӧǰ��ƽ��ʱ��ѹǿ֮�ȣ���������ȣ���
��3��ƽ�ⳣ��K��
�ο��𰸣�10L�ܱ������м���5.0molSO2��4.5molO2��c��SO2��=0.50mol/L��c��O2��=0.45mol/L����10min��Ӧ��ƽ��ʱO2��Ũ��Ϊ0.30mol/L��
��? 2SO2+O2
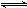
?2SO3
��ʼŨ�ȣ�mol/L��?0.50?0.45?0
�仯Ũ�ȣ�mol/L��?0.30?0.15?0.30
ƽ��Ũ�ȣ�mol/L��?0.20?0.30?0.30
��1��10min��SO2��ת����Ϊ0.3mol/L0.5mol/L��100%=60%����10min��SO2��ת����Ϊ60%��
��2��ͬ��ͬѹ�£����ʵ�����ѹǿ�����ȣ��������ڷ�Ӧǰ��ƽ��ʱ��ѹǿ֮��Ϊ5mol+4.5mol(0.2+0.3+0.3)��10mol=19��16��
�������ڷ�Ӧǰ��ƽ��ʱ��ѹǿ֮��Ϊ19��16��
��3��ƽ�ⳣ��K=c(SO3)2c(O2)��c(SO2)2=(0.3mol/L)2(0.2mol/L)2��0.3mol/L=7.5L/mol����ƽ�ⳣ��KΪ7.5L/mol��
���������
�����Ѷȣ�һ��
3��ѡ���� ��ӦX��g����Y��g��  2Z��g������H<0���ﵽƽ��ʱ������˵����ȷ���ǣ�������
2Z��g������H<0���ﵽƽ��ʱ������˵����ȷ���ǣ�������
A����С���������ƽ�������ƶ�
B�����������Z�IJ�������
C������c��X����X��ת��������
D�������¶ȣ�Y��ת��������
�ο��𰸣�D
������������ݸ÷�Ӧ���ص���ƽ���ƶ�ԭ�����������
A���÷�ӦΪ��Ӧǰ���������ʵ�������ķ�Ӧ��ƽ�ⲻ��ѹǿӰ�죬��С���������ƽ�ⲻ�ƶ���B.��������ʹƽ���ƶ������ı����IJ��ʡ�C.����c��X����ƽ�������ƶ���Y��ת��������X������ת���ʷ�����С��D.�÷�Ӧ������Ӧ�Ƿ��ȷ�Ӧ�������¶ȣ�ƽ�������ƶ���Y��ת��������
�㲦��֪ʶ����ѧƽ���Ӱ�����ء�ת�������⡣������������ѧ֪ʶ�����ͽ����ѧƽ������������������Ѷȣ��еȡ�
�����Ѷȣ�һ��
4��ѡ���� ���ڿ��淴Ӧ2SO2 (g)+ O2(g)  ?2SO3(g)?DH <0��һ���¶�����ƽ����ΪK������˵����ȷ����
?2SO3(g)?DH <0��һ���¶�����ƽ����ΪK������˵����ȷ����
A������SO2��ת����Kֵһ������
B����СѹǿKֵ��С
C�������¶�Kֵ����
D��KֵԽ��SO2ת����Խ��
�ο��𰸣�D
������������黯ѧƽ�ⳣ�����й��жϡ���ѧƽ�ⳣ��ֻ�뷴Ӧ���¶��й�ϵ������ѡ��A��B���Ǵ���ģ�����Ӧ�Ƿ��ȷ�Ӧ�������¶�ƽ�����淴Ӧ������У�ƽ�ⳣ���Ǽ�С�ģ�ѡ��C����ȷ����ѧƽ�ⳣ������һ�������£������淴Ӧ�ﵽƽ��״̬ʱ��������Ũ�ȵ���֮���ͷ�Ӧ��Ũ�ȵ���֮���ı�ֵ�����ѡ��D��ȷ����ѡD��
�����Ѷȣ���
5������� ��14�֣�
(1)һ�������£������Ϊ3 L���ܱ������У�һ����̼��������Ӧ���ɼ״�(����ΪCu2O/ZnO)��CO(g)��2H2(g)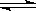 CH3OH(g)��
CH3OH(g)��
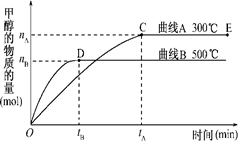
�������������ͼ��������и��⣺
�ٷ�Ӧ�ﵽƽ��ʱ��ƽ�ⳣ������ ʽK��?��
ʽK��?��
������ �¶ȣ�Kֵ??(�������С�����䡱)
�¶ȣ�Kֵ??(�������С�����䡱)
��2��һ���¶��£���3 mol A�����1 mol B����ͨ��һ�ܱ������У��������·�Ӧ��3A(g) + B(g) 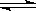 ?xC(g) ����д���пհף�����������̶�Ϊ2 L����Ӧ2 minʱ���ʣ��0.6 mol B��C��Ũ��Ϊ0.4 mol/L��
?xC(g) ����д���пհף�����������̶�Ϊ2 L����Ӧ2 minʱ���ʣ��0.6 mol B��C��Ũ��Ϊ0.4 mol/L��
��x=?
������Ӧ��4 min�ﵽƽ�⣬ƽ��ʱC��Ũ��________ 0.8 mol/L(����ڡ�������?�ڡ���С�ڡ�)��
��ƽ�������У�C���������Ϊ22%����B��ת������______________��
��3�����û�ѧ��Ӧԭ���о��������ȵ��ʼ��仯����ķ�Ӧ����Ҫ���塣
�ٺϳɰ���ӦN2 (g)+3H2(g) 2NH3(g)�����ں��¡���ѹ��������ƽ����ϵ��ͨ���������ƽ��?��
2NH3(g)�����ں��¡���ѹ��������ƽ����ϵ��ͨ���������ƽ��?�� ������������ҡ���������ʹ�ô�����������Ӧ�ġ�H________������� ����С�� ���ı䡱����
������������ҡ���������ʹ�ô�����������Ӧ�ġ�H________������� ����С�� ���ı䡱����
����������Ѱ����ʵĴ����͵缫���ϣ���N2��H2Ϊ�缫��Ӧ���HCl��NH4ClΪ�������Һ��������ȼ�յ��,�ŵ�����У���Һ��笠�����Ũ����������д���õ�ص�������Ӧʽ? ?��
?��
�ο��𰸣���14�֣�
��1����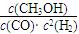 ?�ڼ�С
?�ڼ�С
��2����2(2��)��<��2�֣���36����2�֣�
��3���������ı䣨2�֣���N2+8H++6e��=2NH4+��2�֣�
�����������
�����Ѷȣ�һ��